Щелочные металлы контрольная работа
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
1. Решите цепочку превращений
Na _ _+O2 ___-> A _ _+Na ___-> B ___+H2O - > NaOH __ +? __> Na 2 SO 4
2. Запишите уравнение реакции взаимодействия калия с кислородом и расставьте коэффициенты методом электронного баланса.
3. Какой объем водорода может быть получен при растворении в воде 94,5 г рубидия, содержащего 10 % примесей, если выход водорода составил 90% от теоретически возможного?
K _ _+O2 ___-> A _ _+K ___-> B ___+H2O - > KOH __ +? __-> KNO 3
2. Запишите уравнение реакции взаимодействия рубидия с кислородом и расставьте коэффициенты методом электронного баланса.
3. Какой объем водорода может быть получен при растворении в воде 22,5 г лития, содержащего 5 % примесей, если выход водорода составил 80% от теоретически возможного?
Li _ _+O2 ___-> A ___+H2O - > B __ +HCI __-> C __ +? __-> Li 2 SO 3
2. Запишите уравнение реакции взаимодействия натрия с кислородом и расставьте коэффициенты методом электронного баланса.
3. Какой объем водорода может быть получен при растворении в воде 81,5 г калия, содержащего 3 % примесей, если выход водорода составил 95% от теоретически возможного?
Rb _ _+O2 ___-> A _ _+Rb ___-> B ___+H2O - > RbOH __ +? __-> Rb 3 PO 4
3. Какой объем водорода может быть получен при растворении в воде 49,5 г натрия, содержащего 7 % примесей, если выход водорода составил 80% от теоретически возможного?
Na _ _+O2 ___-> A _ _+Na ___-> B ___+H2O - > NaOH __ +? __> NaNO 3
K _ _+O2 ___-> A _ _+K ___-> B ___+H2O - > KOH __ +? __-> K 2 SO 4
Li __+O 2 ___-> A ___+H 2 O - > B __ +HNO 2 __-> C __ +? __-> Li 2 S
Rb _ _+O2 ___-> A _ _+Rb ___-> B ___+H2O - > RbOH __ +? __-> RbCI
По теме: методические разработки, презентации и конспекты

Контрольная работа по теме "Металлы"
Контрольно-измерительные тесты по теме "Металлы" .

Контрольная работа 9 класс по теме "Металлы"
В эту работу входит:-характеристика элемента-генетическая цепь-задача .

Контрольная работа по теме "Металлы" (9 класс, коррекция)
Контрольная работа в 9 классе завершает тему «Металлы», она рассчитана на академический час и позволяет проверить качество знаний, умений и навыков у учащихся коррекционных классов.Работа .
Конспект урока по теме:"Металлы, их положение в Периодической системе, строение атомов металлов. Общие физические свойства металлов."
Урок по химии в 9 классе. Тема: «Общие химические свойства металлов. Взаимодействие металлов со сложными веществами. Электрохимический ряд напряжений металлов».
Урок по химии в 9 классе. Тема: «Общие химические свойства металлов. Взаимодействие металлов со сложными веществами. Электрохимический ряд напряжений металлов». Цели урока учебные, воспитательные и р.

План урока химии по теме "Положение металлов в Периодической системе химических элементов Д.И. Менделеева, строение их атомов. Строение металлов – простых веществ. Физические свойства металлов".
План урока № 62 (9кл). Положение металлов в Периодической системе химических элементов Д.И. Менделеева, строение их атомов. Строение металлов – простых веществ. Физические свойства металлов.

Технологическая карта урока "Контрольная работа №1 Металлы""
Дифференцированный подход стал основой при разработке данной контрольной работы, что позволяет учащимся самостоятельно определить степень освоения раздела "Металлы" уже на первом этапе.
Контрольная работа по теме "Щелочные металлы"
А 1. Сколько электронов содержат на внешнем энергетическом уровне атомы щелочных металлов:
а) два б) один в) три г) четыре
А 2. В химических реакциях металлический натрий проявляет:
а) окислительные свойства б) восстановительные свойства
в) кислотные свойства г) основные свойства
А 3. В ряду химических элементов Na → K → Rb → Cs → Fr металлические свойства:
а) усиливаются б) ослабевают
в) не изменяются г) изменяются периодически
А 4. Какой из щелочных металлов при взаимодействии с кислородом образует оксид:
а) натрий б) рубидий в) калий г) литий
А5. Соединения щелочных металлов с водородом называется:
а) галогениды б) гидроксиды в) гидриды г) нитриды
А 6. Какой из металлов в лаборатории хранят под слоем керосина:
а) железо б) калий в)медь г) цинк
А 7. Карбонат какого щелочного металла имеет техническое название «поташ»:
а) натрия б) калия в) лития г) цезия
А 8. На воздухе легче всего окисляется:
а) натрий б) литий в) рубидий г) калий
А 9. Какая формула соответствует гидроксиду и оксиду лития:
а) Li OH и Li 2 O б) Li ( OH )2 и LiO в) Li 2 O и Li ( OH )2 г) Li ( OH )2 и Li O 2
А 10. Какой металл поддерживает работу сердечной мышцы:
а) литий б) кальций в) калий г) рубидий
Часть Б (на выбор одно задание)
Б 1. Закончите уравнения реакций, характеризующие химические свойства металла. Дайте название продуктам реакции.
1) Na + Cl 2 =
2) Na + O 2 =
3) Na + H 2 =
4) Na + S =
5) Na + N 2 =
Na + H 2 O =
Б 2. Получите металл ( Al ) из его оксида ( Al 2 O 3) (пирометаллургия) всеми способами:
( восстановление углем С, угарным газом СО, водородом Н2, более активным металлом)
Часть С (на выбор одно задание)
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
К → К2О2→ К2О → КОН → К2 S О4
С 2. Решите задачу:
Какой объем кислорода потребуется для его взаимодействия с натрием количеством вещества 0,3 моль?
КОНТРОЛЬНАЯ РАБОТА
Тема: «Щелочные металлы». Вариант №2
А 1. В 1 группе главной подгруппе от лития к цезию металлические свойства
А 2. На внешнем энергетическом уровне атомы щелочных металлов содержат электронов:
А 3. Какой из металлов в лаборатории хранят под слоем керосина:
а) цинк б) магний в) медь г) натрий
А 4. В химических реакциях металлический калий проявляет:
а) окислительные свойства б) кислотные свойства
в) восстановительные свойства г) основные свойства
А 5. Калий взаимодействует с кислородом. Продукт этой реакции называется:
а) гидроксиды б) оксид в) гидрид г) пероксид
А 6. Карбонат какого щелочного металла имеет техническое название «глауберова соль»:
а) лития б) калия в) натрия г) цезия
А 7. Какая формула соответствует оксиду и гидроксиду калия:
а) К2 O 2 и К O Н б) Са O и Са( OH )2 в) К2 O и К( OH ) г)Са( OH )2 и Са O 2
А 9. Какой металл поддерживает работу сердечной мышцы:
А 10. При взаимодействии какого металла с водой одним из продуктов будет щелочь:
а) железо б) калий в) серебро г) цинк
Б 1. Закончите уравнения реакций, характеризующие химические свойства металла. Дайте названия продуктам реакций.
1) К + Cl 2 =
2) К + O 2 =
3) К + H 2 =
4) К + S =
5) К + N 2 =
6) К + H 2 O =
Б 2. Получите металл ( Fe ) из его оксида ( Fe 2 O 3) (пирометаллургия) всеми способами:
( восстановление углем С, угарным газом СО, водородом Н2, более активным металлом).
С1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Na → Na 2О2 → Na 2О→ Na ОН → Na 2 S О4
С2. Решите задачу:
Какой объем кислорода потребуется для его взаимодействия с калием количеством вещества 0,2 моль?
Получите свидетельство о публикации сразу после загрузки работы

Получите бесплатно свидетельство о публикации сразу после добавления разработки
Олимпиады «Осенний фестиваль знаний 2022»

Комплекты учителю

Качественные видеоуроки, тесты и практикумы для вашей удобной работы
Вебинары для учителей

Бесплатное участие и возможность получить свидетельство об участии в вебинаре.
Проверочная работа № 1 « Общая характеристика металлов, сплавы, Щелочные и Щелочноземельные металлы.»
Проверочная работа разработаны в тестовой форме для тематического контроля по школьному курсу химии 9 класса к авторской программе О.С. Габриэляна.
Содержимое разработки
Проверочная работа № 1 « Общая характеристика металлов, сплавы, Щелочные и Щелочноземельные металлы.»
1. Электронное строение внешнего энергетического уровня атомов щелочных металлов:
А) n S 1 В) n S 2 P 1 Б) n S 2 Г) n S 2 P 2
2. Степень окисления щелочных металлов:
А) - 1 В) – 2 Б) +1 Г) +2
3. Выберите ряд элементов, относящихся к щелочным металлам:
А ) Ca, Zn, Cl В ) Li, Na, Rb Б ) Mg, K, Al Г ) Cr, Mn, Co
4. Самый лёгкий щелочной металл: А) Na В) K Б) Li Г) Cs
5 Наиболее ярко выраженные металлические свойства у: А)Mg B)Ra Б)Ва Г)Са
6. С какими из перечисленных веществ реагируют щелочноземельные металлы:
А) S В) H 2 O Б) Cl 2 Г) Fe
7.Гидроксид кальция реагирует с: ( выберите все правильные ответы)
8.Сплав меди и олова 1) Бронза 2) чугун 3) сталь 4) дюралюминий
9/ Природный мел- это: А) CaSO4 Б) MgSO4 В)CaCO3 Г)ВаSO4
10/Способ получения натрия и калия: А) алюмотермия В) электролиз Б) магниетермия Г) пиролиз
11. Щелочные металлы находятся в природе в виде
А) оксидов Б) сульфидов В) в самородном виде Г) солей
В1. Установите соответствие между формулой вещества и названием
Формула вещества название
А) Ca(OH)2 1) едкое кали
Б) NaHCO3 2) известковое молоко
В) KOH 3) жженая магнезия
B 2 Верны ли следующие суждения о свойствах элементов IIA группы и строении их атомов?
А. Активность металлов возрастает от бериллия к радию.
Б. Атомы металлов IIA группы имеют электронную конфигурацию внешнего слоя ns 2 np 2.
1) оба суждения неверны 2) верно только А 3) верно только Б 4) верны оба суждения
C 1 Используя метод электронного баланса, составьте уравнение реакции
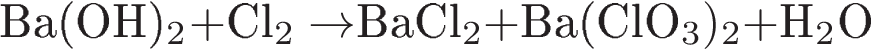
Определите окислитель и восстановитель.
С2 Рассчитайте массу осадка, который выпадет при взаимодействии избытка карбоната калия с 17,4 г раствора нитрата бария
Система оценивания:
0 – 9 баллов – «2» 10 – 16 баллов – «3»
17 – 20 баллов – «4» 21 – 24 баллов – «5»
Проверочная работа № 1 « Общая характеристика металлов, сплавы, Щелочные и Щелочноземельные металлы.» ВАРИАНТ 2
1.Электронное строение внешнего энергетического уровня атомов щелочноземельных металлов.
А ) n S 1 В ) nS 2 P 1 Б ) nS 2 Г ) n S 2 P 2
2/ Степень окисления бериллия, магния и щелочноземельных металлов.
А) +2 В) +4 Б) - 2 Г) - 4
3/ Выберите ряд элементов, относящихся к щелочноземельным металлам:
А) Ba, Sr, Ca В) Mg, K, Al Б) Na, K, Li Г) Ca, Mg, Ве
4/ Является радиоактивным металлом А) магний В) стронций Б) барий Г) радий
5/ Наиболее ярко выраженные металлические свойства у: А) лития В) калия Б) натрия Г) рубидия
6. С какими из перечисленных веществ реагируют щелочные металлы: А) S В) H 2 O Б) Cl 2 Г) Fe
7.С каким из перечисленных ниже классов веществ не взаимодействуют щелочи:
8/Сплав железа с углеродом 1)Бронза 2) чугун 3) латунь 4) дюралюминий
9/Где применяется соединения магния MgSO 4
А)в машиностроении Б)для получения серной кислоты В)для получения стекла
10. Где содержат щелочные металлы?
1) под слоем воде 2) под слоем керосина 3) под слоем спирта
4) под слоем смеси воды и спирта
11 . Какое свойство нехарактерно для вещества NaOH
А) разъедает бумагу Б) дает ожоги на коже В) твердое Г) жидкое
B 1 Установите соответствие между формулой вещества и его техническим названием:
Б) BaSO4 2) кристаллическая сода
В) NaOH 3) глауберова соль
Г) MgSO4 4) горькая соль
Д) CaCO3 5) баритова каша
B 2 Верны ли следующие суждения о магнии и его соединениях?
А. Магний реагирует и с кислотами, и со щелочами.
Б. Оксид магния является основным оксидом.
C1 Используя метод электронного баланса, составьте уравнение реакции
Определите окислитель и восстановитель
C 2 Решите задачу. К раствору силиката калия массой 20,53 г прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.
проверочные и зачетные задания по темам "Щелочные металлы" и "Щелочноземельные металлы"
тест по химии (9 класс) по теме
I задание: выберите правильный ответ
- Все элементы главной подгруппы I группы периодической системы относятся к …
1) типичным окислителям
2) переходным элементам
2. Все ѕ – элементы, кроме водорода и гелия, являются…
1) газообразными веществами, без цвета и запаха
2) жидкостями при комнатной температуре
3. Атомы щелочных элементов имеют …
1) по одному электрону на внешнем уровне
2) по два электрона на внешнем уровне
3) полностью заполненный внешний уровень
4. Атомы щелочных элементов имеют …
1) возможность терять два внешних электрона, образуя катион
со степенью окисления +2
2) возможность терять единственный внешний электрон, образуя катион
со степенью окисления +1
3) возможность приобретать один электрон на внешний уровень, образуя
анион со степенью окисления -1
5. Франций, завершающий I группу, является…
1) очень твёрдым
2) самым распространённым в земной коре
6. Все ѕ – металлы очень активны и поэтому…
1) самовоспламеняются на воздухе
2) хранятся в воде
3) хранятся в керосине
7.Поскольку внешние электроны ѕ – металлов легко переходят к другим элементам,
все эти металлы являются…
1) типичными изоляторами
2) сильными восстановителями
8. Все щелочные металлы горят в атмосфере кислорода, образуя…
1) пероксиды состава Ме 2 О 2
2) оксиды состава Ме 2 О
3) пероксиды Ме 2 О 2 и оксиды Ме 2 О
9. Оксид калия может быть получен в результате реакции…
1) К 2 О 2 + 2К === 2К 2 О 3) 2КО 2 + О 3 === К 2 О + 3О 2 ↑
2) КО 2 + 3К === 2К 2 О
10. Все ѕ – металлы соединяются с водородом уже при незначительном нагревании,
11. При взаимодействии щелочных металлов с водой образуютя…
1) гидриды и кислород
2) щёлочи и водород
3) пероксиды и водород
12. Сульфатом калия является вещество, имеющее формулу…
13. Металлы I группы главной подгруппы будут взаимодействовать с кислотами те, …
1) которые в ряду напряжения металлов стоят после Н
2) которые в ряду напряжения металлов стоят до Н
3) будут реагировать все
14. Пара металлов, обладающих наиболее сходными свойствами:
15. Реакция замещения возможна между…
1) серебром и железом
2) хлоридом железа и серебром
3) нитратом меди (I I) и серебром
4) нитратом серебра и железом
I I задание: Осуществите превращения, запишите соответствующие уравнения реакций.
Nа → Nа 2 О 2 → NаО 2 → Nа 2 СО 3 → Nа Сl
I I I задание: закончите уравнения реакций
- Все элементы главной подгруппы I I группы периодической системы относятся к …
3. Атомы щелочноземельных элементов имеют …
4. Атомы щелочноземельных элементов имеют …
5. Радий, завершающий I I группу, является…
8. Все щелочноземельные металлы горят в атмосфере кислорода, образуя…
1) оксиды состава МеО
2) гидроксиды состава МеОН
3) оксиды Ме 2 О
9. Оксид кальция может быть получен в результате реакции…
1) 2Са + О 2 === 2СаО 3) 2КО 2 + О 3 === К 2 О + 3О 2 ↑
2) Са + 2Н 2 О = Са(ОН) 2 + Н 2
10. Все ѕ – металлы соединяются с водородом, образуя…
11. При взаимодействии щелочноземельных металлов с водой образуютя…
2) основания и водород
12. Сульфатом кальция является вещество, имеющее формулу…
13. Металлы I I группы главной подгруппы будут взаимодействовать с кислотами те, …
15. Оксиды щелочноземельных металлов имеют общую молекулярную формулу…
Мq СО 3 → МqСl 2 → Мq (ОН) 2 → МqО →Мq
Щелочные и щелочноземельные металлы
- Напишите уравнения реакций, позволяющих осуществить следующие превращения:
Са → СаО → СаСО 3 → Са(NО 3 ) 2
- Окислительные или восстановительные свойства проявляют щелочные металлы при взаимодействии с неметаллами? Напишите два уравнения реакций, подтверждающих ваш ответ.
- Напишите уравнения реакций, позволяющих осуществить следующие превращения: Nа → NаОН → NаНСО 3
- Напишите уравнения реакций взаимодействия: а) натрия с серой; б) кальция с хлором; в) лития с водой.
- Окислительные или восстановительные свойства проявляют щелочноземельные металлы при взаимодействии с неметаллами? Напишите два уравнения реакций, подтверждающих ваш ответ.
- Напишите уравнения реакций, позволяющих осуществить следующие превращения: NаНСО 3 → Nа 2 SО 4 → Nа 2 О

Общая характеристика металлов (проверочная работа)
Проверочная работа состоит из 2-х частей. Часть А- химический диктант. Часть В- нужно написать уравнения реакций.
Проверочный тест по теме "Щелочные металлы"
Тест по теме "Щелочные металлы" предназначен для проверки знаний после прохождения темы. Тест включает вопросы по строению атомов щелочных металлов и свойствам щелочных металлов.
проверочные работы по теме "Металлы" 9 класс
Данные проверочные работы предназначены для текущего контроля усвоения знаний обучающимися. В заключении проводится контрольная работа.

Проверочная работа по теме "Щелочные металлы" ( 9класс)
Раздаточный материал для пров. работы по теме "Щелочные металлы" (4 варианта). Дополнительные задания (составление электронного баланса, ионных уравнений) учитель формулирует устно.
Проверочная работа "Щелочноземельные металлы и их соединения" (9класс)
Раздаточный материал для проверочной работы (4 варианта). Дополнительные задания можно дать устно.
Проверочная работа по теме "Сравнение металлов" 11 класс,базовый уровень
Проверочная работа по теме "Сравнение металлов" 11 класс,базовый уровень.

Проверочная работа по теме"Металлы" для 9 класса
Данная проверочная работа по теме "Металлы" предназначена для учащихся 9 класса, как контроль в конце 1 четверти.
Проверочная работа по теме "Щелочные металлы" ( 9класс)
методическая разработка по химии (9 класс) на тему
| Вложение | Размер |
|---|---|
| shchel._met._i_ikh_soedineniya.docx | 16.93 КБ |
Подтяните оценки и знания с репетитором Учи.ру
ЩЕЛОЧНЫЕ МЕТАЛЛЫ И ИХ СОЕДИНЕНИЯ
Написать уравнения реакций между веществами:
5) NaOH + H 2 SO 4
6) LiOH + Cu(NO 3 ) 2
3) Li 2 O + N 2 O 5
6) KOH + H 3 PO 4
4) Li 2 O + H 2 O
7) LiOH + N 2 O 5
4) LiOH + H 2 CO 3

История России. Проверочная работа по теме"Гражданская война" (9класс)
Проверочная работа по истории России для 9 класса по теме "Гражданская война" состоит из 3 вариантов. Данная работа проводится после полного изучения темы. Для удобства пользования количество варианто.
Проверочная работа "Сравнение свойств элементов" (8, 9класс)
Раздаточный материал для проверочной работы (8вариантов) можно использовать в разных темах 8кл и в 9кл.
Читайте также:
