Молярная масса металла формула
1. Ознакомить студентов с основными химическими законами и единицами массы.
2. С помощью математической обработки подученных студентами экспериментальных данных сделать вывод о названии металла, данного для работы и его положении в периодической таблице Д.И. Менделеева.
ОСНОВНЫЕ ПОНЯТИЯ
Вспомним основные частицы вещества:
Молекула – наименьшая частица вещества, обладающая его химическими свойствами и состоящая из атомов. Атом – наименьшая частица элемента, обладающая его химическими свойствами. Химический элемент можно определить как вид атомов, характеризующийся определенной совокупностью свойств.
Простейшим примером сказанному может служить молекула хлористого водорода ( HCl ). Водород и хлор, вступая в реакцию, теряют свои свойства, характерные для газообразных Н2 и Cl2, поэтому считается, что в состав хлористого водорода входят элементы – водород и хлор.
Масса атомов и молекул выражается в атомных единицах массы (а.е.м.), принятых в 1961 г. За одну атомную единицу массы принимается 1/12 часть массы атома изотопа углерода 12 С. Таким образом, масса атома или молекулы любого вещества представляется относительной величиной, показывающей, во сколько раз масса данного атома (молекулы) тяжелее выбранной атомной единицы массы.
Так, относительная атомная масса цинка (Ar) равна 65.38 а.е.м., относительная молекулярная масса воды (Mr) равна 1,008 ∙ 2 + 15,9994 = 18,0154 а.е.м. и т.д.
Однако при решении задач и в расчетах по уравнениям реакций гораздо чаще пользуются понятием «моль».
Моль – это количество вещества, содержащее столько молекул, атомов, ионов, электронов или других структурных единиц, сколько содержится атомов в 12 граммах изотопа углерода 12 C.
Применяя слово «моль», необходимо в каждом случае точно указывать, какие единицы входят в данное вещество. Существует понятия «моль атомов», «моль молекул» и т.д. Масса одного моля взятого вещества называется его молярной массой. Она выражается в г/моль.
Числовое значение молярной массы вещества в г/моль равно относительной молекулярной массе Mr, если вещество состоит из молекул, или относительной атомной массе Ar, если вещество состоит из атомов. Например, молярная масса атомарного кислорода равна ~16 г/моль, молекулярного кислорода ~32 г/моль.
Моль любого вещества содержит совершенно одинаковое количество структурных единиц. Это число называет числом Авогадро, его значение принимают равным 6,02·10 23 .
Часто в химических расчетах используется понятие эквивалента.
Эквивалентом вещества называется такое его количество, которое соединяется без остатка с 1 молем атомов водорода или замещает то же количество атомов водорода в химических реакциях.
Например, в соединениях HCl, H2S и NH3 эквивалент элементов хлора, серы и азота соответственно равен 1 моль, ½ моля и 1/3 моля. Масса одного эквивалента называется его эквивалентной массой или молярной массой эквивалента.Выражается в г/моль.
Так, в приведенных примерах эквивалентные массы хлора, серы и азота легко подсчитать, используя атомные массы этих элементов, они соответственно равны mэ(Cl) = 35,5 г/моль; mэ(S) = 32:2 = 16 г/моль; mэ(N) = 14:3 = 4,7 г/моль. Из разобранных примеров видно, что эквивалентная масса элемента находится из соотношения
Эквивалентная масса или .
Понятие об эквивалентах и эквивалентных массах распространяется также на сложные вещества. Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода или вообще с одним эквивалентом любого другого вещества.
1. Эквивалентная масса оксида складывается из значений эквивалентных масс, составляющих оксид элементов.
а) Эквивалентные массы металла и кислорода в оксиде ZnO, соответственно, равны половине молярных масс атомов:
б) Валентность серы в оксиде SO3 равна 6, следовательно
2. Эквивалентная масса кислоты равна её молярной массе, деленной на основность кислоты (число атомов водорода в молекуле кислоты).
а) Молярная масса HNO3 равна 63 г/моль. Кислота одноосновная, следовательно .
б) Молярная масса H3PO4 равна 98 г/моль. Основность равна 3.
3. Эквивалентная масса основания равна его молярной массе, деленной на валентность металла, образующего основание.
Молярная масса Mg(OH)2 равна 58 г/моль, валентность цинка 2. .
4. Эквивалентная масса соли равна отношению её молярной массы к произведению валентности металла на число его атомов в молекуле.
а) Молярная масса Na2CO3 равна 106 г/моль. Валентность металла I, число его атомов 2.
5. Эквиваленты одних и тех же сложных веществ и их эквивалентные массы могут иметь различные значения, если их рассматривать не как отдельные вещества, а составные части химических реакций, в которых они участвуют.
| H2CO3 + 2NaOH = Na2CO3 + 2H2O | (1) |
| H2CO3 + NaOH = NaHСO3 + H2O | (2) |
эквивалент H2CO3 и его масса зависит от количества атомов водорода, участвующих в реакции и соответственно равны:
| , – по уравнению (1); | (1) |
| , – по уравнению (2); | (2) |
| Cr(OH)3 + 2HCl = CrOHCl2 + 2H2O; | (3) |
| Cr(OH)3 + 3HCl = CrCl3 + 3H2O; | (4) |
| , – по уравнению (3); | (3) |
т.к. в реакции было замещено только две гидроксидных группы на кислотный остаток.
| , – по уравнению (4); | (4) |
т.к. произошло замещение всех трех гидроксогрупп.
Известно несколько способов определения эквивалента.
I. Прямое или непосредственное определение эквивалента из соединения элементов с водородом или кислородом.
Пример 1. Рассчитать эквивалент железа в его оксиде FeO.
Эквивалент кислорода по определению равен ½ моля атомов, эквивалентная масса кислорода равна 16 : 2 = 8 г/моль. В данном соединении на ½ моля атомов кислорода приходится столько же, т.е. ½ моля атомов железа. Следовательно, эквивалент железа в данном оксиде равен ½ моля, а его эквивалентная масса 56 : 2 = 28 г/моль.
II. Определение эквивалента с помощью закона эквивалентов.
Закон эквивалентов (эквивалентных масс), предложенный в 1803-1814 гг. Дальтоном и Рихтером: Элементы и вещества соединяются друг с другом, а также замещают друг друга, в химических реакциях в строго определенных весовых количествах, прямо пропорциональных их эквивалентам.
Математическая запись закона такова:
где m1 и m2 – массы взаимодействующих элементов или веществ, г;
mЭ1 и mЭ2 – соответственно эквивалентные массы этих веществ, г/моль.
Пример 2. Определить эквивалентную и молярную массы 3-валентного металла, зная, что 0,52 г его при окислении образуют 0,98 г оксида.
Решение. В соответствии с законом эквивалентов
Массу кислорода определим по разности масс оксида и металла
mO = 0,98 – 0,52 = 0,46 г.
Эквивалентная масса кислорода известна, она равна 8 г/моль.
Т.к. валентность металла равна 3, то его молярная масса
Пример 3. Вычислить эквивалентную массу металла, если в его хлориде массовая доля хлора 79,78 %, эквивалентная масса хлора равна 53,45 г/моль.
Решение. Массовая доля w металла в хлориде равна
w = 100 - 79,78 = 20,22 %.
Согласно закону эквивалентов, отношение массы металла и массы хлора в соединении должно быть равно отношению их эквивалентных масс
Пример 4. Определите молярную массу двух валентного металла, если 14,2 г оксида этого металла образуют 30,2 г сульфата металла.
Эквивалентная масса сульфата металла равна .
Согласно закону эквивалентов
Т.к. валентность металла равна 2, то его молярная масса равна:
A = 27,5 · 2 = 55 г/моль.
III. Если в химической реакции одно из участвующих веществ находится в газообразном состоянии, то запись закона эквивалентов выражается формулой
где соответственно m(Me) и mэ(Me) – масса металла и его эквивалентная масса, а V и Vэ - объем вступившего в реакцию газа и объем эквивалентной массы этого газа.
Для расчета объемов реагирующих газов необходимо знание Закона Авогадро и его следствий.
Закон Авогадро (1911): В равных объемах различных газов при постоянных температуре и давлении содержится одинаковое число молекул.
Следствия из закона Авогадро:
1. Один моль любого газа при нормальных условиях (н.у.) –температура 0 ºС и давление 760 мм.рт.ст. занимает один и тот же объем равный 22,4 литра. Этот объем называют – молярным объемом газа VМ = 22,4 л/моль.
2. Один моль любого газа содержит одно и то же число молекул, а именно NA = 6,02 · 10 23 моль -1 .
3. Относительная плотность одного газа по другому равна отношению их молярных (M) или относительных молекулярных масс
На основании этих следствий можно рассчитать количество вещества
Пример 5. Рассчитать массу 3 л хлора, взятого при н.у.
Решение. Т.к. молярная масса хлора (Cl2) равна 35,5 ∙ 2 = 71 г/моль то из соотношения (IV) легко найти массу искомого объема
Пример 6. Сколько молей и сколько молекул содержится в 2,2 г углекислого газа? Какой объем они занимают при н.у.?
Решение. Т.к. молярная масса углекислого газа (СО2) равна 44 г/моль, то
Найдем объем газа при н.у.
Пример 7. Определите массу молекулы газа, если масса 2 л газа (н.у.) равна 0,357 г.
Решение. Исходя из молярного объема газа определим молярную массу газа
Число молекул в 1 моль любого вещества равно постоянной Авогадро. Следовательно, масса молекул газа (m) равна
Первое следствие из закона Авогадро позволяет рассчитать объемы эквивалентных масс различных газов:
Так, если эквивалентная масса водорода равна 1,008 г/моль, то её объем равен
Подобным образом находится объем эквивалентной массы кислорода, который оказывается равным
Пример 8. При растворении 0,506 г металла в серной кислоте выделилось 100,8 мл водорода, измеренного при н.у. Определить эквивалентную массу металла.
Задачу можно решить двумя способами:
а) прямой подстановкой данных в формулу (II).
б) используя формулу (I), откуда
, где mэ(H) = 1,008 г/ моль.
Для решения задачи в этом случае надо найти m(H2). Согласно следствию из закона Авогадро
Теперь найденное значение m(H2) подставим в формулу (I)
Значения эквивалентных масс позволяют определить атомную массу металлов по формуле:
A = тэ · В, (V)
где В – валентность металла
А – его атомная масса, в г/моль.
Если же валентность металла неизвестна, то атомную массу можно определить через удельную теплоемкость. В данных расчетах используется правило Дюлонга и Пти: Произведение удельной теплоемкости простого твердого вещества на его атомную массу для большинства элементов приблизительно одинаково. Полученная величина имеет среднее значение, равное 26,8 Дж/моль·К (6,3 кал/моль·град). Она носит название атомной теплоемкости металлов (СА) и представляет собой количество тепла, необходимого для нагревания 1 моля атомов металла на один Кельвин. Математически это правило имеет вид
| СА = А · С ~ 26,8 Дж/моль·К | (VI) |
где С – удельная теплоемкость металла, Дж/г·К;
А – атомная масса взятого металла, г/моль.
Под удельной теплоемкостью понимается то количество тепла, которое необходимо затратить для нагревания 1 г вещества на 1 Кельвин.
Пример 9. При окислении 0,16 г металла образовалось 0,223 г оксида. Вычислить точную атомную массу металла, зная, что удельная теплоемкость 0,635 Дж/г·К.
Решение. По правилу Дюлонга и Пти найдем приближенное значение атомной массы данного металла
По формуле (1) найдем эквивалентную массу этого металла. Масса кислорода 0,223 г. – 0,16 г. = 0,063 г.
Зная приближенную атомную массу металла и его эквивалентнуюмассу, можно найти валентность этого металла.
Молярная масса

Для решения многих задач по химии нужно знать количество молекул или других частиц, необходимое для реакции. Однако оперировать столь малыми числами неудобно, поэтому ученые ввели новые величины. В этой статье вы познакомитесь с такими понятиями, как моль, количество вещества, молярная масса в химии.
О чем эта статья:
Что такое моль
Прежде чем говорить о том, как найти молярную массу вещества, определимся с понятием «моль». Его ввели как искусственную величину для упрощения расчетов. Это количество вещества, в котором содержится столько же мельчайших частиц, сколько в 12 г одного из изотопов углерода — C12.
Для всех химических веществ это количество одинаково и представляет собой число Авогадро 6,02 · 10 23 . Постоянная Авогадро обозначается NA, а измеряется в моль -1 .
Число Авогадро — это количество молекул, ионов или других мельчайших частиц в 1 моле вещества.
NA = 6,02 · 10 23 моль -1 .
Историческая справка
В 1811 году химик Амедео Авогадро предположил, что если взять два равных объема газов в равных значимых условиях (при одинаковой температуре и давлении), то количество молекул в этих объемах тоже будет одинаковым. Опираясь на свою гипотезу, он определил атомные и молекулярные массы многих веществ, а также рассчитал количество атомов в молекулах воды, оксидов азота и т. д. Однако в научных кругах гипотеза Авогадро долго не находила понимания. Общепринятой она стала только в 1860 году.

Что такое молярная масса
Молярная масса — это масса одного моля вещества, она измеряется в граммах деленных на моль (г/моль). Данная величина представляет собой отношение массы вещества к его количеству, которое измеряется в молях.
Как обозначается молярная масса: М.
, где — это масса вещества, а — количество вещества.
Единица измерения молярной массы: г/моль.
Несмотря на то, что в 1 моле любого химического вещества содержится одинаковое количество молекул (и оно равно числу Авогадро), молярные массы разных веществ отличаются. Все потому, что отличаются атомы, которые входят в состав этих молекул. В частности, разница между ними заключается в относительной атомной массе (Ar) — например, Ar(Mg) = 24, а Ar(Hg) = 200. Сейчас станет ясно, какое это имеет значение.
Как определить молярную массу
Данная величина тесно связана с такими понятиями, как относительные атомная и молекулярная массы. Именно относительные, потому что абсолютную массу молекулы или атома вещества в химии не используют для решения задач — это слишком малые величины.
Относительная атомная масса вещества (Ar) показывает, во сколько раз его атом больше 1/12 атома углерода. Это значение для каждого химического элемента можно увидеть в таблице Менделеева.
Относительная молекулярная масса (Mr) складывается из Ar каждого атома в молекуле вещества с учетом индексов. Она показывает, на сколько масса молекулы больше 1/12 атома углерода.
, где — это количество атомов.
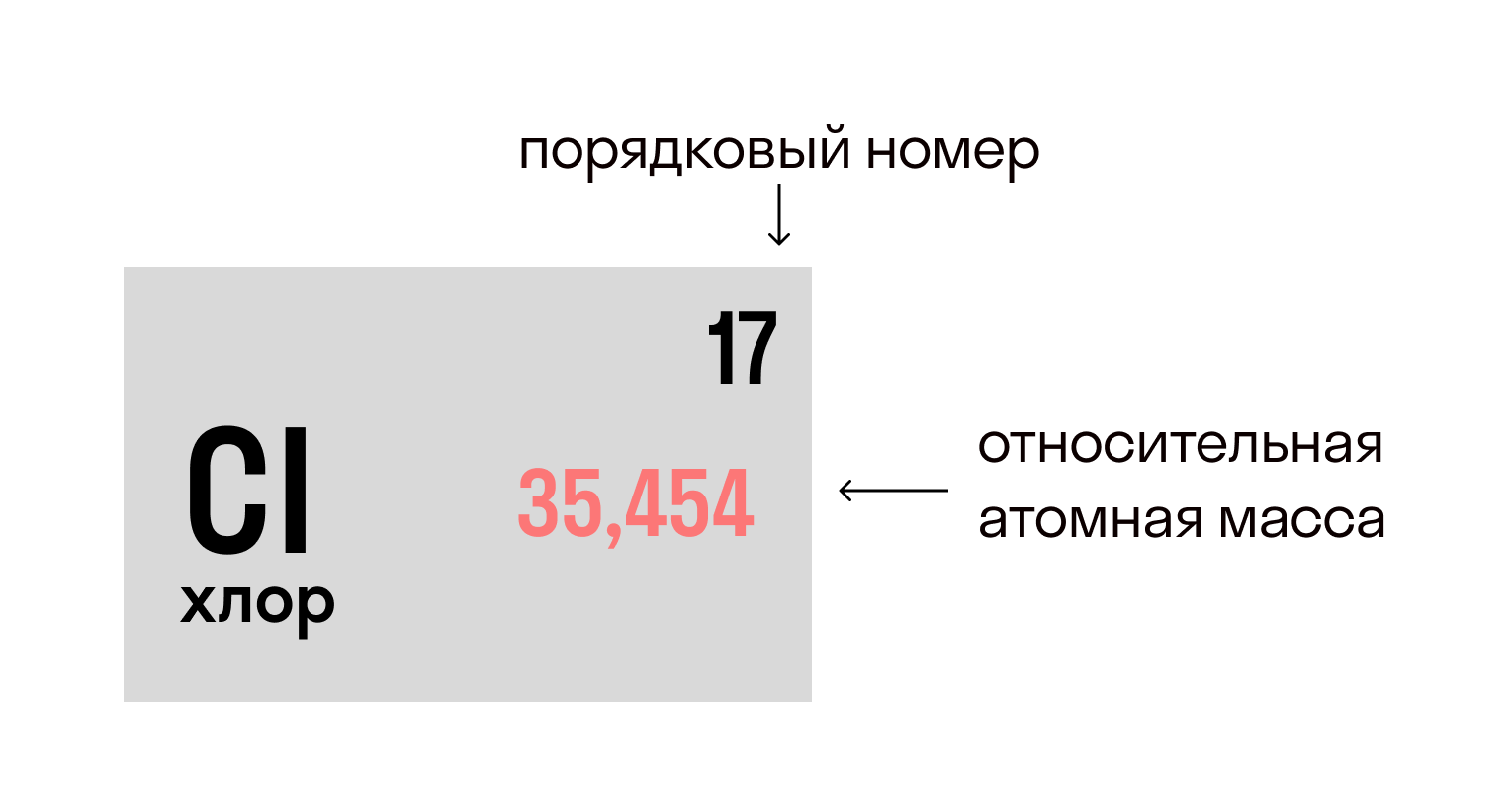
Разберемся на примерах.
В молекуле хлорида натрия NaCl есть 1 атом натрия и 1 атом хлора, при этом Ar(Na) = 23, Ar (Cl) = 35,5.
Mr(NaCl) = 23 + 35,5 = 58,5.
В молекуле NaNO2 есть 1 атом натрия, 1 атом азота и 2 атома кислорода.
Собственно, для вычисления молярной массы больше ничего и не требуется.
Молярная масса вещества численно равна относительной молекулярной массе. Но путать эти два понятия не стоит — у них разный физический смысл. Молярная масса характеризует 1 моль, а относительная молекулярная — 1 молекулу.
Количество вещества
Из предыдущих формул понятно, что молярная масса и количество вещества тесно связаны. Рассмотрим эту связь подробнее. Начнем с того, что количество вещества может обозначаться как латинской буквой , так и греческой буквой (ню). Международное обозначение — , но не стоит удивляться, встретив в формулах любую из этих букв.
В формуле нахождения молярной массы мы обозначили количество вещества через :
Пользуясь этим, можно найти количество вещества (в молях), если нам известны его абсолютная и молярная масса.
Пример 1
Как определить, какое количество вещества включают 350 г сульфата бария BaSO4?
Мы помним, что M = Mr (значение молярной массы равно значению относительной молекулярной).
Подставим значение молярной массы в формулу:
Есть и еще одна формула количества вещества, которая позволяет найти его, если известно число молекул или других структурных единиц.
, где — число структурных единиц, — число Авогадро.
Пример 2
Допустим, некий объем CaCO3 содержит 3,01 · 10 23 молекул. Как найти количество вещества, соответствующее данному объему?
Воспользуемся формулой моль.
Молярный объем
Выше мы находили количество вещества через молярную массу, но для газов это можно сделать и через молярный объем. Согласно закону Авогадро количество любого газа, равное 1 моль, будет занимать один и тот же объем, если газы рассматриваются при одинаковой температуре и давлении.
При стандартных физических условиях — температуре 0°С и давлении 1 атм или 760 мм ртутного столба, 1 моль газа занимает объем 22,4 л.
Молярный объем — это объем газа, взятого в количестве 1 моль. Он обозначается Vm.
При нормальных условиях Vm = 22,4 л/моль.
Значения молярного и фактического объема газа помогают найти количество вещества.
, где — фактический объем газа, а — молярный объем.
Сколько молей содержится в 120 литрах газа при нормальных условиях?
Рассчитаем по формуле моль.
Ответ: 120 литров любого газа при стандартных условиях содержат 5,36 моль.
Относительная плотность одного газа по другому
Иногда для решения задачи нужно знать, как найти молярную массу газа, о котором сообщается лишь его плотность по воздуху или по другому газу. Это возможно, если знать формулу относительной плотности, которая обозначается буквой D.
, где и — некие газы.
Как определить, во сколько раз угарный газ плотнее водорода?
Для начала найдем молярную массу CO и H2:
Ответ: угарный газ в 14 раз плотнее водорода.
Как посчитать молярную массу газа х, о котором известно, что он в 10 раз плотнее углекислого газа CO2?
Подсчитаем для начала молярную массу углекислого газа:
Ориентируясь на формулу относительной плотности, произведем расчет молярной массы искомого газа х.
М(х) = D(х/CO2) · M(CO2) = 10 · 44 = 440 г/моль.
Ответ: у данного газа молярная масса 440 г/моль.
Примеры задач
Итак, мы разобрались, как находить молярную массу жидкости, газа или твердого тела и как это понятие связано с количеством вещества, а также с относительной плотностью одного газа по другому. Чтобы закрепить знания, посмотрите, как эти сведения применяются в решении задач.
Задача 1
Известно, что 300 г неустановленного вещества содержат 12,04 · 10 23 молекул. Чему равна молярная масса данного вещества?
N(х) = 12,04 · 10 23 .
Найдем количество вещества моль.
Подставим количество вещества в формулу :
Ответ: молярная масса данного вещества 150 г/моль.
Задача 2
Какой объем займет водород в количестве 0,7 моль?
По формуле мы можем найти объем .
Зная, что молярный объем при обычных условиях составляет 22,4 л/моль, вычислим фактический объем водорода:
Ответ: объем водорода составляет 15,68 литров.
Задача 3
В порции оксида серы SO3 содержится 8,356 · 10 23 атомов кислорода. Какова масса этой порции?
N(O) = 8,356 · 10 23 .
Для решения задачи нам подходит формула , т. е. . Но для начала нужно найти количество вещества.
Мы знаем, что в одной молекуле SO3 есть 3 атома кислорода, исходя из этого можно вычислить количество молекул в порции оксида:
Зная количество молекул, рассчитаем количество вещества:
Теперь можно узнать молярную массу SO3:
M(SO3) = 32 + 16 · 3 = 80 г/моль.
Рассчитаем фактическую массу через молярную массу:
Ответ: абсолютная масса порции оксида серы 36,8 грамм.
Задача 4
Как рассчитать молярную массу простого вещества, о котором известно, что в порции 100 г содержится 15,05 · 10 23 молекул? Назовите это вещество.
N(x) = 15,05 · 10 23 .
В данном случае поможет вычислить молярную массу NA, с помощью которого мы сначала узнаем количество вещества:
Исходя из этого, рассчитаем молярную массу:
Ответ: согласно таблице Менделеева можно предположить, что это кальций Ca.
Задача 5
Определите, насколько сероводород H2S плотнее водорода H2?
Нам требуется вычислить относительную плотность сероводорода по водороду:
Урок 5. Моль и молярная масса
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.

Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·10 23 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·10 23 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12 C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·10 23 ).

Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·10 23 атомов . Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·10 23 молекул . Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
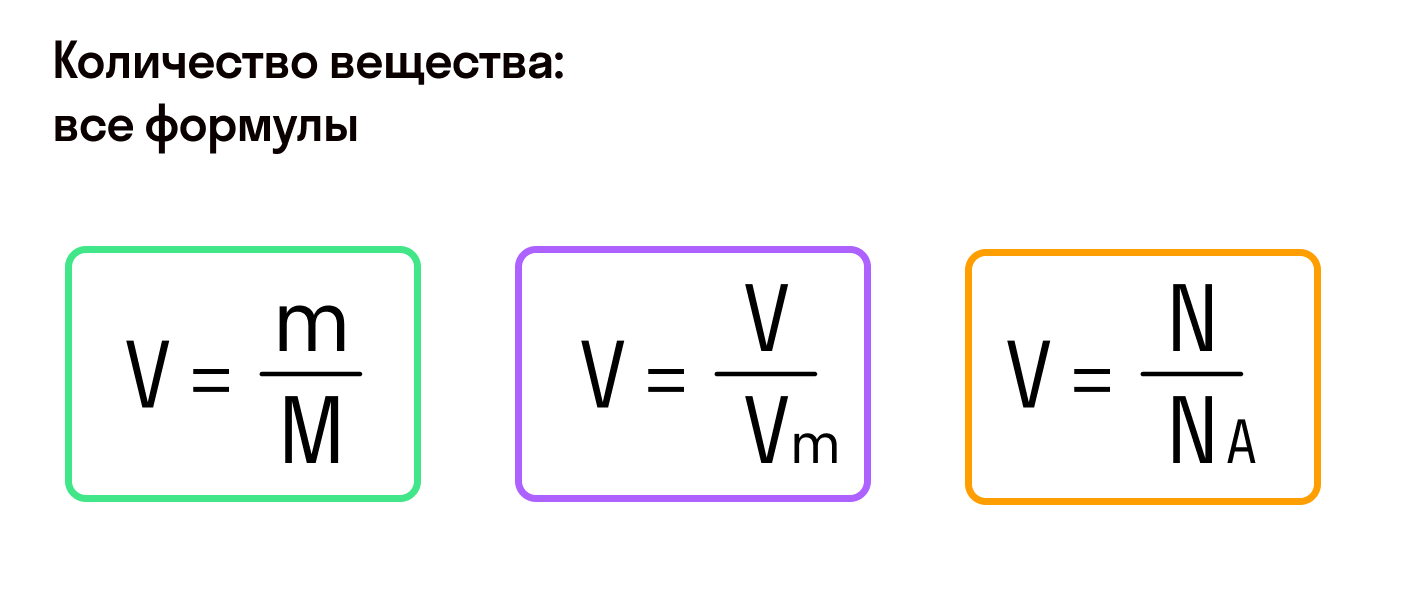
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
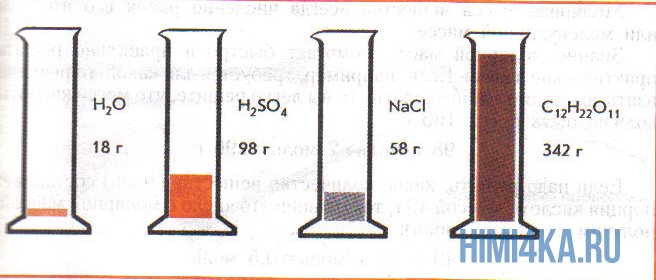
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
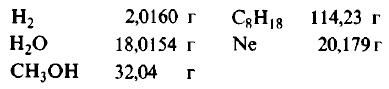
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·10 23 ; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·10 23 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·10 23 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·10 23 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·10 23 × 0,25 = 1,505·10 23 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
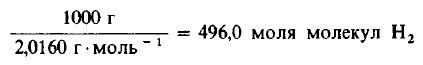
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·10 23 молекул/моль, что равно 2,99·10 26 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 9. Молярная масса и молярный объем
В уроке 9 «Молярная масса и молярный объем» из курса «Химия для чайников» выясним, что подразумевается под молярной массой и молярным объемом; приведем формулы для их вычисления. Напоминаю, что в прошлом уроке «Химическое количество вещества и моль» мы выяснили, что такое химическое количество вещества; рассмотрели моль в качестве единицы количества вещества, а также познакомились с постоянной Авогадро.

Вы знаете, что одинаковое химическое количество любых веществ содержит одно и то же число структурных единиц. Но у каждого вещества его структурная единица имеет собственную массу. Поэтому и массы одинаковых химических количеств различных веществ тоже будут различны.
Молярная масса — это масса порции вещества химическим количеством 1 моль.
Молярная масса вещества Х обозначается символом M(Х) . Она равна отношению массы данной порции вещества m(Х) (в г или кг) к его химическому количеству n(Х) (в моль):
В Международной системе единиц молярная масса выражается в кг/моль. В химии чаще используется дольная единица — г/моль.
Определим молярную массу углерода. Масса углерода химическим количеством 1 моль равна 0,012 кг, или 12 г. Отсюда:
Молярная масса любого вещества, если она выражена в г/моль, численно равна его относительной молекулярной (формульной) массе.
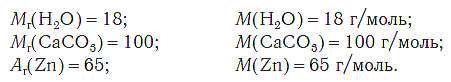
На рисунке 47 показаны образцы веществ (H2O, CaCO3, Zn), химическое количество которых одно и то же — 1 моль. Как видите, массы разных веществ химическим количеством 1 моль различны.

Молярная масса является важной характеристикой каждого отдельного вещества. Она отражает зависимость между массой и химическим количеством вещества. Зная одну из этих величин, можно определить вторую — массу по химическому количеству:
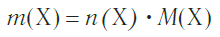
и, наоборот, химическое количество по массе:
а также число структурных единиц:
Взаимосвязь между этими тремя характеристиками вещества в любом его агрегатном состоянии можно выразить простой схемой:
В отличие от твердых и жидких веществ все газообразные вещества химическим количеством 1 моль занимают одинаковый объем (при одинаковых условиях). Эта величина называется молярным объемом и обозначается Vm .
Подобно молярной массе, молярный объем газа равен отношению объема данного газообразного вещества V(Х) к его химическому количеству n(Х) :
Так как объем газа зависит от температуры и давления, то при проведении различных расчетов берутся обычно объемы газов при нормальных условиях (сокращенно — н. у.). За нормальные условия принимаются температура 0 °С и давление 101,325 кПа.
Установлено, что при нормальных условиях отношение объема любой порции газа к химическому количеству газа есть величина постоянная и равная 22,4 дм 3 /моль. Другими словами, молярный объем любого газа при нормальных условиях:
Молярный объем — это объем, равный 22,4 дм 3 , который занимает 1 моль любого газа при нормальных условиях.
Пример 1. Вычислите химическое количество SiO2, масса которого равна 240 г.

Пример 2. Определите массу серной кислоты H2SO4, химическое количество которой 2,5 моль.

Пример 3. Сколько молекул CO2 и сколько атомов кислорода содержится в углекислом газе массой 110 г?

Пример 4. Какой объем занимает кислород химическим количеством 5 моль при нормальных условиях?

Краткие выводы урока:
- Масса вещества химическим количеством 1 моль называется его молярной массой. Она равна отношению массы данной порции вещества к его химическому количеству.
- Объем газообразных веществ химическим количеством 1 моль при нормальных условиях одинаков и равен 22,4 дм 3 .
- Величина, равная 22,4 дм 3 /моль, называется молярным объемом газов.
Надеюсь урок 9 «Молярная масса и молярный объем» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии. Данный урок был заключительным в главе «Основные химические понятия».
Определение молярной массы эквивалента металла
Теоретические основы. Согласно закону эквивалентов, вещества реагируют друг с другом в количествах, пропорциональных их эквивалентам.
Фактор эквивалентности (химический эквивалент), fЭ - это количество вещества (моль), которое реагирует с 1 молем атомов водорода или замещает это количество в химических соединениях.
Молярная масса эквивалента, МЭ - это масса одного эквивалента вещества (г/моль).
МЭ = fЭ М (М - молярная масса вещества)
Вычисление молярных масс эквивалентов проводятся с использованием следующих формул:
а) для простых веществ и элементов в соединениях
МЭ = М / В (В - валентность элемента)
б) для кислот или оснований МЭ = М / n(n - основность кислоты или кислотность основания, т.е. число ионов Н + или ОН - )
в) для оксидов и солей МЭ = М / p q( p - число атомов металла; q - валентность металла)
Число эквивалентов веществаn = m / MЭ.
Для веществ, находящихся в газообразном состоянии
n = V 0 / VЭ 0 (V 0 - объем газа при н.у.)
VЭ 0 - молярный объем эквивалента газа - объем, занимаемый одним эквивалентом газа при нормальных условиях.
Способы записи закона эквивалентов:
Цель работы. Экспериментально определить объем водорода, выделившегося в процессе реакции магния с соляной кислотой. Зная эквивалентный объем водорода, вычислить молярную массу эквивалента магния, используя закон эквивалентов.
Порядок работы.
1. Опыты по определению объемов газов, выделяющихся в процессе реакции, проводятся в специальных приборах, называемых эвдиометрами. Стандартный эвдиометр состоит из двух соединенных резиновым шлангом трубок, одна из которых градуирована (бюретка) и соединена посредством резиновой пробки и шланга с пробиркой. Неградуированная трубка называется уравнительным сосудом. Выделяющийся водород из склянки Оствальда (или пробирки) поступает в верхнюю часть градуированного сосуда и вытесняет из него воду. Разность уровней воды в градуированном сосуде до и после реакции равна объему выделившегося водорода. Открытый неградуированный сосуд называется уравнительным.
2. Проверьте герметичность прибора: присоединив пробирку к эвдиометру, опустите уравнительный сосуд на 20-25 см ниже его первоначального положения; если прибор герметичен, уровень воды в градуированном сосуде, несколько понизившись в начальный момент, в дальнейшем остается постоянным.
3. Отсоединив пробирку, установите уравнительный сосуд так, чтобы уровень воды в градуированном сосуде совпал с верхней меткой шкалы - V1 (уровень отсчитывается по нижнему мениску жидкости).
4. Взвесьте на технохимических весах 0.12-0.15 г магниевой стружки (m) и заверните металл в бумагу, на которой проводилось взвешивание, таким образом, чтобы получившийся сверток мог свободно перемещаться в пробирке и был открыт с одного конца для обеспечения доступа кислоты к магнию.
5. Отмерьте мерным цилиндром 10 мл соляной кислоты и залейте ее в пробирку.
6. Держа пробирку наклонно, поместите в верхнюю часть ее сверток с магнием и присоедините к эвдиометру.
7. Стряхните сверток с магнием в кислоту. В процессе химической реакции следите за тем, чтобы весь магний прореагировал с соляной кислотой.
8. После окончания реакции охладите пробирку до комнатной температуры.
9. Опустите уравнительный сосуд до приведения воды в нем к одному уровню с водой в градуированном сосуде. Снимите показание уровня воды - V2.
10. Запишите температуру ( t ) и давление ( Р ) в лаборатории. По таблице зависимости давления пара от температуры (приложение 1) определите давление насыщенного водяного пара ( h ).
11. Проведите расчет молярной массы эквивалента магния. Имейте в виду, что измеренный при давлении Р и температуре t объем выделившегося водорода (V2 - V1 ) не может быть непосредственно применен к расчетам молярной массы эквивалента металла. Необходимые расчетные формулы приводятся в форме лабораторного отчета.
12. Рассчитайте по формуле теоретическое значение молярной массы эквивалента магния.
13. Рассчитайте абсолютную ( А ) и относительную ( К ) ошибки опыта.
14. Сделайте выводы о точности Ваших измерений и возможных причинах ошибки.
15. Составьте лабораторный отчет по прилагаемой форме.
Форма лабораторного отчета.
1. Название лабораторной работы.
2. Краткое описание, цель работы.
3. Уравнение реакции.
4. Экспериментальные данные:
а) масса металла m = .
б) уровень воды в бюретке до реакции V1 = .
в) уровень воды в бюретке после реакции V2= .
г) объем выделившегося водорода V = V1 - V2 = .
Читайте также:
