Металлы в природе и технике
В самородном виде
и в виде соединений находятся в
природе серебро, медь,
ртуть и олово.
Металлы, которые находятся в
ряду напряжений до олова,
встречаются в природе только
в виде соединений - минералов
Металлы низкой активности
Активные металлы
Менее активные металлы
?
?
?
Золото в природе чрезвычайно рассеяно.
По распространенности в земной коре оно занимает 74 место. Но оно содержится везде: в земле, воде, в организмах растений и животных. И всё это составляет около 100 млрд. тонн.
Крупнейшие в мире золотые самородки были найдены в Австралии, они весили 86 и 112 кг.
Я солнцу подобно, и ярче огня,
Монеты и слитки куют из меня
Платина относится к наименее распространенным в природе элементам. Земная кора содержит 5×10−7% платины. В самородном состоянии встречается в основном в виде сплавов с другими металлами, например, золотом и железом.
Самым крупным существующим в настоящий момент платиновым самородком является «Уральский гигант» весом 7 кг 860,5 г.
Был обнаружен в 1904 г.
На букву «П» моё названье,
Я с золотом дружу,
И в корону для красавиц
Вместе с золотом вхожу.
По распространенности в земной коре занимает 67 место, но запасы его в 20 раз больше, чем золота. Самый крупный самородок серебра весил 13,5 тонн.
Известно я давным-давно.
Чтоб не испортилась вода,
Меня в походы брали.
И мной героев награждали.
Иду на мелкую монету,
В колоколах люблю звенеть,
Мне ставят памятник за это
И знают: имя мое -
По распространенности в земной коре занимает 26 место.
Самый большой самородок меди весил 420 тонн. Был найден в 1857 г. в США.
Выступающие части этого самородка были отбиты каменными топорами
По распространенности занимает 66 место.
В самородном виде встречается редко, причем чаще её находят в виде сплавов (амальгам) с золотом, серебром и палладием.
Когда случайно я прольюсь
– блестящим шариком качусь
Руды – содержащие минералы природные образования, в которых металлы находятся в количествах, пригодных в технологическом и экономическом отношении для получения металлов в промышленности. В основном металлы получают из оксидных и сульфидных руд.
Сульфидные руды
Медный колчедан - CuFeS2
Цинковая обманка - ZnS
Свинцовый блеск (галенит) - PbS
Сульфид ртути (киноварь) - HgS
Бурый железняк (лимонит) – 2Fe2O3·3H2O
Среди металлов самый славный,
важнейший в мире элемент.
Железо
Магнитный железняк
(магнетит) –Fe3O4
Красный железняк
(гематит) – Fe2O3
Подумайте:
1. Чем различаются руды железа?
2. Какую руду лучше использовать для получения железа?
Исследование свойств руд железа
?
Подумайте:
Какой основной химический процесс лежит в основе получения металлов?
Процесс восстановления
Mn+ + nē = M0
Связаны с промышленным получением металлов из природного сырья
?
Основателем науки о металлах в России считается великий русский ученый М. В. Ломоносов.
Ему принадлежит первый в России учебник по горному делу и металлургии.
Несколько поколений русских инженеров воспитывалось на этом замечательном труде. Среди них П. П. Аносов.
1711 - 1765
Михаил Васильевич Ломоносов
Разработал способ получения булатной стали.
Он впервые использовал микроскоп для исследования внутреннего строения металлов.
Труды Аносова были продолжены Д. К. Черновым
1799 - 1851
Павел Петрович Аносов
Является основоположником
современного металловедения и металлографии – науки о строении металлов и сплавов.
Его научные открытия легли в основу производства высококачественных чугуна и стали.
1839 -1921
Дмитрий Константинович Чернов
Открыл процесс вытеснения металлов из растворов солей под действием других металлов и металлотермический метод.
Показал, что алюминий при высокой температуре восстанавливает оксиды до металлов.
1827 - 1911
Николай Николаевич Бекетов
«Металлург»,
Л. Татьяничева
Я в космос не летал.
Но эта сталь
— Моя.
А это значит,
Помогал и я
Достичь тебе
Загадочной звезды,
Которую держал
В своих ладонях ты.
Я в космос не летал.
В грохочущей ночи
С любовью я ковал
Путей твоих лучи.
Я отдых отвергал
И годы напролет
Сто тысяч сил впрягал
В твой чудо-звездолет.
Сильна моя ладонь.
Сильнее, чем металл,
Чем стужа и огонь.
А в космос — не летал!
«Россия, богатая железными рудами различного свойства, не бедна и искусными руками», - писал Аносов П.П. Этими искусными руками являются руки металлургов.
Профессию металлурга по значимости можно сравнить с профессией хлебороба. Хлебороб создает пищу для людей, а металлург – то, без чего не невозможно представить машины, дома технику.
Поэтому людям этой профессии поэты посвящают стихи:
Указом Президиума Верховного Совета СССР в 1957 году был утвержден День металлурга , с тех пор третье воскресенье июля стало праздничным днем для всех работников отрасли.
Россия занимает первое место по производству и экспорту никеля
Второе место по производству алюминия и титана
Третье место по экспорту металлопродукции
Четвертое место по производству стали
методы переработки руд, основанные на химических реакциях, происходящих при высоких температурах (греч. пирос – огонь).
Стадии получения и уравнения реакций:
медь, цинк, хром и др.
Получаемые металлы:
Алюминотермия –
восстановление металлов из оксидов с помощью алюминия
Способы получения металлов
1. Обжиг руды
2. Плавка - восстановление металлов из оксидов с помощью
угля, водорода, оксида углерода (II), более активных
металлов
ZnO + C = Zn + CO ↑
2ZnS + 3O2 = 2ZnO + 2SO2 ↑
Природное соединение растворяют в подходящем реагенте с целью получения раствора соли этого металла CuO + 2HCl = CuCl2 + H2O
Гидрометаллургия
методы получения металлов, основанные на химических реакциях, происходящих в растворах.
Стадии получения и уравнения реакций:
Получаемые металлы:
серебро, цинк молибден, золото, уран, медь и др.
Способы получения металлов
Из полученного раствора данный металл вытесняют более активным или восстанавливают электролизом
CuCl2 (раствор) + Fe = FeCl2 + Cu
методы получения металлов, основанные на электролизе, т.е. выделение металлов из растворов или расплавов их соединений с помощью электрического тока.
Электрометаллургия –
CuCl2
расплав
Уравнение реакции электролиза:
электролиз
Cu + Cl2
Получаемые металлы:
щелочные, щелочноземельные и алюминий
Негативное воздействие на окружающую среду:
1.Загрязнение почвы по причине массового складирования отходов.
Для выработки 1 т стали необходимо 3 т сырья. Поэтому образующиеся после выплавки стали шлаки также складируют в отвалы, что крайне пагубно влияет на почву.
Например, в уральском регионе скопилось 6 млрд. тонн отходов.
Предприятия черной металлургии выбрасывают в атмосферу 25% металлосодержащей пыли и оксида углерода (II) от общего количества этих веществ, попадающих в атмосферу.
На металлургию приходится 50 % выброса сернистого газа.
Также выбрасываются токсичные для человека вещества: бензопирен, фториды, соединения марганца, вольфрама, хрома и других металлов.
Металлургия использует 25% от всей потребляемой российской промышленностью воды. Например, для получения 1 т. алюминия используется 1150 т. воды, 1 т. никеля – 4000 т. В водоемы возвращается 60-70 % чистой воды и 30-40 % загрязненной различными примесями и вредными соединениями
Переработка и
использование отходов
Строительство очистных
сооружений и
замкнутых систем
водоснабжения
Разработка
новых технологий
Будущее за новыми чистыми технологиями
Существуют проекты добычи руды не нарушая ландшафт, с помощью биотехнологий. Используют рудные растворы с тионовыми и железо-бактериями, способными переводить нерастворимые сульфиды в растворимые сульфаты, которые подаются на гидрометаллургическую переработку.
Преимущества метода:
Используется на месте залегания руд.
Не загрязняется окружающая среда.
ТЕСТ на тему: «Металлы в природе. Общие способы их получения.»
1
2
3
4
5
Вариант 1
Современные очистные сооружения на предприятиях достаточно эффективны, но имеют высокую стоимость. Будучи директором крупного завода и имея в своем распоряжении значительную сумму денег, как вы поступите:
а)положите в банк для уплаты штрафов за загрязнение природной среды;
б) вложите в строительство очистных сооружений;
в)часть вложите в расширение производства, часть – для повышение зарплаты рабочих.
Из природных веществ можно назвать рудой:
а) мел; б) гранит; в) бурый железняк; г) песок
Кому принадлежал первый в России учебник по горному делу и металлургии:
а) Н.К. Чернову; ) П.П. Аносову; в) Н.Н. Бекетову; г) М.В. Ломоносову
Гидрометаллургия представляет собой получение металлов:
а) обжигом сульфидов;
б) переводом их соединений в раствор с последующим восстановлением;
в) обработку руды водяным паром
С помощью электролиза впервые был получен металл:
а) медь; б) железо; в) свинец; г) натрий
ТЕСТ на тему: «Металлы в природе. Общие способы их получения.»
Вариант 2
Вы работаете на металлургическом заводе и случайно узнаете о неисправности в системе очистных сооружений. Как вы поступите:
а) сообщите директору завода, чтобы он принял решение;
б) сделаете вид, что вам ничего неизвестно о неисправности;
в) скажете директору и, если он не примет меры, будете активно действовать сами
К рудам не относится:
а) мрамор; б) магнитит; в) галенит; г) лимонит.
Среди минералов не встречаются:
а) оксиды металлов; б) сульфиды металлов; в) гидриды металлов; г) силикаты металлов
Металлический марганец получают алюминотермией из оксида марганца (IV)/ Составьте уравнение реакции. Сумма коэффициентов в правой части уравнения равна:
а) 4; б) 5; в) 6; г) 7.
В настоящее время для получения хрома в качестве восстановителя чаще всего используется:
а) медь; б) натрий; в) хлор; г) алюминий
Проверь себя
Из записанных уравнений выберите те, которые относятся к пирометаллургическому способу:
2ZnS + 3O2 = 2 ZnO + 2SO2
ZnSO4 +Mg = MgSO4 + Zn
ZnO + CO = Zn + CO2
ZnO + H2SO4 = ZnSO4 + H2
ZnSO4 +Mg = MgSO4 + Zn
ZnO + H2SO4 = ZnSO4 + H2
ZnSO4 +Mg = MgSO4 + Zn
ZnO + H2SO4 = ZnSO4 + H2
2ZnS + 3O2 = 2 ZnO + 2SO2
ZnO + CO = Zn + CO2
2ZnS + 3O2 = 2 ZnO + 2SO2
ZnO + CO = Zn + CO2
2ZnS + 3O2 = 2 ZnO + 2SO2
ZnO + CO = Zn + CO2
2ZnS + 3O2 = 2 ZnO + 2SO2
ZnO + CO = Zn + CO2
Металлы в природе ПЛАН : Металлы в технике Способы получения металлов Характеристика чёрной и цветной металлургии Металлы в организме Металлы в истории. - презентация
Презентация на тему: " Металлы в природе ПЛАН : Металлы в технике Способы получения металлов Характеристика чёрной и цветной металлургии Металлы в организме Металлы в истории." — Транскрипт:
2 Металлы в природе ПЛАН : Металлы в технике Способы получения металлов Характеристика чёрной и цветной металлургии Металлы в организме Металлы в истории Коррозия металлов
4 Металлы в природе встречаются в 3-х формах: 1. В свободном виде 2. Как в свободном, так и в виде соединений 3. Только в виде соединений МЕТАЛЛЫ В ПРИРОДЕ Только в соединениях Как в свободном так и в виде соединений Главным образом в виде соединений Только в свободном виде Li K Ca Na Mg Al Mn Zn Cr Ni Sn PbCu Ag Hg Au Pt Самый распространённый металл на Земле – алюминий (более 8% от земной коры).
5 Тяжёлые Медь,цинк, свинец,олово, никель Лёгкие Алюминий,титан,магний Благородные Золото,платина,серебро Редкоземельные Цирконий,селен,германий железо, сталь, чугун
7 СПОСОБЫ ПОЛУЧЕНИЯ МЕТАЛЛОВ 1. Пирометаллургия - восстановление металлов из руд при высоких температурах с помощью восстановителей (углерода, оксида углерода(П), водорода, магния, алюминия). 2. Гидрометаллургия – растворение природного соединения металла с последующим восстановлением его из раствора. 3. Электрометаллургия - способ получения металла с помощью электрического тока (электролиз).
8 Металлургические базы Казахстана Медь Подтвержденные запасы меди Казахстана оцениваются в 37 млн т (или 5,5% от мировых запасов). По этому показателю Республика занимает 4-е место в мире после Чили, Индонезии и США. На территории Республики Казахстан разведано более 90 месторождений меди. К числу крупнейших отно сится Джезказганское месторождение медистых песчаников, месторождения медно- порфирового типа Актогайское и Айдарлы. Цинк Подтвержденные запасы цинка Казахстана оцениваются в 25,7 млн т (9,5 % мировых запасов), по этому показателю Республика находится на 4-м месте в мире после Австралии, США и России. Запасы цинка сосредоточены более в чем 50-ти месторождениях, при этом преобладающим типом являются полиметаллические руды. По данным «Инфомайн», добыча цинксодержащих руд осуществляется на 16 месторождениях. Свинец Подтвержденные запасы свинца Казахстана оцениваются в 11,7 млн т (или 10,1% мировых запасов), по этому показателю Республика находится на 6-м месте после России, Австралии, Канады, США и Китая. Запасы свинца Казахстана сосредоточены в более 50 месторождениях. По данным «Инфомайн», добыча свинец содержащих руд осуществляется на 15 месторождениях. Алюминий В Казахстане разведано свыше 20 месторождения бокситов, основная часть запасов Республики (около 90%) сосредоточена в месторождениях, находящихся на территории Костанайской области (Западно-Тургайский и Центрально- Тургайский бокситовые районы). При этом разрабатывается 10 месторождений бокситов. Торгайский бокситовый рудник (ТБРУ) разрабатывает бокситы Восточно- Тургайской группы (Аркалыкское, Северное, Нижнее- Ашутское, Верхнее- Ашутское, Уштобинское месторождения). Золото Разведанные запасы золота Казахстана оцениваются на уровне 1700 т (4% от мировых запасов) по этому показателю Республика занимает 7 место в мире после ЮАР, США, Австралии, России, Канады, Узбекистана и Индонезии. В настоящее время в Казахстане разведано 199 промышленных месторождений золота, практически во всех регионах страны, в том числе 127 коренных месторождений, 40 комплексных, 32 рассыпных. Серебро Запасы серебра Казахстана разведаны более чем в 100 месторождениях, при этом основная доля (около 60%) приходится на полиметаллические (медно-свинцово- цинковые) месторождения. Уровень содержания серебра в рудах этих месторождений находится на уровне от 40 до 100 г/т. Около 25% запасов серебра Республики сосредоточено в месторождениях медистых песчаников (Жезказганское и др.), где содержание серебра составляет г/т. Доля собственно золото- серебряных руд в общем объеме запасов и добычи серебра незначительна.
9 Добыча руды Обогащение руды Выплавка чернового металла Выплавка рафинированного металла Производство проката
10 Химические элементы Макроэлементы О, С, N, H, Mg, K, Na, Ca, Fe, S, P Микроэлементы B, Co, Cu, Mo, Zn, V, I, Br Ультрамикро- элементы менее U, Ra, Au, Hg, Be, Cs, Se
11 Mg Zn K Ca Cd Sr 90 Pb Be Cs 137 Cd Sr 90 Pb Be Cs 137
14 свинец железо медь олово золото ртуть
15 Избыток железа превращает человека в агрессивное существо с жестоким, эгоистичным характером. Такие люди очень активны, постоянно чем-то заняты. Любят командовать, поэтому чаще всего становятся военными, спортивными инструкторами или бизнесменами. Но таких «железных дровосеков» можно смягчить, если давать им меньше мяса.
16 Люди, в организме которых больше всего меди, мягки и покладисты. Они любят красивую жизнь и вкусную еду, предпочтение отдают сладостям. Они всегда готовы прийти на помощь, у них дружные семьи и много друзей. Чаще всего они становятся писателями, музыкантами или художниками. Однако их часто обманывают и предают, пользуясь их слабостями. Поэтому, если в этом описании вы узнали себя, постарайтесь потреблять больше продуктов, содержащих железо, – так вы компенсируете мягкость меди.
17 Чрезмерное содержание в организме свинца делает человека вялым и апатичным. Он всегда не в настроении, вечно находит повод для недовольства. Чаще всего такие люди оказываются в положении жертвы. Из них получаются отменные подчиненные, ведь они не инициаторы, а предпочитают, скорее, подчиняться распоряжениям. Таким людям просто необходимо разбавлять свой свинец золотом, медью, оловом и серебром.
18 Олово – это тот металл, который в избытке содержится в организме мыслителей, философов и путешественников. У них – отменное чувство юмора, а их энтузиазм часто переходит в одержимость. Свинец сделает их более серьезными, а железо – крепкими.
19 Драгоценные металлы и в организме - драгоценность. Серебро, например, - металл чувствительных, эмоциональных людей, обладающих огромной интуицией, или ясновидящих. Золото преобладает в организме тщеславных, заносчивых людей. Но это лишь видимость: внутри они добры и щедры, просто к ним нужно отыскать подход. Они - верные друзья, готовые в любую минуту прийти на помощь. Им необходимо пополнять свой организм и другими металлами - на характере это, возможно, не отразится, а здоровье укрепит.
20 Болтливые люди, оказывается, любят поговорить от. обилия в организме ртути. Еще такие люди хитры, беспринципны и легко предают. Им явно необходимо разбавить этот жидкий металл железом.
21 Самопроизвольное разрушение металлов под влиянием окружающей среды. В реальных условиях самый распространенный вид разрушения конструкций и изделий из металлов и сплавов..
22 Коррозию металлов и сплавов вызывают такие компоненты окружающей среды: Вода Кислород Оксид углерода и серы Водные растворы солей (морская и грунтовая воды) Химический состав металла Температура Давление
23 Под угрозой разрушения находится до 50% металлоконструкций. Коррозии подвержены бетон, пластмасс, особенно изделия из железа. Не подвержены этому лишь драгоценные металлы из золота, платины.
25 Для борьбы существует много способов: Нанесение защитных покрытий (Предохраняемый ме покрывают серебром, золотом, хромом,никелем) Нержавеющая сталь (Содержит 12%хрома, 10% никеля. Легкие включают титан, алюминий) Ингибитор ( В-ва снижающие агрессивность среды)
26 Зашита стальных конструкций в автодорожной отрасли является актуальной. Это связано с несоответствием сроков эксплуатации и сроков антикоррозийной зашиты.
27 Широко использованные лакокрасочные системы имеют срок эксплуатации 4-10 лет Горячее цинкование стальных конструкций обеспечивает сроки лет
28 Основным принципом защиты черных металлов является принцип катодной защиты посредством жертвенных электронов. Принцип заключается в том, что один металл (цинк) расходуется для защиты другого металла (железа). Цинк подвергается коррозии гораздо медленнее, чем железо.
29 Современный автомобиль - комфортабельный, быстроходный, удобный в эксплуатации, но очень уязвимый. Создается впечатление, что против него ополчилось все: солнце, вода, соль, песок, атмосферные загрязнения.
30 Автомобильные заводы ведут большие работы по увеличению срока службы автомобилей. В результате этих усилий двигатель и остальные агрегаты продолжительное время сохраняют свои силы и молодость, в то время как кузов - основная часть автомобиля - дряхлеет и приходит в негодность. Чтобы дойти до такого состояния, ему требуется всего каких- нибудь 6-7 лет.
31 Коррозия настолько агрессивна, что начинает поражать автомобили уже в первый год их эксплуатации, а на третьем году, по данным исследований, на кузовах отечественных легковых автомобилей возникает очагов коррозии, и самое неприятное, что приостановить начавшийся процесс очень трудно.
32 Благоприятную обстановку для развития коррозии создавали: - высокие напряжения и вибрации несущих кузовов; - появление различных замысловатых конструкций со скрытыми полостями - удобными накопителями влаги и грязи; - различные украшения, навешенные на автомобиль. Контакт этих декоративных деталей с металлом кузова становился очагом коррозии; - качество (пористость, микротрещины) самого металла, где каждая пора при доступе влаги становилась микроэлементом; - окружающая среда с большим содержанием продуктов сжигания топлива и двуокиси серы, которая, взаимодействуя с влагой, образует серную кислоту; - химические средства против обледенения дорог, среди которых хлористый кальций и натрий прекрасно впитывает влагу, создавая живительную среду развития коррозии.
И ИХ ИСПОЛЬЗОВАНИЕ В ЖИЗНИ ЧЕЛОВЕКА. I. Общая характеристика металлов. II. Разновидность металлов. III. Свойства металлов. IV. Нахождение металлов в природе. - презентация
Презентация на тему: " И ИХ ИСПОЛЬЗОВАНИЕ В ЖИЗНИ ЧЕЛОВЕКА. I. Общая характеристика металлов. II. Разновидность металлов. III. Свойства металлов. IV. Нахождение металлов в природе." — Транскрипт:
1 И ИХ ИСПОЛЬЗОВАНИЕ В ЖИЗНИ ЧЕЛОВЕКА
2 I. Общая характеристика металлов. II. Разновидность металлов. III. Свойства металлов. IV. Нахождение металлов в природе. V. Применение металлов в жизни человека.
3 Мета́лл (название происходит от лат. metallum шахта) группа элементов, обладающая характерными металлическими свойствами, такими как высокая тепло- и электропроводность, высокая пластичность и др. К металлам относятся примерно 70 % всех химических элементов.лат.тепло-электропроводностьпластичностьхимических элементов
4 Щелочные: Щёлочноземельные: Переходные: Литий Кальций Железо Натрий Стронций Платина Калий Барий Медь Рубидий Цинк Цезий Золото Серебро Палладий Ртуть Никель Кобальт Другие: Алюминий, Свинец, Олово
5 Металлический блеск. Хорошая электропроводность. Возможность лёгкой механической обработки (пластичность; однако, некоторые металлы, например германий и висмут, непластичны.)германийвисмут Высокая плотность Высокая температура плавления (искл.: ртуть, галлий и щелочные металлы.)ртуть галлийщелочные металлы Большая теплопроводность В реакциях всегда являются восстановителями
6 Многие металлы широко распространены в природе. Так, содержание некоторых металлов в земной коре следующее: алюминия 8,2% железа 4,1% кальция 4,1% натрия 2,3% магния 2,3% калия - 2,1 % титана 0,56%
7 Большое количество натрия и магния содержится в морской воде: 1,05%, 0,12%. В природе металлы встречаются в различном виде: в самородном состоянии: серебро, золото, латина, медь, иногда ртуть. в виде оксидов в виде смешанных оксидов различных солей Многие металлы часто сопутствуют основным природным минералам: скандий входит в состав оловянных, вольфрамовых руд, кадмий в качестве примеси в цинковые руды, ниобий и тантал в оловянные. Железным рудам всегда сопутствуют марганец, никель, кобальт, молибден, титан, германий, ванадий.
9 В медицине благородные металлы применяют для изготовления инструментов, деталей приборов, протезов, а также различных препаратов, главным образом на основе серебра. Сплавы платины с иридием, палладием и золотом почти незаменимы при изготовлении игл для шприцев. Из медицинских препаратов, содержащих благородных металлов, наиболее распространены ляпис, протаргол и др. Благородные металлы применяют при лучевой терапии (иглы из радиоактивного золота для разрушения злокачественных опухолей), а также в препаратах, повышающих защитные свойства организма.
10 Металлы составляют одну из основ цивилизации на планете Земля. Среди них как конструкционный материал явно выделяется железо. Объем промышленного производства железа примерно в 20 раз больше, чем объем производства всех остальных металлов, вместе взятых. Широкое внедрение железа в промышленное строительство и транспорт произошло на рубеже XVIII. XIX вв. В это время появился первый чугунный мост, спущено на воду первое судно, корпус которого был изготовлен из стали, созданы первые железные дороги. Однако начало практического использования человеком железа относят к IX в. до н.э. Именно в этот период человечество из бронзового века перешло в век железный В природе, хотя и очень редко, но встречается самородное железо. Его происхождение считают метеоритным, т.е. космическим, а не земным. Поэтому первые изделия из железа (они изготавливались из самородков) ценились очень высоко – гораздо выше, чем из серебра и даже золота.
11 Коррозия- самопроизвольный процесс разрушения материалов и изделий из них под химическим воздействием окружающей среды. Ржавлением называют только коррозию железа и его сплавов. Другие металлы коррозируют, но не ржавеют. Хотя коррозируют практически все металлы, в повседневной жизни человек чаще всего сталкивается с коррозией железа.
12 Несмотря на широкое внедрение в нашу сегодняшнюю жизнь стекла, керамики, основным материалом продолжает оставаться железо и сплавы на его основе. С изделиями из железа мы на каждом шагу встречаемся в быту и знаем, как много хлопот доставляют его ржавление и сама ржавчина.
"Металлы в природе. Общие способы получения металлов"

Презентация предназначена для учащихся 9 класса, ее можно использовать при изучение темы "Металлы", а так же при подготовке к ОГЭ. В презентации рассматривается вопрос о нахождении металлов в природе и общих способах получения металлов - прирометаллургии, гидрометаллургии, электрометаллургии и микробиологической способе.
Содержимое разработки

Металлы в природе.
Общие способы получения металлов.
Презентация к уроку. 9 класс .Химия. Антонова Ирина Павловна . Учитель химии и биологии МБОУ СОШ№8

ЦЕЛЬ УРОКА :
- Познакомиться с природными соединениями металлов и с самородными металлами; получить понятие о рудах и металлургии, рассмотреть такие ее разновидности, как пиро–, гидро–, электрометаллургия, термическое разложение соединений металлов, продемонстрировать лабораторные способы получения металлов и ознакомиться с промышленным производством металлов.
РАСПРОСТРАНЕННОСТЬ МЕТАЛЛОВ В ПРИРОДЕ
Процентное содержание металлов в морской воде:
В ПРИРОДЕ МЕТАЛЛЫ МОГУТ ВСТРЕЧАТЬСЯ
Железный метеорит




KCl • MgCl 2 • 6H 2 O


СУЛЬФАТЫ, ФОСФАТЫ, КАРБОНАТЫ

Черная- получение
железа и его
сплавов (сталь, чугун)
Цветная- получение
остальных металлов
и их сплавов

- Восстановление металлов из руд при высоких температурах с помощью восстановителей.
Соль → оксид
Соли кислородсодержащих кислот – термическое разложение:
CuCO 3 = CuO + CO 2
Соли бескислородных кислот- обжиг:
2ZnS + ЗО 2 = 2ZnО + 2SО 2

Пирометаллургия
Восстановление углем или угарным газом:
CuO + C → Cu + CO
CuO + CO → Cu + CO 2
Водородотермия:
Cr 2 O 3 + H 2 → Cr + H 2 O
Металлотермия:
Fe 2 O 3 + Al → Fe + Al 2 O 3

- Получение металлов израстворових солей.
- Перевод нерастворимого соединения в раствор:
CuO + H 2 SO 4 = CuSO 4 + H 2 O
CuSO 4 + Fe = FeSO 4 + Cu.
2NaCl → 2Na + Cl 2
MgBr 2 → Mg + Br 2
- Микробиологические методы получения металлов.

-82%
Металлы в природе. Способы получения металлов
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобретя в каталоге.
Получите невероятные возможности



Конспект урока "Металлы в природе. Способы получения металлов"
С металлами в свободном состоянии человек знаком с самой глубокой древности. Изначально человеку было известно только 7 металлов, так называемы «металлы древности».

За последние 250 лет открыто и получено в свободном виде 86 новых металлов.
Использовать металлы в свободном виде человек начал в древние века. Первыми металлами из них были золото, серебро, медь. Освоение выплавки железа в больших масштабах сделало огромный переворот в промышленности.

В природе металлы встречаются как в виде простых веществ (в свободном виде), а также в виде соединений. Малоактивные металлы: медь, золото, серебро, платина, палладий и др. в природе могут находиться как в свободном виде, так и в составе соединений. Активные металлы: натрий, калий, кальций, алюминий, магний и др. встречаются в природе только в виде соединений: оксидов, сульфидов, карбонатов и т.д.
Если металл в природных условиях находится в свободном состоянии, то для получения чистого металла нужно только избавиться от соответствующих смесей. Получение металлов из соединений – это задача металлургии.
Большинство металлов находится в природных условиях в виде соединений – руд. Руда – это природное минеральное образование, в котором атомы химических элементов находятся в окисленном состоянии. Для получения металла для этого необходимо провести процесс восстановления:
Для данного процесса используют восстановители, такие как, водород, более активные металлы, углерод (в виде кокса), оксид углерода (II), постоянный электрический ток.
Технологические процессы, лежащие в основе промышленных способов получения металлов из руд, можно разделить на пирометаллургические, гидрометаллургические, электрометаллургические.
Пирометаллургические способы получения металлов основаны на использовании различных восстановителей для получения металлов путем восстановления из руд при высокой температуре.
В гидрометаллургических методах процесс восстановления протекает в водном растворе.
В электрометаллургических процессах восстановителем является постоянный электрический ток.
Водород как восстановитель может использоваться для получения металлов со средней и малой химической активностью: например, меди, вольфрама, молибдена. В данном случае водород восстанавливает металл из его оксида при высокой температуре.
Восстановить металлы из их оксидов можно с помощью более активного металла, поэтому процесс восстановление металлами называется металлотермией. Если в роли восстановителя металла выступает алюминий, то данный процесс называется алюмотермией.

Так, алюминий используется для получения кальция из его оксида, а металлический кальций используют для получения цезия.
Ca + 2СsСl = CaCl2 + 2Cs
Углерод и оксид углерода (II) являются сильными восстановителями.
CuO + CO = Cu + CO2↑

Свободный углерод (в виде кокса) и оксид углерода (II) служат восстановителями при производстве железа в доменном процессе. В общем виде:
Постоянный электрический ток является самым сильным восстановителем. С помощью электрического тока получают многие активные металлы: натрий, калий, кальций и др. При этом процесс идёт не в водном растворе, а в расплаве при повышенной температуре.
Алюминий в промышленных масштабах получают путём электролиза раствора оксида алюминия в расплавленном криолите (Na3AlF6).
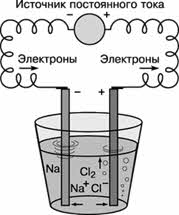
Таким образом, большинство металлов в природе находятся только в виде соединений, в самородном состоянии встречаются золото, медь, палладий и др. Получение металлов из соединений – это задача металлургии. В зависимости от способа получения металлов различают следующие методы: пирометаллургия, электрометаллургия и гидрометаллургия. В пирометаллургическом методе использую восстановители: водород, углерод, оксид углерода (II), более активные металлы.
Читайте также:
