Как сделать цепочку превращений в органической химии
Предлагаем вам сборку заданий по теме Взаимосвязь органических соединений. Ответы вы найдёте внизу страницы.
Задания 32


Задание 3

Задание 4

Задание 5

Задание 6

Задание 7

Задание 8

Задание 9

Задание 10


Задание 12

Задание 13

Задание 14

Задание 15

Задание 16

Задание 17

Задание 18
![]()
Задание 19

Задание 20

Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
Задание 21

Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
Задание 22
При написании уравнений реакций указывайте преимущественно образующиеся продукты, используйте структурные формулы органических веществ.
Ответы:

Задание 2

Задание 3

Задание 4

Задание 5

Задание 6

Задание 7
Задание 8
Задание 9
Задание 10
Задание 11

Задание 12


Задание 14
Задание 15

Задание 16
Задание 17

Задание 18![]()
Задание 19![]()
Задание 20![]()
Задание 21![]()
Задание 22![Взаимосвязь органических соединений]()
Также предлагаем вам плейлист видео-уроков и видео-объяснений заданий на эту тему:

Химические цепочки превращений - это один из наиболее часто встречающихся в школьных учебниках, а также на самостоятельных, проверочных и контрольных типов задач по химии. Чтобы успешно их решать, нужно понимать, как именно они устроены и каким образом стоит подходить к ним. Рассмотрим, как решать цепочки превращений в общем и на конкретных примерах.
Общие принципы решения химических цепочек превращений
Для начала нужно внимательно прочитать условие задачи и изучить цепочку. Четко поняв, что требуется в задаче, можно переходить непосредственно к ее решению.
- Выписав отдельно цепочку химических превращений, пронумеруйте количество необходимых реакций (они обозначены стрелочками от одного вещества к другому).
- Определите, к какому классу веществ относится каждый член цепочки и, если необходимо, выпишите на черновике отдельно в столбик каждое вещество из цепочки и его класс. В случае когда имеются неназванные вещества и их класс неизвестен, проанализируйте, какие вещества могут быть получены из исходного и какого класса вещество должно выступить исходным для следующего после неназванного вещества элемента цепочки.
- Проанализируйте, каким образом можно получить вещество этого класса из исходного для каждого элемента цепочки. В случае если прямая реакция невозможна, подумайте, какие классы веществ можно получить из исходного вещества и из каких получаемых веществ можно позже синтезировать конечное требуемое вещество.
- Составьте схему уравнения первой из необходимых реакций. Не забудьте расставить коэффициенты в уравнении.
- Последовательно осуществите цепочку химических превращений, рассматривая каждую реакцию в отдельности. Проверьте себя, уделяя внимание оформлению реакций.
Пример решения цепочки превращений
Допустим, в задаче имеется химическая цепочка превращений следующего вида:
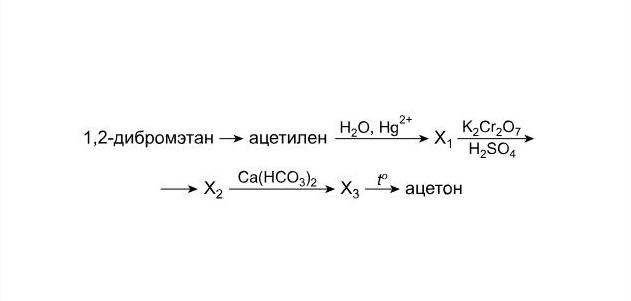
Необходимо найти вещества, обозначенные как Х1, Х2 и Х3, и осуществить указанные реакции. Рассмотрим, какие реакции необходимо выполнить для решения этой цепочки после того, как вы пронумеруете стрелки и определите классы веществ.
- Для того чтобы из 1,2-дибромэтана получить ацетилен, нужно воздействовать на него спиртовым раствором щелочи при нагревании. В ходе этой реакции от одной из молекул 1,2-дибромэтана отщепятся две молекулы бромоводорода. Эти молекулы будут нейтрализованы щелочью.
- Далее, исходя из условий протекания реакции, вы делаете вывод, что это реакция М. Г. Кучерова. Она приводит к образованию ацетальдегида.
- Ацетальдегид, реагируя в присутствии серной кислоты с дихроматом калия, дает уксусную кислоту.
- Гидрокарбонат вступает в реакцию обмена с раствором кислоты.
- Полученный ацетат щелочноземельного металла при нагревании разлагается, образуя карбонат металла и кетон.
Таким образом, записанное поэтапно решение данной химической цепочки превращений будет выглядеть так:
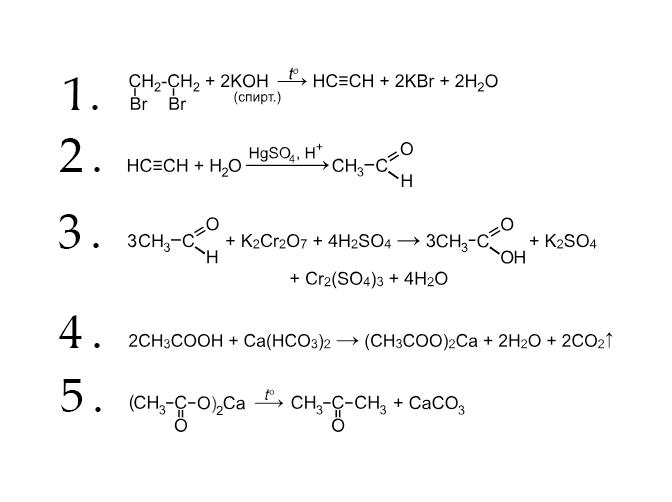
Полезные советы
Решая цепочки химических уравнений, важно помнить, что конечный результат зависит от каждой последовательно верно решенной реакции в этой цепочке. Следовательно, проверяя себя на последнем этапе, нужно перепроверить возможность каждой реакции и правильность составления и решения уравнения.
Кроме того, если вы сомневаетесь, верно ли вывели ту или иную формулу вещества, вы можете заглянуть на этапе обучения в справочник химических веществ. Важно при этом помнить, что надо не просто сверяться с ним, а запоминать формулы и стараться в дальнейшем самостоятельно воспроизводить их.

Какой вообще алгоритм действий при решении таких задач?
· Определяем класс исходного вещества.С2H5OH — классический предельный одноатомный спирт.
· Определяем условия реакции.Нам дана серная кислота и реакция происходит при нагревании. В Органической химии сочетание H2SO4/tозначаетдегидратацию.
Дегидратация — реакция отщепления воды от молекул органических соединений
Но все дело в том, что в данном случае у нас возможны 2 варианта: образование простого эфира —межмолекулярная дегидратация или образование алкена — внутримолекулярная дегидратация.
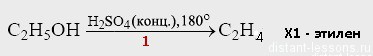
· По следующей реакции определяем исходное веществоХ1 подвергается слабому окислению. Слабому, т.к. выбраны достаточно мягкие условия — водная среда (H2O) и низкая температура). Простые эфиры не окисляются, а вот алкены очень даже хорошо вступают в реакции такого рода, следовательно, в первая реакция у нас была внутримолекулярная дегидратация:
Полученное вещество — этилен — вещество с двойной связью (алкен)
В теперь внимание. При окислении в зависимости от условий реакции алкены дают разные продукты!

Обратите внимание на эти реакции. Зазубривать их не надо, надо запомнить логику:
— при мягком окислении образуется диол -двухатомный спирт;
— при более жестком окислении рвется двойная связь и образуетсякислота;
— совсем жесткое окисление — это горение.
Спирты, как и остальные органические соединения, при горении образуют углекислый газ (СO2) и воду (H2O).
В нашем случае окисление прошло в мягких условиях, поэтому образовалсяэтандиол или этиленгликоль — двухатомный спирт.
Х2 — 1,2-этандиол, или этиленгликоль
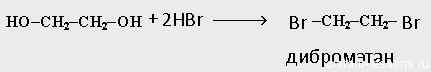
· Взаимодействие с избытком HBr.Взаимодействие спиртов с галогеноводородами дает галогеналканы. Но здесь не просто взаимодействие, а взаимодействие с ИЗБЫТКОМ. Это означает, что обе группы -ОН будут заменены на Br: Х3 — 1,2-дибромэтан.
· В следующей реакции продуктом является этин или ацетилен. Алкины содержат меньше атомов водорода, поэтому такая реакция будет называтьсядегидрирование.
Дегидрирование —реакция отщепления водорода
У нас еще уходит Br, поэтому такая реакция — это дегидрогалогенирование.

Алкины — вещества с тройной связью.Условия реакции— KOH в спиртовом растворе (Y).Именно в спиртовом, т.к. в водном растворе будет происходить совершенно другая реакция — присутствие -OH-групп здесь крайне нежелательно!
Ну и чтобы написать последнюю реакцию, нам надо определить вещество C2H4O.Оно отличается от этина ровно на молекулу H2O. Это непредельный спирт. ПоэтомуZ=H2O

В первой цепочке начало — классический способ получения метана:
4Al + 3C -> Al4C3 карбид алюминия
Al4C3 + 12H2O -> 4Al(OH)4 + 3CH4 Х1 = метан
Хлорирование метана ( 1 моль) на свету — т.е. образуется монохлорпроизводное:
CH4 + Cl2 -> CH3Cl + HCl X2 = хлорметан
Чтобы получить этан, нужно провести реакцию Вюрца:
2CH3Cl + 2Na -> C2H6 + 2NaCl
При нагревании и действии катализатора обычно происходит дегидрирование — из алканов образуются алкены:

(\"\u0433\u0435\u043d\u0435\u0437\u0438\u0437\" \u043f\u043e-\u0433\u0440\u0435\u0447\u0435\u0441\u043a\u0438 \u043e\u0431\u043e\u0437\u043d\u0430\u0447\u0430\u0435\u0442 \"\u043f\u0440\u043e\u0438\u0441\u0445\u043e\u0436\u0434\u0435\u043d\u0438\u0435\"). \u042d\u0442\u0430 \u0441\u0432\u044f\u0437\u044c \u0437\u0430\u043a\u043b\u044e\u0447\u0430\u0435\u0442\u0441\u044f \u0432 \u0442\u043e\u043c, \u0447\u0442\u043e \u0438\u0437 \u0432\u0435\u0449\u0435\u0441\u0442\u0432 \u043e\u0434\u043d\u043e\u0433\u043e \u043a\u043b\u0430\u0441\u0441\u0430 \u043c\u043e\u0436\u043d\u043e \u043f\u043e\u043b\u0443\u0447\u0438\u0442\u044c \u0432\u0435\u0449\u0435\u0441\u0442\u0432\u0430 \u0434\u0440\u0443\u0433\u0438\u0445 \u043a\u043b\u0430\u0441\u0441\u043e\u0432. \u0427\u0442\u043e \u0431\u044b\u00a0 \u0443\u043c\u0435\u0442\u044c \u043e\u0441\u0443\u0449\u0435\u0441\u0442\u0432\u043b\u044f\u0442\u044c \u0446\u0435\u043f\u043e\u0447\u043a\u0443 \u043f\u0440\u0435\u0432\u0440\u0430\u0449\u0435\u043d\u0438\u0439, \u043d\u0435\u043e\u0431\u0445\u043e\u0434\u0438\u043c\u043e \u0437\u043d\u0430\u0442\u044c \u0441\u0432\u043e\u0439\u0441\u0442\u0432\u0430 \u0432\u0435\u0449\u0435\u0441\u0442\u0432.
\u00a0\u041d\u0430\u043f\u0440\u0438\u043c\u0435\u0440,
1. \u043f\u0440\u043e\u0441\u0442\u043e\u0435 \u0432\u0435\u0449\u0435\u0441\u0442\u0432\u043e- \u043e\u043a\u0441\u0438\u0434- \u043e\u0441\u043d\u043e\u0432\u0430\u043d\u0438\u0435- \u0441\u043e\u043b\u044c
\u00a0\u00a0 \u00a0 \u00a0 \u00a0 Ca \u2192CaO \u2192 Ca(OH)\u2082 \u2192CaCO\u2083
2Ca+ O\u2082 = 2CaO \u043e\u043a\u0441\u0438\u0434 \u043a\u0430\u043b\u044c\u0446\u0438\u044f
CaO + H\u2082O = Ca(OH)\u2082 \u043e\u0441\u043d\u043e\u0432\u0430\u043d\u0438\u0435 - \u0433\u0438\u0440\u043e\u043a\u0441\u0438\u0434 \u043a\u0430\u043b\u044c\u0446\u0438\u044f
Ca(OH)\u2082 + CO\u2082 = CaCO\u2083 + H\u2082O \u0441\u043e\u043b\u044c - \u043a\u0430\u0440\u0431\u043e\u043d\u0430\u0442 \u043a\u0430\u043b\u044c\u0446\u0438\u044f
2. \u043f\u043e\u0441\u0442\u043e\u0435 \u2192\u0432\u0435\u0449\u0435\u0441\u0442\u0432\u043e \u2192 \u043e\u043a\u0441\u0438\u0434\u2192 \u043e\u043a\u0441\u0438\u0434 \u2192 \u00a0 \u043a\u0438\u0441\u043b\u043e\u0442\u0430 \u2192\u0441\u043e\u043b\u044c
\u0421\u0435\u0440\u0430 \u2192 \u043e\u043a\u0441\u0438\u0434 \u0441\u0435\u0440\u044b(IV) \u2192\u00a0 \u043e\u043a\u0441\u0438\u0434 \u0441\u0435\u0440\u044b(VI) \u2192 \u0441\u0435\u0440\u043d\u0430\u044f \u043a\u0438\u0441\u043b\u043e\u0442\u0430\u2192 \u0441\u0443\u043b\u044c\u0444\u0430\u0442 \u0431\u0430\u0440\u0438\u044f
S + O\u2082=SO\u2082 \u043e\u043a\u0441\u0438\u0434 \u0441\u0435\u0440\u044b(IV)
SO\u2082 + O\u2082 =SO\u2083 \u043e\u043a\u0441\u0438\u0434 \u0441\u0435\u0440\u044b(VI)
SO\u2083 + H\u2082O = H\u2082SO\u2084 \u0441\u0435\u0440\u043d\u0430\u044f \u043a\u0438\u0441\u043b\u043e\u0442\u0430
H\u2082SO\u2084 + BaCI\u2082 = BaSO\u2084 + HCI \u0441\u0443\u043b\u044c\u0444\u0430\u0442 \u0431\u0430\u0440\u0438\u044f + \u0441\u043e\u043b\u044f\u043d\u0430\u044f \u043a\u0438\u0441\u043b\u043e\u0442\u0430
\u00a0\u00a0 \u00a0 \u00a0 \u00a0\u00a0
Читайте также:








