Как печатают органы на 3д принтере
Пред тем, как начать читать статью, вы можете посмотреть мое видео на тему 3D печати органа.
Ежегодно в мире умирает тысячи людей, которые не смогли дождаться очереди на получение донорских органов. Даже в США в настоящее время своей очереди ожидают более 150 000 человек, и это число постоянно увеличивается.
Но даже успешная пересадка не дает стопроцентной гарантии на принятие нового органа. Все дело в иммунитете, чтобы собственная иммунная система не отторгла новообретенные органы, пациентам приходится принимать препараты, действие которых может не дать необходимый для жизнедеятельности результат. Решить эту проблему пытается биопринтинг - технология создания объёмных моделей на клеточной основе с использованием 3D-печати, при которой сохраняются функции и жизнеспособность клеток.
Зарождения биопринтинга началось в 2000-м году, когда биоинженер Томас Боланд перенастроил настольные принтеры для печати фрагментов ДНК. Оказалось, что размер человеческих клеток сопоставим с размерами капли стандартных чернил и составляет примерно 10 микрон. Исследования показали, что 90% клеток сохраняют жизнеспособность в процессе биопечати.
В 2003 году Томас Боланд запатентовал технологию печати клетками. С этого момента печать органов на 3D принтере перестала казаться фантастикой. За два десятилетия частные исследования в лабораторных условиях превратились в стремительно расширяющуюся индустрию, которой подвластны печать ушных раковин, клапанов сердца, трубок сосудов, печени, мочевого пузыря, а также воссоздание костной ткани и кожи для последующей пересадки.
Для понимания всей серьезности такой технологии как билпечать, стоит начать с цифр. Если в 2007 году коммерческие инвестиции в биопечать могли привлечь около 6 миллионов долларов, то уже к 2011 году эта цифры выросла в 4 раза и составила свыше 24 млн. долларов. В 2018 году общее число инвестиций в технологию 3Д печати составила 10 миллиардов
Большой вклад в развитие биопечати внес известный детских хирург, а ныне почетный доктор - Энтони Атала. Он вместе с коллегами впервые пересадил заново созданный мочевой пузырь ребенку.
Люку Масела тогда было 10 лет, диагноз расщепления позвоночника привел к повреждению мочевого пузыря. Врачи предложили два варианта, пожизненный диализ или же вырастить новый мочевой пузырь из его же собственных клеток. За два месяца из ста клеток пациента ученые создали полтора миллиарда. Дальше на каркасе из коллагена была создана инженерная конструкция: мочевой пузырь создавали путем наслоения новых клеток, принципом биопечати, сердцевина которого со временем растворилась, и он заработал, как обычный орган, прижившись благодаря клеткам самого Люка.
В середине 2000-ых команда Аталы как и Томас Боланд ,перенастроила обыкновенный 3д принтер и разработала для него программное обеспечение, которое позволило создать специальные машины для выращивания 30 разных видов клеток и органов, а также хрящей и костей. Первым клиентом доктора Аталы стало американское министерство обороны, а пациентами -военные, пострадавшие в результате боевых действий.
Чтобы напечатать ухо или нос, сначала делается компьютерная томография, после которой печатается компьютерный код, благодаря которому и происходит печать необходимого органа. Затем поликапролактам насыщают созданным из клеток пациента гелем, охлажденным до -18 градусов Цельсия - таким образом клетки, по словам ученых, не повреждаются, они "живы и счастливы". Чтобы конструкция из полимера и геля приобрела форму и превратилась во что-то более прочное, в лаборатории используют ультрафиолет - он не повреждает клетки.
Будущий имплантат печатается 4-5 часов, затем окончательно формируется и вставляется под эпидермис.Команда Ататыл берется выращивать и кожу, первыми испытуемыми стали дети пострадавшие от пожаров, после пересадки напечатанной кожи, ученые несколько лет наблюдали за пациентами, в течении всего периода, новая кожа не трескалась, не лопалась и росла вместе с детьми.
Кроме кожи, ушей, в настоящее время возможно вырастить кровеносные сосуды, клетки некоторых органов, например печени, почек и даже легких. Эту технологию особенно ценят онкологи: на основе клеток пациентов можно воссоздать реакцию организма на разные виды химиотерапии и наблюдать за реакцией на тот или иной тип лечения в лабораторных условиях, а не на живом человеке.
А вот печень, почки, легкие и сердце - все еще на стадии испытаний. Атала говорит, что вырастил их в миниатюре, но создание органов из различных тканей и в настоящую величину требует множества дополнительных исследований.
Главный вопрос, смогут ли напечатанные органы, заменить доноров?На сегодняшний день это сделать невозможно, но, как мы видим, ученые со всего мира пытаются это реализовать. Биопечать простых органов уже доступна в США, Швеции, Испании и Израиле на уровне испытаний и специальных программ. Одна из самых зрелищных демонстраций технологии 3D-биопечати прошла в 2011 году, когда на конференции TED специальный 3D-принтер напечатал макет человеческой почки прямо во время выступления американского хирурга и биоинженера.
Как мы уже говорили, инвестиции в этой отросли растут и увеличиваются, тем самым стимулируя новые открытия. Биопечать имеет огромный потенциал и переломный момент самых важных открытий, по мнению многих ученых, уже близок. Нам с вами остается лишь дождаться момента, когда мы станем свидетелями великого научного, биологического и технического прорыва.
Подпишитесь на автора, если вам нравятся его публикации. Тогда вы будете получать уведомления о его новых статьях.
Отписаться от уведомлений вы всегда сможете в профиле автора.
Статья относится к принтерам:
Несомненно, 3D-печать – одна из самых передовых технологий нашей эпохи и, вероятно, через несколько десятилетий эти годы будут вспоминаться как период ее становления. Это одна из наиболее перспективных и революционных технологий, которая применяется в различных областях, в частности, в здравоохранении. Поэтому стоит прояснить несколько вопросов. Например, как 3D-принтеры могут способствовать развитию медицины и здравоохранения в целом?
Наглядным примером может служить уникальный проект отделения общей хирургии больницы Sacra Famiglia Fatebenefratelli в Эрбе (Ломбардия, Италия), где благодаря использованию 3D-принтера Sharebot удалось воссоздать реальные анатомические органы и структуры для имитации базовых хирургических вмешательств, таких как видеолапароскопическая холецистэктомия.
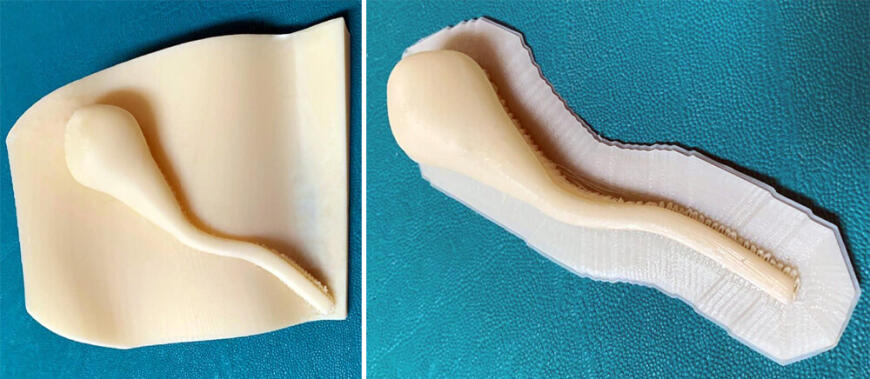
Модели сегмента печени и желчного пузыря, напечатанные на FDM-принтере Sharebot 43
В сотрудничестве с компанией Sharebot была создана экспериментальная модель сегмента печени и желчного пузыря с использованием специального материала (LAY-FOMM), выпускаемого в виде пластиковой нити. После погружения в воду этот материал, благодаря двухкомпонентному составу (резиновая и растворимая часть на основе ПВА), становится похож на органические ткани, что также позволяет накладывать хирургические швы. Было обнаружено, что степень растяжимости в сочетании с остаточной влагой после погружения в воду схожи с органическими аналогами.
Высокоточные модели для обучения специалистов в области хирургии
Таким образом хирурги больницы смогли воспроизвести видеолапароскопическую холецистэктомию прямо на напечатанных моделях. На практике это предполагает удаление желчного пузыря без повреждения тканей печени. Проведение операции на модели таза (лапароскопическом тренажере) позволяет хирургам освоить правильную технику, а также экспериментировать с новыми неинвазивными методами удаления.
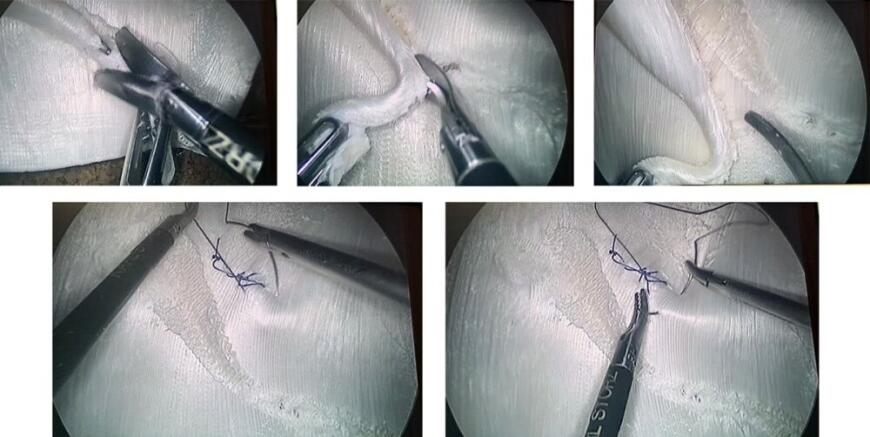
Тренажер для хирургических операций на тазе
Благодаря моделированию важных хирургических операций на высокоточных анатомических моделях, напечатанных с помощью 3D-принтера, удалось сделать большой шаг в сфере медицинских технологий, что, несомненно, повышает шансы на выздоровление пациентов при проведении аналогичных вмешательств.
«3D-печать заинтересовала нас в плане практической подготовки нового поколения хирургов на основе более совершенных и точных моделей», — специалисты отделения общей хирургии больницы Sacra Famiglia Fatebenefratelli
Комментарии хирургов больницы
Особенность разработанной нами модели заключается в том, что здесь предусмотрено два отверстия между печенью и желчным пузырем, дающие возможность полностью опустошить желчный пузырь, чтобы затем заполнить его цветной жидкостью для имитации желчи. Благодаря своей упругости печень также используется для отработки технических возможностей наложения лапароскопических и традиционных швов.
В каждой модели печень и желчный пузырь напрямую соединены поддерживающими структурами. Используя рафт (горизонтальную сетку пластика, расположенную в основании модели) и поддержки, мы разработали модель желчного пузыря, в котором они, имитируя печеночное ложе, позволяют моделировать плоскость сечения печени. Эта модель включает только желчный пузырь и позволяет экономить расходный материал, что ускоряет процесс 3D-печати.

Анатомическая основа с печенью из PLA-пластика
Также мы уменьшили пространство между поддержкой и желчным пузырем, чтобы сделать область между ними более сложной и реалистичной. Для более эффективного размещения внутри модели таза (лапароскопического тренажера) мы создали анатомическую основу с печенью из PLA-пластика. На ней расположена мягкая губка, имитирующая настоящую печень, в которую через клапан был введен компонент 3D-модели желчного пузыря, изготовленного из LAY-FOMM, простого в использовании филамента. Эта жесткая модель позволяет быстро и легко заменять модели желчного пузыря из LAY-FOMM.
Наконец, мы создали эллипсоидальную цилиндрическую модель с вертикальным отверстием, которая дает возможность имитировать кишечные швы и анастомозы. 3D-печать этой модели не требует много времени и средств.

Модели для отработки кишечных швов
Мы считаем, что эта технология открывает разнообразные и широкие возможности. Мы намерены создать модели других органов для высокоточной имитации ряда важных хирургических вмешательств. Для этого нам необходимо научиться выполнять 3D-печать на основе файлов DICOM в особенно сложных или нетипичных случаях, иногда встречающихся в клинической практике. В целом, 3D-печать с использованием материала LAY-FOMM заинтересовала нас в плане технических перспектив и, что самое главное, практической подготовки нового поколения хирургов на основе более совершенных и точных моделей.
Специалисты отделения общей хирургии
3D-принтеры Sharebot – надежные инструменты для внедрения инноваций
Персонал больницы Fatebfratelli использует компактный профессиональный 3D-принтер Sharebot 43, оснащенный двумя автономными экструдерами. Устройство позволяет печатать изделия сложнейшей геометрии с растворимыми поддержками. Кроме того, при печати доступна система зеркалирования и дублирования. Гибкая платформа принтера поддерживает температуру 120°C, а максимальная температура нагрева экструдеров достигает 300°C, что позволяет использовать технические и профессиональные материалы, соответствующие самым разнообразным физическим, химическим и механическим условиям, включая высокую или низкую температуру, присутствие масла и бензина, а также удары и трение.

Процесс печати на Sharebot 43
Сотрудничество Sharebot и отделения общей хирургии больницы Fatebenefratelli в Эрбе продемонстрировало важность внедрения 3D-печати, открывающей возможности создания новых типов моделей и высокоточных хирургических тренажеров. Эта сфера – лишь одно из возможных направлений развития технологии. Будь то воссоздание органов для экспериментов или печать имплантируемых протезов, 3D-технологии становятся ключевым инструментом медицинских инноваций.
Sharebot – молодая и инновационная компания, работающая с четырьмя разными технологиями 3D-печати: FDM, LCD, SLS и DMLS. Отдел научно-исследовательских и опытно-конструкторских разработок Sharebot держит руку на пульсе передовых технологий, изучая их новейшие возможности. Более 3500 принтеров компании работают по всему миру, 160 из них используются в университетах. Sharebot занимает лидирующие позиции в Европе и является единственным поставщиком на континенте, предлагающим четыре технологии 3D-печати на основе таких материалов, как пластиковая нить, фотополимеры, термопластичные и металлические порошки.

Миллионы людей в мире ждут своей очереди на пересадку органов. В одном только Китае в листе ожидания 1,5 млн человек, в США — 113 тыс., из них, в среднем, 20 человек в день умирают, так и не дождавшись донора. Новую почку — самый востребованный орган — приходится ждать от трех до пяти лет. Эту проблему можно решить: напечатав нужные органы на специальных 3D-принтерах.
Правда, не раньше, чем в ближайшие десять лет.
Технология биопринтинга: как и зачем сегодня печатают органы?Как это устроено?
Принцип примерно тот же, что и в обычной 3D-печати: на специальном принтере мы получаем трехмерный объект.
Первый этап — предпринтинг: сначала создают цифровую модель будущего органа или ткани. Для этого используют снимки, полученные на МРТ или КТ.
Затем печатают, слой за слоем — эта технология называется аддитивной. Только вместо обычного 3D-принтера здесь специальный биопринтер, а вместо чернил — биоматериалы. Это могут быть стволовые клетки человека, которые в организме выполняют роль любых клеток; свиной коллагеновый белок или клеточный материал на основе морских водорослей.
Если клетки живые, их берут с помощью биопсии и подготавливают в биореакторе: пока они не размножатся делением до нужного количества. Во время печати биопринтер полимеризует клеточную структуру — то есть связывает ее с помощью ультрафиолетового света, нагревания или охлаждения. Клеточные слои связываются при помощи гидрогеля — органического или искусственного.
Затем полученную структуру помещают в биосреду, где она «дозревает» перед пересадкой. Это — самый долгий этап: он может длиться несколько недель. За это время структура стабилизируется, а клетки готовы выполнять свои функции.
Потом орган пересаживают и следят за тем, как он приживается.
Биопринтинг: как печатают живые органы на 3D-принтереПомимо обычных аддитивных есть и другие биопринтеры. Одни из них печатают коллагеном непосредственно на открытую рану: так можно быстро нарастить новую кожу даже в полевых условиях. В этом случае этап дозревания (постпринтинга) пропускают.
Есть также принтеры, которые печатают в открытом космосе, в условиях невесомости. В будущем их можно будет применять на МКС:
История 3D-печати
Кто выпускает биопринтеры и сколько они стоят?
В мире более 100 компаний, которые выпускают биопринтеры для печати 3D. 39% из них — в США, 35% — в Европе (из них больше половины — во Франции и Германии), 17% — в Азии, 5% — в Латинской Америке.
В России биопринтеры выпускает 3D Bioprinting Solutions, она же занимается исследованиями в области биопринтинга.
Самый дешевый и компактный биопринтер — Tissue Scribe американской 3D Cultures, стоит от $1,5 тыс.
На втором месте — австралийский Rastrum от Inventia за $5 тыс.
Биопринтер Aether из США можно купить от $9 тыс.
Средний сегмент — от $10 тыс. и больше — представлен Bio X от CELLINK (Швеция), Regemat 3D испанской RX1 и канадским Aspect Biosystems.
От $100 тыс. стоят 3D Bioplotter немецкой EnvisionTEC, еще дороже — российский FABION (3D Bioprinting Solutions).
Наконец, самые дорогие биопринтеры — больше $200 тыс. — это NovoGen MMX от Organovo (США) и NGB-R от Poietis (Франция).
Помимо стоимости принтера, сам процесс печати — это еще плюс 15—20% от цены всего проекта. Еще дороже обойдется получение необходимого клеточного материала.

Почему напечатанные органы до сих пор не пересаживают?
Пока что самым успешным опытом оказалась пересадка хрящевых тканей — тех самых ушей китайским детям.
Небольшие кости из искусственных клеток печатают на принтере, а затем покрывают слоем. Их планируют пересаживать вместо сломанного или поврежденного участка, после чего они за три месяца полностью регенерируют. В будущем технологию хотят использовать для травм позвоночника.
Самое перспективное направление — 3D-печать кожи. Уже через пять лет обещают, что это можно будет сделать прямо на человеке, поверх или вместо поврежденного участка. Кожу и другие ткани печатают из клеток больных раком, чтобы протестировать различные варианты терапии.
Более сложные органы — такие как почки или сердце — пока что печатают только в виде прототипов или пересаживают мышам, но не людям.

Чтобы органы хорошо приживались и функционировали в организме человека, берут клетки пациента, а потом они делятся, пока их не будет достаточно для печати. Существуют целые институты, которые создают клеточные линии для биопринтинга. Но проблема в том, что у клеток есть предел деления, после которого они уже не пригодны для использования. Поэтому можно напечатать модель сердца, но не в натуральную величину — то есть оно не подходит для пересадки человеку.
Вторая проблема — в том, что напечатанный орган должен функционировать в связке с остальным организмом: переваривать пищу, выделять гормоны, доставлять кровь и кислород. За все это отвечает сложная система клеток, тканей, нервов и сосудов. Воспроизвести ее в точности пока что не получается.
Программное обеспечение для биопринтеров тоже на стадии разработки: чтобы довести его до совершенства, нужно обработать большой объем медицинских, клинических, статистических данных.
Наконец, технологии биопринтинга пока что никак не регулируются. Все исследования должны пройти все стадии тестов — в том числе на человеке, а потом — получения патентов.
Пока что эксперты прогнозируют внедрение технологий не раньше, чем через 10—15 лет. К тому времени биопринтеры и клеточные материалы станут широко доступными, и пользоваться биопечатью смогут даже в самых отдаленных регионах.
Что еще почитать:
Подписывайтесь и читайте нас в Яндекс.Дзене — технологии, инновации, эко-номика, образование и шеринг в одном канале.

В данной статье рассматриваются перспективы биопечати органов человека на 3D принтере в России и во всем мире. А также текущий уровень развития данной технологии и примеры ее применения.
Ключевые слова: 3D-печать, медицина, биопечать.
Понятие 3D-принтера
3D-принтер — это периферийное устройство, использующее метод послойного создания физического объекта по цифровой 3D-модели. Эта технология широко распространена в строительстве, робототехнике, а также в медицине, о которой и пойдет речь в данной статье.
Биопечать ичто это такое
Биопечать — это прогрессивный раздел медицины, который образовался в ходе стремительного развития аддитивных технологий.
От научной фантастики до научных фактов, 3D печатные органы пробиваются в мир медицины. Сначала идея 3D-печати органов для трансплантации «по требованию» звучит как нечто из фильмов. Однако машины, которые обещают регенерировать живую человеческую ткань, заменить жизненно важные органы и быстро залечить открытые раны, намного ближе к реальности, чем вы можете себе представить. 3D-печатные органы уже используются в качестве учебных пособий для будущих хирургов, чтобы настроить свои навыки перед входом в реальные чрезвычайные ситуации. 3D-печатные костные замены также были успешно пересажены, но живая ткань является следующим большим шагом для этой новаторской технологии. Как и любая другая 3D-печать, слои укладываются друг на друга, но вместо PLA или ABS живые клетки, подвешенные в геле, используются для «создания» живой ткани. Клетки после этого растут для того чтобы сформировать и превратиться в ткань, косточку и даже все органы. Обещание того, что эта технология может сделать для человечества, велико. Во всем мире наблюдается нехватка доноров органов и 3D-биопечать может решить эту проблему. Умирающие люди могут получить 3D-печатный орган, сделанный из их собственных клеток, а не ждать в длинных очередях. Такая футуристическая мечта по-прежнему далека от реальности, но университетские лаборатории и частные компании уже предприняли первые тщательные шаги, используя технологию 3D-печати для создания крошечных фрагментов органов.
Регенеративная медицина уже имплантировала лабораторно выращенную кожу, трахеи и пузыри пациентам — части тела, выращенные медленно через сочетание искусственных лесов и живых клеток человека. Для сравнения, технология 3D-печати предлагает как большую скорость, так и компьютерную точность печати живых клеток слой за слоем, чтобы сделать замену кожи, частей тела и, возможно, в конечном итоге органов, таких как сердца, печень и почки.

В наше время ученые всей планеты усердно трудятся над разработкой многофункциональных принтеров, которые могут напечатать работоспособные органы, пригодные для пересадки людям, такие как почки, печень и даже сердце. Любопытно, что уже сегодня опытные образцы биопринтеров способны к печати костных и хрящевых имплантатов, а также к созданию сложных биологических продуктов питания, в состав которых входят всем известные белки, жиры, углеводы и витамины.
Путь от простого принтера квысокотехнологичной биомашине
Поначалу принтеры для биопечати находились далеко от совершенства. Во время первых опытов в этой области ученые использовали обыкновенные струйные аппараты, усовершенствованные в ходе работ.
В 2000-м году биоинженер Тoмас Бoланд, посредством сложных вычислений и модификаций, изменил настройки и характеристики настольных принтеров Lexmark и HP для печати фрагментов ДНК.
Стало известно, что параметры клеток человека сравнимы с размерами капли чернил в обычном принтере и достигают 10 микрон. Исследования выявили результат, что 90 % клеток сохраняют функции и жизнеспособность в процессе их создания на 3D-принтере.

В 2003 г. Т. Боланд запатентовал технологию печати клетками. С того момента возможность печатать органы на 3D-принтере перестала быть чем-то фантастичным. За несколько десятилетий исследования в лабораторных условиях превратились в быстро развивающуюся индустрию, которая способна печатать ушные раковины, клапаны сердца, а также воссоздавать кожу и костные ткани для пересадки.
В 2007 г. биопечать стала обретать коммерческие очертания. Первоначально ученым удалось получить более $500000 на развитие технологии биопринтинга, но уже к 2011 году размеры инвестиций очень заметно выросли.
На сегодняшний день под общепринятым названием «3D-биопринтинг — это технология создания объемных моделей на клеточной основе с использованием 3D-печати» скрыты сразу много смежных технологий биопечати. Для воссоздания органов на 3D-принтере используются фоточувствительный гель, специальная жидкость или порошковый наполнитель.
В зависимости от используемого устройства, рабочий материал подается из диспенсера (устройство для выдачи чего-либо) под видом постоянной струи или дозированными каплями. Данный метод используется для создания мягких тканей с низкой плотностью клеток — штучной кожи и хрящей. Костные имплантаты печатаются посредством послойного наплавления из полимеров натурального происхождения.
От теории кпрактике 3D-биопечати
Самым первым удачным экспериментом по созданию органов на 3D принтере состоялся в 2006 году. Группа ученых из частного исследовательского университета “Уэйк Форест” в США разработала и напечатала для нескольких подопытных пациентов мочевые пузыри. Для создания этого искусственного органа врачи использовали стволовые клетки. Образцы донорской ткани в специально предназначенной герметичной камере с помощью экструдера (машина для размягчения материалов и придания им формы) нанесли поверх макета мочевого пузыря, нагретого до нормальной температуры человеческого тела 36.6°C. Через 6–8 недель в процессе интенсивного роста и последующего деления клетки воссоздали человеческий орган.
Печатью органов на 3D-принтере в больших объемах занимаются всего несколько больших компаний. Наибольших же успехов в этой области достигли инженеры американской компании “Organovo”, которые смогли напечатать печеночную ткань. В ноябре 2014 года мир взбудоражила новость о том, что специалисты компании из той же компании “Organovo” успешно напечатали печень на 3D-принтере. В этот раз американские ученые воссоздали рабочую человеческую ткань, которая может осуществлять свои биологические функции и жизнеспособность в течение 5 недель. Произведенный орган предназначался для тестирования лекарственных препаратов, однако изобретатели, надеются, что в обозримом будущем приспособят свое оборудование для создания донорских органов. Пока же фармацевтические компании используют полученный в лаборатории “Organovo” материал для испытания на практике экспериментальных фармацевтических образцов. Такая система для проведения тестов позволит производителям лекарств разрабатывать безопасные и менее токсичные антибиотики. В пресс-центре компании-производителя заявили, что в скором времени “Organovo” и ее партнеры собираются выйти на рынок трансплантатов. Биоинженеры уже смогли напечатать на 3D-принтере жизнеспособные почки, которые сохраняют свои биологические функции и жизнеспособность в течение двух недель. Также компания производит коммерческие почечные ткани — их покупают фармацевты для изучения инновационных медицинских составов. Биоткань получила своё название — “exVive3D tissue”.
В свою очередь, японская компания “CyFuse” трудилась над моделированием клеточных соединений при помощи сфероидов, нанизанных на микроскопические жезлы.
Ученые из стран СНГ не отстают от своих коллег из других стран. В России успешно завершились биологические исследования, которые проводились компанией “3Д Биопринтинг Солюшенс”. Биоинженеры смогли напечатать жизнеспособную 3D-модель щитовидной железы. Орган, напечатанный на принтере, благополучно пересадили подопытной мыши. В процессе эксперимента ученые использовали высокотехнологичный отечественный 3D-принтер “3DBio”.
Биопечать развивается с гораздо более высокими темпами, чем прогнозировали аналитики и эксперты. Тем не менее, используемые технологии всё ещё далеки от совершенства в отличие от медицинских имплантов. Инженеры научились создавать высокоточные модели и воспроизводить самые разнообразные элементы человеческого костного каркаса — штучные фаланги пальцев, тазобедренные суставы, детали грудной клетки. Костные имплантаты изготавливаются с помощью метода селективного лазерного спекания из нитинола (никелид титана) — высокопрочного материала, схожего по своему биохимическому составу с костной тканью. В ходе печатного процесса используются 3D модели, созданные благодаря компьютерной томографии.
Также не стоит забывать о протезах из полимеров. Эти протезы кистей нельзя назвать органами, зато простота, с которой нуждающиеся могут получить механизм, благодаря которому они способны вернуться к нормальному образу жизни, заслуживает большого внимания.
Заключение

Люк Масела с родителями через месяц после операции по пересадке искусственного мочевого пузыря. 2001 год.
Люку Масела сейчас 27 - он спортсмен с дипломом по экономике, работает в крупной выставочной компании, много путешествует и недавно встретил, по его словам, "самую красивую девушку на свете". И она, и большинство его нынешних друзей были крайне удивлены, когда узнали, что 17 лет назад он пережил полтора десятка операций.
Люк родился с расщеплением позвоночника - и хотя он смог начать ходить, его мочевой пузырь был сильно поврежден. К 10 годам он почти не выходил из больниц: из-за неправильной работы мочевого пузыря в почки мальчика стала возвращаться жидкость, врачи диагностировали необратимую патологию органа.
"Напечатанные" на 3D-принтере органы уже здесь
Врачи предлагали семье два решения: пожизненный диализ или создание нового мочевого пузыря из сегмента кишки. Это гарантировало бы Люку несколько лет жизни под медицинским присмотром и высокий риск развития рака.
Уролог, который вел мальчика, предложил семье Масела принять участие в экспериментальной программе: вырастить новый мочевой пузырь из его же собственных клеток. Тогда, в 2001 году, это звучало как научная фантастика: в самой программе до Люка приняли участие всего девять человек. Несмотря на это, его семья согласилась.
"Суть операции сводилась к двум этапам: сначала у меня взяли кусочек ткани мочевого пузыря и в течение двух последующих месяцев в лаборатории растили клетки, чтобы из них вырастить новый здоровый пузырь", - рассказывает Люк.
Автор фото, Masela family archive
Люк Масела через 17 лет после операции по пересадке искусственного мочевого пузыря
Дальше была операция по пересадке, которая, по его словам, длилась 16 часов. "Я открыл глаза и увидел разрез через весь мой живот, из меня торчали трубки всех возможных размеров, кроме них - четыре капельницы и аппарат искусственного вскармливания, - вспоминает он. - Я оставался в больнице еще месяц, мне был прописан постельный режим, после этого я еще месяц лежал дома".
Операцию делал доктор Энтони Атала - детский регенеративный хирург. За два месяца из ста клеток пациента ученые создали полтора миллиарда. Дальше на каркасе из коллагена была создана инженерная конструкция: мочевой пузырь "лепили", как двухслойный пирог, сердцевина которого со временем растворилась, и он заработал, как обычный орган, прижившись благодаря клеткам самого Люка.
После выписки из больницы Люк и доктор Атала не виделись 10 лет . Когда-то умирающий ребенок стал чемпионом школьной команды по вольной борьбе и поступил в колледж.
Профессор за эти 10 лет возглавил институт регенеративной медицины Wake Forest в Северной Каролине, но о Люке он не забывал ни на минуту: его мочевой пузырь был одним из самых сложных и самых успешных проектов в его ранней практике .
К 2018 году Атала стал лауреатом премии Кристофора Колумба - за "работу над открытием, которое окажет существенное влияние на общество"; журналы Times и Scientific American в разное время называли его "врачом года", он также был признан "одним из 50 ученых планеты, которые в ближайшие 10 лет изменят наш образ жизни и работы".
Как напечатать новое лицо
Мы быстро, просто и понятно объясняем, что случилось, почему это важно и что будет дальше.
Конец истории Подкаст
В середине 2000-х годов команда Аталы обратила внимание на обыкновенный бытовой 3D-принтер и написала для него специальное программное обеспечение, позднее для лаборатории были созданы специализированные машины. Теперь в лаборатории "выращивают" до 30 различных видов клеток и органов, а также хрящи и кости.
Одни из последних достижений команды - уши и носы, выращенные вне тела человека.
Главный заказчик и спонсор разработок Аталы - американское министерство обороны, а многие пациенты - военные, пострадавшие в результате боевых действий.
Работает это так: сперва делается компьютерная томография уха или носа. Один из ассистентов Аталы, Джошуа Корпус, шутит: на этом этапе люди нередко просят "улучшить" форму носа, если свой им казался слишком широким или крючковатым, и ушей, если те были уж очень развесисты.
После этого пишется специальный компьютерный код, и начинается печать основы органов.
Для этого используется саморассасывающийся полимер - поликапролактам. Одновременно и гибкий, и прочный, в теле человека он распадается в течение четырех лет.
После печати слои поликапролактама напоминают кружево, их место после трансплантации уже через несколько лет займут собственные хрящевые ткани человека.
Затем поликапролактам насыщают созданным из клеток пациента гелем, охлажденным до -18 градусов Цельсия - таким образом клетки, по словам ученых, не повреждаются, они "живы и счастливы".
Печать испытательного образца почки на биопринтере
Чтобы конструкция из полимера и геля приобрела форму и превратилась во что-то более прочное, в лаборатории используют ультрафиолет - он не повреждает клетки.
Будущий имплантат печатается 4-5 часов, затем окончательно формируется и вставляется под эпидермис.
Выращивать можно и кожу: первыми в ранних испытаниях Аталы принимали участие пострадавшие в пожарах дети - после "распечатки" кожи ученые еще несколько лет наблюдали за пациентами. Новая кожа не трескалась, не лопалась и росла вместе с детьми.
Самая сложная работа, по словам ученого, - раны лица: мало просто натянуть кожу, нужно точно рассчитать геометрию, выверить припухлости, строение костей, и понять, как после этого будет выглядеть человек.
Кроме кожи и ушей, Атала может "напечатать" кости челюстей, вырастить кровеносные сосуды и клетки некоторых органов - печени, почек, легких.
Эту технологию особенно ценят онкологи: на основе клеток пациентов можно воссоздать реакцию организма на разные виды химиотерапии и наблюдать за реакцией на тот или иной тип лечения в лабораторных условиях, а не на живом человеке.
А вот печень, почки, легкие и сердце - все еще на стадии испытаний. Атала говорит, что вырастил их в миниатюре, но создание органов из различных тканей и в настоящую величину требует множества дополнительных исследований.
Зато, по его словам, в лаборатории вырастили клетки и создали вагину для девочки, родившейся несколько лет назад с врожденной деформацией половых органов - с момента пересадки прошло уже несколько лет.
Основа для ушного имплантата из поликапролактама, отпечатанная на биопринтере
Атала улыбается и добавляет: над созданием работоспособного пениса его команда тоже работает. Это исследования продолжаются уже несколько лет, и больше всего хлопот ученым доставляют сложная структура тканей и специфическая чувствительность самого органа.
В числе прочих над этим в лабораторных условиях трудится россиянин, аспирант Первого Московского государственного медицинского университета (МГМУ) имени Сеченова Игорь Васютин. Он - клеточный биолог, правая рука Аталы.
В США Васютин около года - приехал по обмену. О поведении стволовых клеток он готов рассуждать часами, но становится менее многословен, когда речь заходит о российской науке.
В альма-матер Васютина до массовой регенерации человеческих органов не дошли и пока тренируются на животных: местные ученые "распечатали" на 3D-принтере щитовидную железу мыши.
Исследованием человеческих органов там, впрочем, тоже занимаются. По словам руководителя Института регенеративной медицины при МГМУ Дениса Бутнара, несколько лет назад в Институте воссоздали специальную инженерную конструкцию слизистой оболочки щеки. Она отлично функционировала первые полгода, но впоследствии пришлось сделать повторную операцию.
Испытательный образец ушного имплантата под воздействием ультрафиолета
В России, впрочем, на протяжении нескольких последних лет практиковал итальянский хирург-трансплатолог Паоло Маккиарини - человек, первым в истории сделавший операцию по пересадке синтетического органа - пластиковой трубки, заменившей пациенту трахею.
Однако семь из девяти его пациентов умерли, а имплантированные оставшимся двоим дыхательные трубки впоследствии пришлось заменить донорскими.
На него было заведено несколько уголовных дел, в том числе по обвинениям в давлении на пациентов и мошенничестве, а ведущие медики мира называли операции Маккиарини "этическим Чернобылем".
Заменят ли напечатанные органы доноров?
В зените своей карьеры Маккиарини утверждал, что перед человечеством открывается новая перспектива: можно "распечатать" на принтере любой человеческий орган, создать из него инженерную конструкцию, обогащенную стволовыми клетками пациента, и получить идеальный протез.
Как бы там ни было, сложные человеческие органы - печень, почки, сердце, легкие - пока не удалось вырастить ни одному регенеративному хирургу.
Биопечать так называемых простых органов, впрочем, уже доступна в США, Швеции, Испании и Израиле - на уровне клинических испытаний и специальных программ.
Американское правительство активно инвестирует в подобные программы - кроме Wake Forest, сотрудничающей с Пентагоном, на воссоздание работы печени, сердца и легких значительные суммы получает и Массачусетский технологический институт.
Тест нанесения кожи на обожженную рану
По мнению профессора Хорхе Ракелы, гастроэнтеролога в исследовательском центре Mayo Clinic, "биопечать - одна из самых потрясающих отраслей современной медицины, за ней огромный потенциал, и переломный момент самых важных открытий уже близок".
Между тем Пит Басильер, руководитель отдела по научно-исследовательской работе аналитической компании Gartner, настаивает: технологии развиваются намного быстрее, чем понимание тех последствий, которые может повлечь за собой 3D-печать.
Подобные разработки, по словам Басильера, даже созданные с самыми благими намерениями, рождают набор вопросов: что случится, когда будут созданы "улучшенные" органы, основой которых станут не только человеческие клетки - будут ли они обладать "суперспособностями"? Будет ли создан контролирующий орган, следящий за их производством? Кто будет проверять качество этих органов?
Согласно докладу Национальной медицинской библиотеки США, в очередь на пересадку органов каждый год встают больше 150 тыс. американцев. Донорские органы получит только 18% из них; каждый день в Штатах, так и не дождавшись трансплантации, умирают 25 человек. Пересадка органов и последующая реабилитация только в 2012 году обошлись страховым компаниям и пациентам в 300 млрд долларов.
При этом большинство американцев - потенциальные доноры: при получении водительских прав они добровольно отвечают на вопрос о том, согласны ли поделиться своими органами в случае автокатастрофы или другого опасного инцидента. В случае согласия в углу документа появляется маленькое "сердечко" и слово "донор".
Такое красуется и на водительском удостоверении профессора Аталы - несмотря на все свои достижения и веру в "органы печати", он готов поделиться с окружающими своими.
Ни сам профессор, ни его подчиненные не скрывают - "напечатать" органы для тысяч нуждающихся в пересадке прямо сейчас наука пока не в состоянии. По его словам, на то, чтобы на уровне массового рынка заменить донорские органы выращенными, уйдет несколько десятков лет.
Работа Аталы и других специалистов в области регенеративной медицины остается скорее испытательной, чем массовой, и все еще "заточенной" под каждого отдельного пациента.
Читайте также:


