Соединения щелочноземельных металлов таблица формула название применение
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
Конспект урока по теме
«Соединения щелочноземельных металлов»
Цель: Обобщить знания учащихся и сформировать у них полное разностороннее представление
о природных соединениях щелочноземельных металлов, их свойствах, значении в
природе и использовании человеком
Задачи: 1) обучающие: усвоение учащимися представлений о природных соединениях
щелочноземельных металлов, их значении в природе и использовании
2) развивающие: развитие умений составлять формулы веществ по их названиям и
давать названия по химическим формулам; записывать уравнения
химических реакций и рассматривать их с точки зрения
ТЭД и ОВР; отработка навыков проведения химического
эксперимента; показать взаимосвязь химии с другими предметами
(биологией, географией, ИЗО) и областями деятельности человека
(медициной, строительством, сельским хозяйством, архитектурой)
3) воспитывающие: патриотическое, эстетическое воспитание, формирование навыков
ЗОЖ (по предупреждению заболеваний опорно-двигательной
- Для лабораторных работ: штатив для пробирок, пробирка, растворы гидроксида кальция, сульфата меди(II) и соляной кислоты, фенолфталеин, коллекции природных соединений щелочноземельных металлов в чашках Петри;
- Для демонстраций: штатив для пробирок, пробирка, оксид кальция, вода, фенолфталеин, скелет человека, зубы млекопитающих, яйца, упаковки от зубных паст, кораллы, жемчуг, мел, мрамор, известняк; коллекция химических соединений щелочноземельных металлов
- Для окончания урока: раздаточный материал
- Технические средства: компьютер, колонки, медиапроектор, экран.
- Организационный момент
- Повторение пройденного материала
- Изучение нового материала: 1) Генетические ряды щелочноземельных металлов на примере кальция. Оксид и гидроксид кальция. Лабораторная работа «Взаимодействие гидроксида кальция с соляной кислотой и сульфатом меди(II)»; 2) Соли щелочноземельных металлов. Лабораторная работа «Ознакомление с образцами природных соединений кальция». Применение солей
- Закрепление полученных знаний
- Домашнее задание
- Окончание урока
1. Организационный момент
2. Повторение пройденного материала
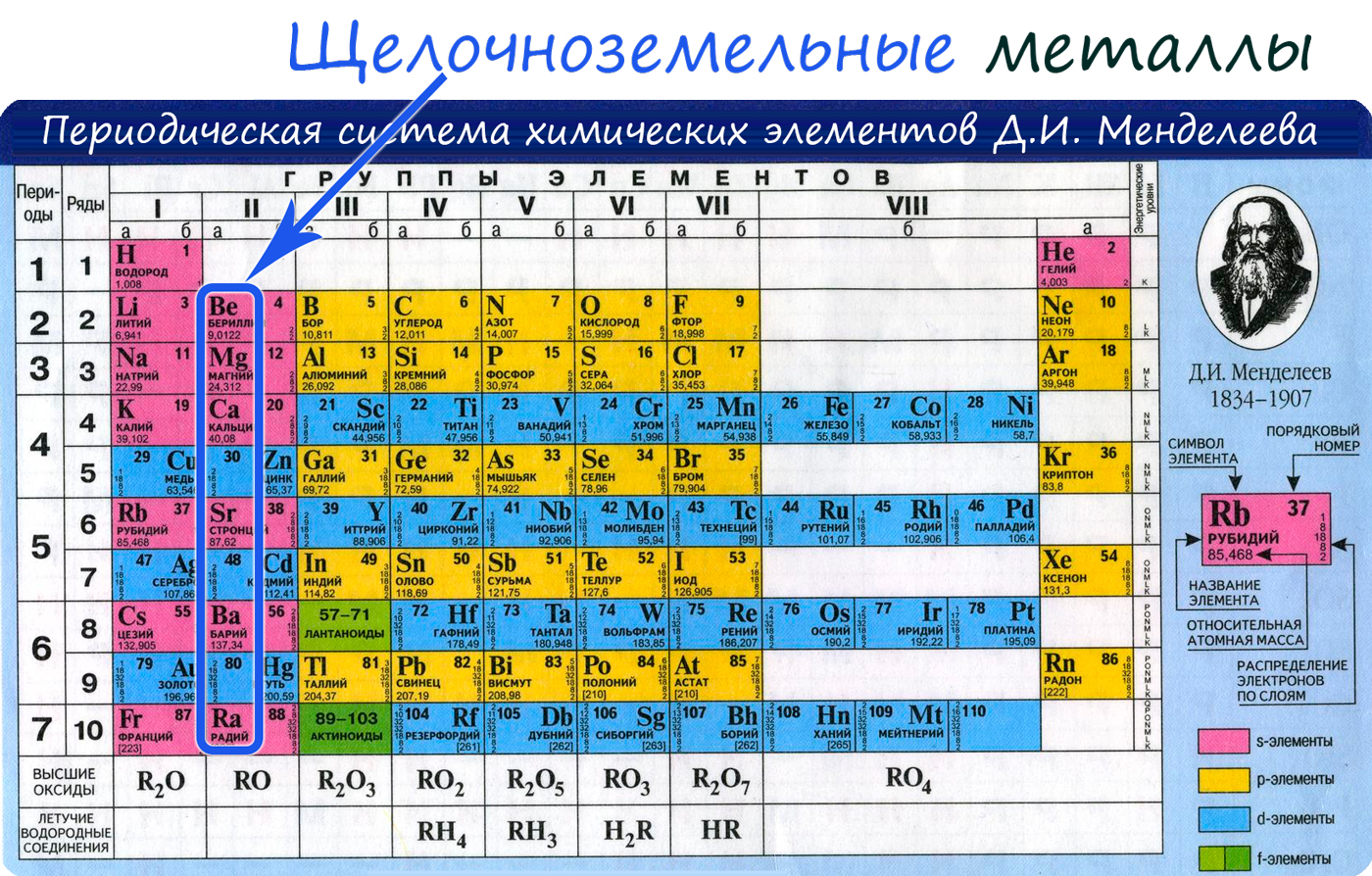
Где в ПСХЭ находятся щелочноземельные металлы?
Какие элементы относятся к щелочноземельным металлам?
Почему они так называются?
Назовите общую особенность в строении атомов элементов II группы главной подгруппы.
Как строение атомов IIА определяет их свойства?
Как меняются металлические свойства элементов IIА группы с увеличением заряда их ядер?
Каково значение кальция в организме человека?
3. Изучение нового материала
Генетические ряды щелочноземельных металлов на примере кальция.
Оксид и гидроксид кальция
Задание. Заполните таблицу:
? Каким цветом выделены формулы и названия оксидов, гидроксидов, солей?
Задание. Используя формулы соединений кальция, составьте генетический ряд этого металла (работа у доски)
Ответ: Ca → CaO → Ca(OH) 2 → CaCO 3
Рассмотрим данные переходы:
- Ca + O 2 → CaO (демонстрация видеоролика) (ОВР у доски)
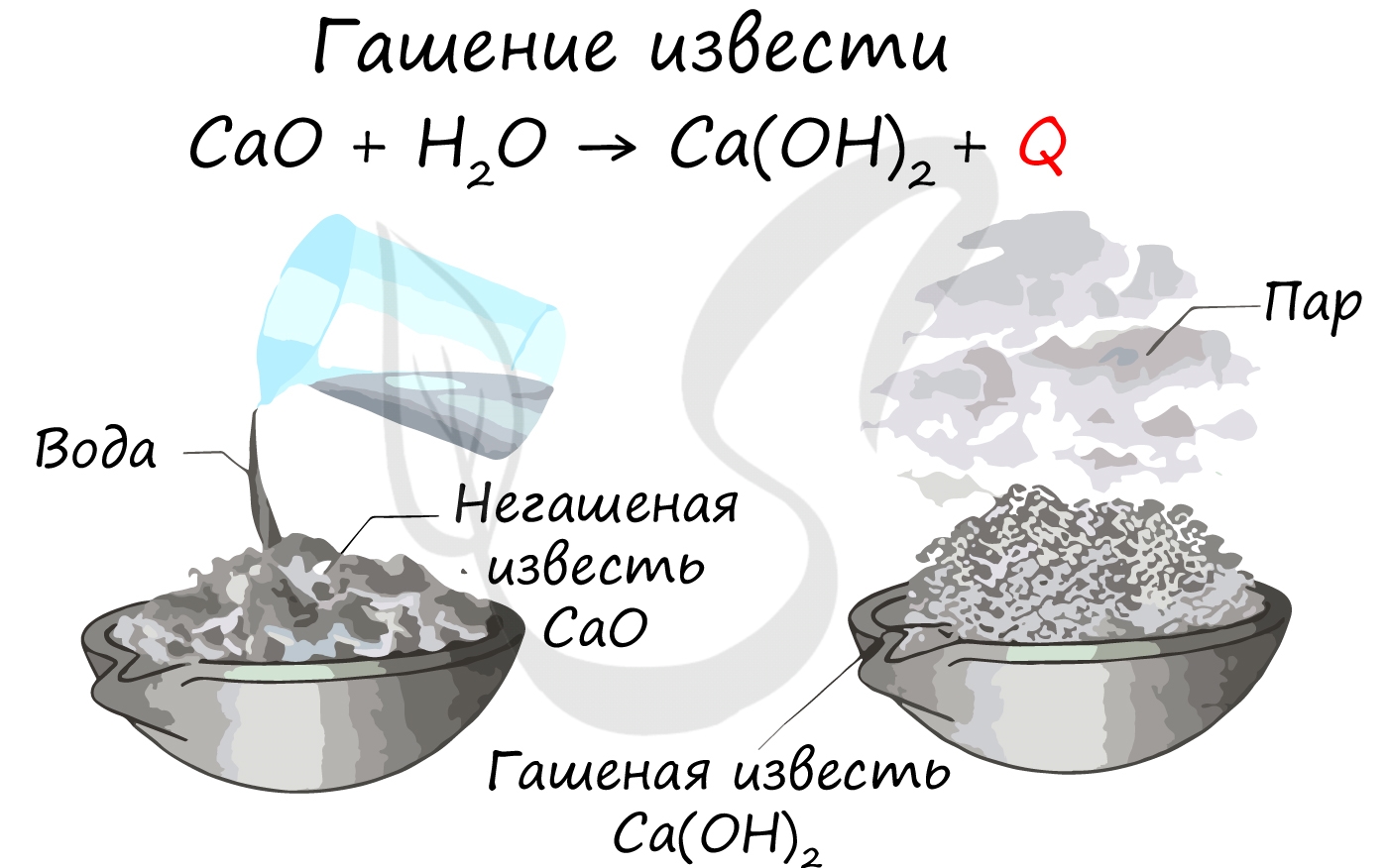
- CaO + H 2 O → Ca(OH) 2 (демонстрация)
Задание. Из предложенного перечня выберите формулы веществ, с которыми может реагировать оксид кальция. Запишите уравнения возможных реакций (самопроверка).
Na, SO 2 , MgO, HCl, CaCl 2 , KOH
Ответ: Как основный оксид CaO реагирует с кислотными оксидами и кислотами, образуя соли:
1. СаO + SO 2 = CaSO 3
2. CaO + 2HCl = CaCl 2 +H 2 O
- Ca(OH) 2 + CO 2 → CaCO 3 (демонстрация биологического опыта «Дыхание») (Качественная реакция)
У травянистых растений газообмен происходит через устьица на листьях и стеблях, у деревьев и кустарников - на стволах через чечевички или трещины
Новые слова : гашёная известь, негашёная известь, гашение, известковая вода, известковое молоко
Задание (работа с текстом учебника): используя текст учебника на странице 63, составьте соответствия
А. Оксид кальция
В. Гидроксид кальция
Г. Реакция оксида кальция с водой, сопровождающаяся выделением большого количества теплоты
Д. Прозрачный раствор гидроксида кальция
Е. Белая взвесь гидроксида кальция в воде
? С какими веществами ещё может реагировать гидроксид кальция? (с кислотами и солями)
Лабораторная работа «Взаимодействие гидроксида кальция с соляной кислотой и сульфатом меди(II)» ТБ!
Ca(OH) 2 + 2HCl→ CaCl 2 + 2H 2 O (ТЭД у доски)
Ca(OH) 2 + СuCl 2 → CaCl 2 + Cu(OH) 2 (ТЭД – дома)
Применение гидроксида кальция:
Задание на дом (дополнительное): Составьте генетический ряд бария
Соли щелочноземельных металлов
На демонстрационном столе – склянки с солями (хлорид, нитрат, карбонат, фосфат, сульфат кальция)
? Опишите физические свойства представленных солей
Данные соединение встречаются и в природе в виде минералов
Лабораторная работа «Ознакомление с образцами природных соединений кальция»
Задание. Рассмотрите образцы и запишите в тетрадь названия природных соединений кальция
На наш урок приглашены специалисты разных областей знаний. В своей работе они не могут обойтись без соединений щелочноземельных металлов.
Задание. По ходу выступлений заполните таблицу:
Самый важный из минералов – известняк (карбонат кальция), без которого не обходится ни одно строительство. Во-первых, он сам является прекрасным строительным камнем. Во-вторых, это сырьё для получения цемента, гашёной и негашёной извести, стекла и др. Известковой щебёнкой укрепляют дороги. Природный мел представляет собой остатки раковин древних животных. Мел применяют для побелки, а также и в школе – школьный мел.
Среднего содержания кальция в почвах (1,37%) вполне достаточно для обеспечения физиологических потребностей растений. Тем не менее, соединения кальция вносят в почвы для химической мелиорации: известковым порошком уменьшают кислотность почв, гипсованием устраняют избыточную щёлочность. Нитрат и фосфаты кальция используются как азотные удобрения.
Минерал скульпторов – мрамор (карбонат кальция). Из него создавал свои прекрасные творения Микеланджело.
Сульфат кальция встречается в природе в виде минерала гипса. Его используют для получения слепков. Для этого применяют полуводный гипс – алебастр.
Гипс используем и мы, медики, для наложения фиксирующих гипсовых повязок. Сульфат магния, известный под названием горькая или английская соль, используют в качестве слабительного средства. Он содержится в морской воде и придаёт ей горький вкус. Сульфат бария благодаря нерастворимости и способности задерживать рентгеновские лучи применяют в рентгенодиагностике («баритовая каша») для диагностики заболеваний желудочно-кишечного тракта. Остальные соединения бария токсичны.
Из всех заболеваний подростков на первом месте стоят нарушения опорно-двигательного аппарата. Одна из причин – недостаточное содержание кальция в пище. Замедление поступления кальция в костную ткань вызывает деформацию костей у взрослых и рахит у детей. Человек должен получать в день 1,5г кальция. Наибольшее его количество содержится в сыре, твороге, петрушке, салате. Другой хороший источник пищевого кальция, часто не берущийся в расчет - мягкие кости лосося и сардин, которые мы съедаем при потреблении этой пищи .
А сколько соединений кальция в составе любой зубной пасты! Из зубной пасты доставляются кальций, фосфор и магний. Кальций и фосфор являются основными строительными элементами эмали зуба. На протяжении всей жизни человека они участвуют в обменных процессах. Необходимость такой добавки обусловлена потребностью зубов в этих элементах при кариесе, и в еще большей степени при некариозных поражениях зубов. Некариозные поражения зубов чаще всего связаны с нарушениями функции щитовидной, поджелудочной, половых желез, заболевания ЖКТ и др., а так же с влиянием внешних неблагоприятных воздействий (ежедневная длительная - более 6 часов - работа с компьютером, экологические влияния) вызывающих заметную убыль минеральных компонентов в тканях зуба, ведущих в начале к повышенной чувствительности зубов, а затем к повреждению в виде кариеса. В связи с этим местное применение паст, содержащих фосфорно-кальциевые добавки, позволяет не только предупредить, но и в известной степени компенсировать потери при наличии заболевания.
Проверка работы некоторых учащихся по заполнению таблицы
Выступление биолога (учитель):
Соединения кальция входят в состав скелетов и зубов позвоночных животных. Такие скелеты называются внутренними, и образованы они фосфатом кальция. На долю кальция приходится более 1,5% массы тела человека, 98% кальция содержится в костях.
? Перечислите функции скелета
! Опорная, защитная, двигательная, кроветворная
А какой ещё тип скелета встречается в природе?
? Какое соединение кальция входит в состав наружного скелета?
? У каких животных наружный скелет образован карбонатом кальция?
! Раковинные корненожки, кораллы, моллюски (раковина, жемчуг)
? Как образуется жемчуг?
! Жемчужина образуется внутри раковины моллюска в результате попадания туда постороннего предмета (песчинки и др.). Далее вокруг предмета -"затравки" происходит отложение перламутровых слоёв. Добыча морского жемчуга ведётся главным образом в Красном море и Персидском заливе , а также у берегов Шри-Ланки и Японии . Пресноводный жемчуг добывается в Германии , России , Китае и странах Северной Америки . В настоящее время ведётся не только поиск природного жемчуга, но и выращивание его в промышленных масштабах (особенно в Японии). Внутрь устрицы помещаются бусинки из прессованных раковин, после чего устрицы возвращаются в воду. Через определённое время бусины, покрытые слоями перламутра, извлекаются из устриц. Искусственный жемчуг в последнее время широко используется как популярный компонент для создания бижутерии и украшений своими руками. Современные технологии позволяют создать искусственные жемчужины любых размеров, форм и цветов, при этом стоимость такого жемчуга существенно ниже натурального. История знает много примеров поистине гигантских жемчужин. Однако ни одна из них не дошла до наших дней: жемчужины не живут больше 150—200 лет, после этого срока камень, увы, рассыпается.
У нас в Карелии есть город, на гербе которого изображён жемчужный венок на голубом поле. Это Кемь. Именно кемский жемчуг из рек Керети, Кеми и Куземки очень хвалили специалисты, считали его образцом пресноводного русского жемчуга «по цвету, блеску и форме». Карельский жемчуг цвет имел серебристый, чуть-чуть голубоватый. Конечно же, самые крупные жемчужные зерна превращали в бусы. Кроме того, им расшивали одежду и головные уборы поморских девушек. В них каждая поморка по праздникам выглядела настоящей царевной. Такими нарядами очень дорожили, берегли их и передавали из поколения в поколение. Мелким жемчугом украшали оклады икон в монастырях, расшивали праздничную одежду священников. Во времена его былой популярности много драгоценных зерен продавалось и за границу. Хитрые иностранные купцы охотно скупали поморский жемчуг, а иногда ввозили его снова в Россию под видом более дорогого «восточного». Поморский жемчуг практически перестали добывать в кемских реках почти 100 лет назад: мало стало перловиц, упали цены на эти прекрасные дары кемских рек. Но времена меняются: сегодня по подсчетам специалистов, в одной из рек северной Карелии обитает около 5 миллионов жемчужниц. Значит, старинный герб Кеми имеет не только историческое значение. Современная Кемь украшена по-настоящему богатым жемчужным венком!
Мы практически ежедневно встречаемся с ещё одним объектом природы, который на 90% образован карбонатом кальция. Отгадайте загадку:
Может и разбиться,
Может и свариться.
Если хочешь , в птенчика
Может превратиться (Яйцо) .
Более десяти лет исследований показали, что яичная скорлупа идеальный источник кальция, который легко усваивается организмом.
Готовят скорлупу так. Яйца моют в теплой воде с мылом, хорошо ополаскивают. Белок и желток выливают из яйца, а скорлупу еще раз прополаскивают и на 5 минут помещают в кипящую воду. Скорлупа яиц, сваренных вкрутую чуть менее активна, но зато готова к использованию. Дозировка от 1,5 до 3 г. в зависимости от возраста. Растереть скорлупу в порошок лучше в ступке. Принимать с утренней едой - с творогами или кашей (раздаточный материал).
Тест с взаимопроверкой
Задание: Какие утверждения верны?
- Все элементы II группы главной подгруппы относятся к щелочноземельным металлам
- Оксид кальция реагирует с кислотными оксидами и кислотами, образуя соли
- Негашёная известь – это гидроксид кальция
- Помутнение известковой воды вызывает угарный газ
- Карбонат и фосфат кальция - это нерастворимые соли
- Алебастр – это полуводный гипс
- Внутренний скелет характерен для позвоночных животных
- В организме человека 98% кальция содержится в костях
- Яичная скорлупа образована фосфатом кальция
- Природный мел представляет собой остатки раковин древних животных
Обязательное: § 12 стр. 62-67, ? 1 на стр. 67, закончите конспект урока
Дополнительное: Составьте генетический ряд бария, запишите уравнения химических
Творческое: Придумайте сказку или задачу с привлечением знаний о щелочноземельных
металлах и их соединений
6. Окончание урока
1. Габриелян, О.С. Химия. 9 класс: учеб. Для общеобразоват. учреждений / О.С. Габриелян. – М.: Дрофа, 2008. – 270 с.
По теме: методические разработки, презентации и конспекты

проверочные и зачетные задания по темам "Щелочные металлы" и "Щелочноземельные металлы"

Свойства Щелочноземельных металлов
щелочноземельные металлы: положение в периодической системе, физические свойства, нахождение в природе, химические свойства, соединения.

Урок по химии 9 класс Соединения магния и щелочноземельных металлов и их применение
Соединения магния и щелочноземельных металлов и их применениеЦель урока: изучить соединения магния и щелочноземельных металлов, знать их формулы и их применение.Задачи урока:Образовательные: 1.

Соединения щелочноземельных металлов
Данная презентация сопровождает изучение учебного материала на уроке химии в 9 классе по теме:"Соединения щелочноземельных металлов".

Проверочная работа "Щелочноземельные металлы и их соединения" (9класс)
Раздаточный материал для проверочной работы (4 варианта). Дополнительные задания можно дать устно.

Конспект урока "Соединения щелочноземельных металлов"
Конспект урока для 9 класса с элементами ФГОС.

Открытый урок по теме: Обзор металлов главных подгрупп ПСХЭ: щелочные и щелочноземельные металлы
Тема урока: Обзор металлов главных подгрупп ПСХЭ: щелочные и щелочноземельные металлы Цель урока: Обобщение и систематизация знаний обучающихся о щелочных и щелочноземельных металлах как о.
Бериллий, магний и щелочноземельные металлы
К главной подгруппе второй группы относятся металлы: бериллий, магний, кальций, стронций, барий, радий.
Щелочноземельные металлы - кальций, стронций, барий, радий.
НАХОЖДЕНИЕ В ПРИРОДЕ
В земной коре содержится бериллия - 0,00053%, магния - 1,95%, кальция - 3,38%, стронция - 0,014%, бария - 0,026%, радий - искусственный элемент.
Встречаются в природе только в виде соединений - силикатов, алюмосиликатов, карбонатов, фосфатов,
MgCO3 – магнезит; CaCO3 • MgCO3 – доломит; KCl • MgSO4 • 3H2O – каинит; KCl • MgCl2 • 6H2O – карналлит
CaCO3 – кальцит (известняк, мрамор и др.); Ca3(PO4)2 – апатит, фосфорит; CaSO4 • 2H2O – гипс; CaSO4 – ангидрит; CaF2 – плавиковый шпат (флюорит)
SrSO4 – целестин; SrCO3 – стронцианит; Ba BaSO4 – барит; BaCO3 – витерит
Физические свойства
Щелочноземельные металлы (по сравнению со щелочными металлами) обладают более высокими t°пл. и t°кип, плотностями и твердостью.
Химические свойства
Очень реакционноспособны, сильные восстановители. Активность металлов и их восстановительная способность увеличивается в ряду: Be–Mg–Ca–Sr–Ba
Возможная степень окисления +2.
1. Взаимодействие с водой.
В обычных условиях поверхность Be и Mg покрыты инертной оксидной пленкой, поэтому они устойчивы по отношению к воде, но с горячей водой магний образует основание Mg(OH) 2.
В отличие от них Ca, Sr и Ba растворяются в воде с образованием гидроксидов, которые являются сильными основаниями:
Ве + H 2 O → ВеO+ H 2
Ca + 2H 2 O → Ca(OH) 2 + H 2
2. Взаимодействие с кислородом.
Все металлы образуют оксиды RO, барий образует пероксид – BaO2:
2Mg + O 2 → 2MgO
Ba + O 2 → BaO 2
3. Взаимодействие с неметаллами:
Be + Cl 2 → BeCl 2 (галогениды)
Ba + S → BaS (сульфиды)
3Mg + N 2 → Mg 3 N 2 (нитриды)
Ca + H 2 → CaH 2 (гидриды)
Ca + 2C → CaC 2 (карбиды)
3Ba + 2P → Ba 3 P 2 (фосфиды)
Бериллий и магний сравнительно медленно реагируют с неметаллами.
4. Взаимодействие с кислотами:
Ca + 2HCl → CaCl 2 + H 2
Mg + H 2 SO 4 (разб.) → MgSO 4 + H 2
5. Качественная реакция на катионы щелочноземельных металлов – окрашивание пламени в следующие цвета:
Ca 2+ - темно-оранжевый; Sr 2+ - темно-красный; Ba 2+ - светло-зеленый
Катион Ba 2+ обычно открывают обменной реакцией с серной кислотой или ее солями:
BaCl 2 + H 2 SO 4 → BaSO 4 ↓ + 2HCl
Ba 2+ + SO 4 2- → BaSO 4 ↓ Сульфат бария – белый осадок, нерастворимый в минеральных кислотах.
Щелочноземельные металлы
К щелочноземельным металлам относятся металлы IIa группы: бериллий, магний, кальций, стронций, барий и радий. Отличаются легкостью, мягкостью и сильной реакционной способностью.
Общая характеристика
От Be к Ra (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционная способность. Уменьшается электроотрицательность, энергия ионизация, сродство к электрону.
- Be - 2s 2
- Mg - 3s 2
- Ca - 4s 2
- Sr - 5s 2
- Ba - 6s 2
- Ra - 7s 2
Природные соединения
- Be - BeO*Al2O3*6SiO2 - берилл
- Mg - MgCO3 - магнезит, MgO*Al2O3 - шпинель, 2MgO*SiO2 - оливин
- Ca - CaCO3 - мел, мрамор, известняк, кальцит, CaSO4*2H2O - гипс, CaF2 - флюорит

Получение
Это активные металлы, которые нельзя получить электролизом раствора. С целью их получения применяют электролиз расплавов, алюминотермию и вытеснением их из солей другими более активными металлами.
MgCl2 → (t) Mg + Cl2 (электролиз расплава)
CaO + Al → Al2O3 + Ca (алюминотермия - способ получения металлов путем восстановления их оксидов алюминием)

Химические свойства
Все щелочноземельные металлы (кроме бериллия и магния) реагируют с холодной водой с образованием соответствующих гидроксидов. Магний реагирует с водой только при нагревании.
Щелочноземельные металлы - активные металлы, стоящие в ряду активности левее водорода, и, следовательно, способные вытеснить водород из кислот:
Хорошо реагируют с неметаллами: кислородом, образуя оксиды состава RO, с галогенами (F, Cl, Br, I). Степень окисления у щелочноземельных металлов постоянная +2.
Mg + O2 → MgO (оксид магния)
При нагревании реагируют с серой, азотом, водородом и углеродом.
Mg + S → (t) MgS (сульфид магния)
Ca + H2 → (t) CaH2 (гидрид кальция)
Ba + C → (t) BaC2 (карбид бария)

Ba + TiO2 → BaO + Ti (барий, как более активный металл, вытесняет титан)
Оксиды щелочноземельных металлов
Имеют общую формулу RO, например: MgO, CaO, BaO.
Оксиды щелочноземельных металлов можно получить путем разложения карбонатов и нитратов:
Рекомендую взять на вооружение общую схему разложения нитратов:

Проявляют преимущественно основные свойства, все кроме BeO - амфотерного оксида.
- Реакции с кислотами и кислотными оксидами
В нее вступают все, кроме оксида бериллия.
Амфотерные свойства оксида бериллия требуют особого внимания. Этот оксид проявляет двойственные свойства: реагирует с кислотами с образованием солей, и с основаниями с образованием комплексных солей.
BeO + NaOH + H2O → Na2[Be(OH)4] (тетрагидроксобериллат натрия)
Если реакция проходит при высоких температурах (в расплаве) комплексная соль не образуется, так как происходит испарение воды:
BeO + NaOH → Na2BeO2 + H2O (бериллат натрия)

Гидроксиды щелочноземельных металлов
Проявляют основные свойства, за исключением гидроксида бериллия - амфотерного гидроксида.
Получают гидроксиды в реакции соответствующего оксида металла и воды (все кроме Be(OH)2)
Основные свойства большинства гидроксидов располагают к реакциям с кислотами и кислотными оксидами.

Реакции с солями (и не только) идут в том случае, если соль растворимы и по итогам реакции выделяется газ, выпадает осадок или образуется слабый электролит (вода).
Гидроксид бериллия относится к амфотерным: проявляет двойственные свойства, реагируя и с кислотами, и с основаниями.
Жесткость воды
Жесткостью воды называют совокупность свойств воды, зависящую от присутствия в ней преимущественно солей кальция и магния: гидрокарбонатов, сульфатов и хлоридов.
Различают временную (карбонатную) и постоянную (некарбонатную) жесткость.
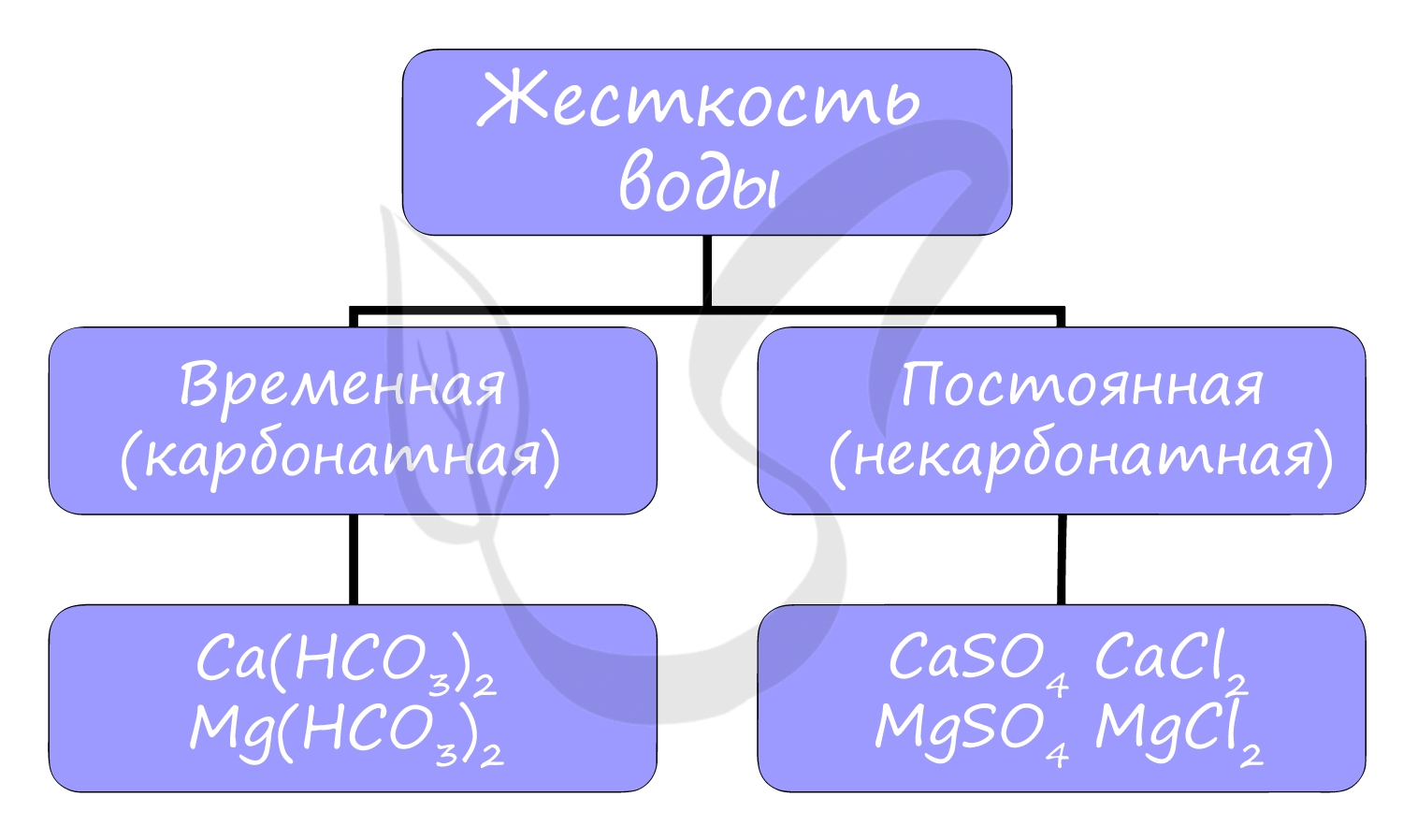
Вероятно, вы часто устраняете жесткость воды у себя дома, осмелюсь предположить - каждый день. Временная жесткость воды устраняется обычным кипячением воды в чайнике, и известь на его стенках - CaCO3 - бесспорное доказательство устранения жесткости:
Также временную жесткость можно устранить, добавив Na2CO3 в воду:
С постоянной жесткостью бороться кипячением бесполезно: сульфаты и хлориды не выпадут в осадок при кипячении. Постоянную жесткость воды устраняют добавлением в воду Na2CO3:
Жесткость воды можно определить с помощью различных тестов. Чрезмерно высокая жесткость воды приводит к быстрому образованию накипи на стенках котлов, труб, чайника.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Щелочные металлы
К щелочным металлам относят химические элементы: одновалентные металлы, составляющие Ia группу: литий, натрий, калий, рубидий, цезий и франций.
Эти металлы очень активны, быстро окисляются на воздухе и бурно реагируют с водой. Их хранят под слоем керосина из-за их сильной реакционной способности.

От Li к Fr (сверху вниз в периодической таблице) происходит увеличение: атомного радиуса, металлических, основных, восстановительных свойств, реакционной способности. Уменьшается электроотрицательность, энергия ионизации, сродство к электрону.

- Li - 2s 1
- Na - 3s 1
- K - 4s 1
- Rb - 5s 1
- Cs - 6s 1
- Fr - 7s 1
- NaCl - галит (каменная соль)
- KCl - сильвин
- NaCl*KCl - сильвинит

Получить такие активные металлы электролизом водного раствора - невозможно. Для их получения применяют электролиз расплавов при высоких температурах (естественно - безводных):
NaCl → Na + Cl2↑ (электролиз расплава каменной соли)
Одной из особенностей щелочных металлов является их реакция с кислородом. Литий в такой реакции преимущественно образует оксид, натрий - пероксид, калий, рубидий и цезий - супероксиды.
K + O2 → KO2 (супероксид калия)
Помните, что металлы никогда не принимают отрицательных степеней окисления. Щелочные металлы одновалентны, и проявляют постоянную степень окисления +1 в различных соединениях: гидриды, галогениды (фториды, хлориды, бромиды и йодиды), нитриды, сульфиды и т.д.
Li + H2 → LiH (в гидридах водород -1)
Na + F2 → NaF (в фторидах фтор -1)
Na + S → Na2S (в сульфидах сера -2)
K + N2 → K3N (в нитридах азот -3)
Щелочные металлы бурно взаимодействуют с водой, при этом часто происходит воспламенение, а иногда - взрыв.
Na + H2O → NaOH + H2↑ (воду можно представить в виде HOH - натрий вытесняет водород)
Иногда в задачах может проскользнуть фраза такого плана: ". в ходе реакции выделился металл, окрашивающий пламя горелки в желтый цвет". Тут вы сразу должны догадаться: речь, скорее всего, про натрий.
Щелочные металлы по-разному окрашивают пламя. Литий окрашивает в алый цвет, натрий - в желтый, калий - в фиолетовый, рубидий - синевато-красный, цезий - синий.

Оксиды щелочных металлов
Имеют общую формулу R2O, например: Na2O, K2O.
Получение оксидов щелочных металлов возможно в ходе реакции с кислородом. Для лития все совсем несложно:
В подобных реакциях у натрия и калия получается соответственно пероксид и супероксид, что приводит к затруднениям. Как из пероксида, так и из супероксида, при желании можно получить оксид:
По свойствам эти оксиды являются основными. Они хорошо реагируют c водой, кислотными оксидами и кислотами:
Li2O + H2O → LiOH (осн. оксид + вода = основание - реакция идет, только если основание растворимо)
Na2O + SO2 → Na2SO3 (обратите внимание - мы сохраняем СО серы +4)
Гидроксиды щелочных металлов
Относятся к щелочам - растворимым основаниям. Наиболее известные представители: NaOH - едкий натр, KOH - едкое кали.
Гидроксиды щелочных металлов получаются в ходе электролиза водных растворов их солей, в реакциях обмена, в реакции щелочных металлов и их оксидов с водой:
KCl + H2O → (электролиз!) KOH + H2 + Cl2 (на катоде выделяется водород, на аноде - хлор)

Проявляют основные свойства. Хорошо реагируют с кислотами, кислотными оксидами и солями, если в ходе реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).
LiOH + H2SO4 → LiHSO4 + H2O (соотношение 1:1, кислота в избытке - получается кислая соль)
2LiOH + H2SO4 → Li2SO4 + 2H2O (соотношение 2:1, основание в избытке - получается средняя соль)
KOH + SO2 → KHSO3 (соотношение 1:1 - получается кислая соль)
2KOH + SO2 → K2SO3 + H2O (соотношение 2:1 - получается средняя соль)
С амфотерными гидроксидами реакции протекают с образованием комплексных солей (в водном растворе) или с образованием окиселов - смешанных оксидов (при высоких температурах - прокаливании).
NaOH + Al(OH)3 → Na[Al(OH)4] (в водном растворе образуются комплексные соли)
NaOH + Al(OH)3 → NaAlO2 + H2O (при прокаливании образуется окисел - смесь двух оксидов: Al2O3 и Na2O, вода испаряется)
Реакции щелочей с галогенами заслуживают особого внимания. Без нагревания они идут по одной схеме, а при нагревании эта схема меняется:
NaOH + Cl2 → NaClO + NaCl + H2O (без нагревания хлор переходит в СО +1 и -1)
NaOH + Cl2 → NaClO3 + NaCl + H2O (с нагреванием хлор переходит в СО +5 и -1)
В реакциях щелочей с йодом образуется исключительно иодат, так как гипоиодит неустойчив даже при комнатной температуре, не говоря о нагревании. С серой реакция протекает схожим образом:
NaOH + I2 → NaIO3 + NaI + H2O (с нагреванием)

NaOH + S → Na2S + Na2SO3 + H2O (сера переходит в СО -2 и +4)
Уникальным является также взаимодействие щелочей с кислотным оксидом NO2, который соответствует сразу двум кислотам - и азотной, и азотистой.
Читайте также:
