Сходства металлов и неметаллов
С физической точки зрения металлы отличаются от неметаллов:
— металлическим блеском (который имеют также и некоторые неметаллы: йод и углерод в виде графита) ;
— возможностью лёгкой механической обработки;
— высокой плотностью (обычно металлы тяжелее неметаллов) ;
— высокой температурой плавления (исключения: ртуть, галлий и щелочные металлы) ;
Все металлы, кроме ртути и франция находятся при нормальных условиях в твёрдом состоянии.
Металлы не отличаются разнообразной цветовой окраской: в основном, все они серые, за исключением красноватой меди и желтоватого золота. Неметаллы гораздо больше разнообразны по цвету.
Металлов намного больше, чем неметаллов, при том, их количество с открытием новых элементов в конце Периодической системы возрастает.
В технике металлы применяются, как констрункциооные материалы, их используют в качестве рабочей части инструментов (также используют алмаз, нитрид бора, керамику) , из металлов изотавливают электрические провода, в то же время их используют и в качестве материалов с повышенным сопротивлением для резисторов и электронагревательных элементов (нихром и т. п.) .
При обычных условиях неметаллы существуют в разных агрегатных состояниях. Из-за отсутствия в кристаллической решётке неметаллов свободных электронов, они плохо проводят тепло и электричество. Большинство из неметаллов не имеет металлического блеска.
С химической точки зрения на внешнем электронном уровне у большинства металлов небольшое количество электронов (1-3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны) . Валентные электроны металлов как правило слабо связаны с ядром, причём с увеличением заряда ядра эта связь ослабевает вследствие большего радиуса атома. Металлы, как правило, реагируют с кислотами (реакция замещения) , причём в зависимости от разбавленности кислоты могут выделяться различные продукты с различной степенью окисления неметаллов в них.
Характерной особенностью неметаллов является большее (по сравнению с металлами) число электронов на внешнем энергетическом уровне их атомов. Это определяет их большую способность к присоединению дополнительных электронов, и проявлению более высокой окислительной активности, чем у металлов.
Неметаллы имеют высокие значения сродства к электрону, большую электроотрицательность и высокий окислительно-восстановительный потенциал.
Благодаря высоким значениям энергии ионизации неметаллов, их атомы могут образовывать ковалентные химические связи с атомами других неметаллов и амфотерных элементов. В отличие от преимущественно ионной природы строения соединений типичных металлов, простые неметаллические вещества, а также соединения неметаллов имеют ковалентную природу строения.
У некоторых неметаллов наблюдается проявление аллотропии. Так, для газообразного кислорода характерны две аллотропных модификации — кислород (O2) и озон (O3), у твёрдого углерода множество форм — алмаз, астралены, графен, графан, графит, карбин, лонсдейлит, фуллерены, стеклоуглерод, диуглерод, углеродные наноструктуры (нанопена, наноконусы, нанотрубки, нановолокна) и аморфный углерод уже открыты, а ещё возможны и другие модификации, например, чаоит и металлический углерод.
В молекулярной форме в виде простых веществ в природе встречаются азот, кислород и сера.
Все инертные газы также встречаются в природе в основном в свободном виде.
Но чаще неметаллы находятся в химически связанном виде: это вода, минералы, горные породы, различные силикаты, фосфаты, бораты. По распространённости в земной коре неметаллы существенно различаются. Наиболее распространёнными являются кислород, кремний, водород; наиболее редкими — мышьяк, селен, иод.
Все металлы наделены металлическим блеском, они превосходные проводники электрического тока и тепла. Большинство из них пластичны, при физическом воздействии металлы легко меняют форму. Неметаллы, наоборот, плохие проводники тепла и электрического тока.
Строение металлов и неметаллов – главная отличительная характеристика. Неметаллы – обладатели большего числа неспаренных электронов, размещающихся на внешних уровнях. Металлы имеют металлическую кристаллическую решетку. А неметаллам присущи молекулярные (к примеру, кислороду, хлору и сере) и атомарные (углероду, образующему алмаз) кристаллические решетки.
металлов маленькая электроотрицательность, а значит и окислительно-восстановительный потенциал невелик. Они, как правило, принимают электроны и окисляются, проявляя восстановительные свойства. Неметаллы, наделенные большой электроотрицательностью и значительным окислительно-восстановительным потенциалом, могут выступать как в качестве окислителей, так и в качестве восстановителей (такое возможно в присутствии наиболее мощного окислителя).
У металлов есть весьма интересное свойство – амфотерность. Амфотерным металлам присущи свойства и металлов, и неметаллов. Например, цинк, находясь в состоянии высшей степени окисления, ведет себя как неметалл.
Металлы и неметаллы
Наш мир наполняют различные простые вещества – металлы или неметаллы. При существовании 120 химических элементов, Вселенную наполняют более 400 простых веществ. Этот парадокс связан с понятием аллотропии – явлением образования одним химическим элементом двух и более простых веществ. Например, атом кислорода может формировать молекулярный кислород О2 и озон О3.
План урока:
Физические свойства металлов
Металлы – химические элементы, атомы которых в процессе реакции стремятся отдавать электроны. Они обладают металлической кристаллической решеткой и общими физическими свойствами. На данный момент известно более 87 металлов.
Для металлов характерен ряд свойств:
- твердость (кроме ртути, которая представляет собой жидкость);
- металлический блеск;
- проводимость электрического тока и тепла;
- пластичность.
Металлы при ударах не разрушаются, а меняют форму. С этой особенностью связано то, что из них производят проволоку, металлические листы и др. Развитие бронзового и железного века связано с производством товаров из металлов.
Физические свойства неметаллов
Неметаллы – химические элементы, атомы которых стремятся принять чужие электроны. Для них характерны атомные и молекулярные кристаллические решетки. Для атомов неметаллов не характерны общие физические свойства. На данный момент существует 22 неметалла.
Для неметаллов характерен ряд свойств:
- хрупкость (неметаллы нельзя ковать);
- отсутствие блеска;
- непроводимость электрического тока и тепла.
Расположение металлов и неметаллов в периодической таблице Д.И. Менделеева
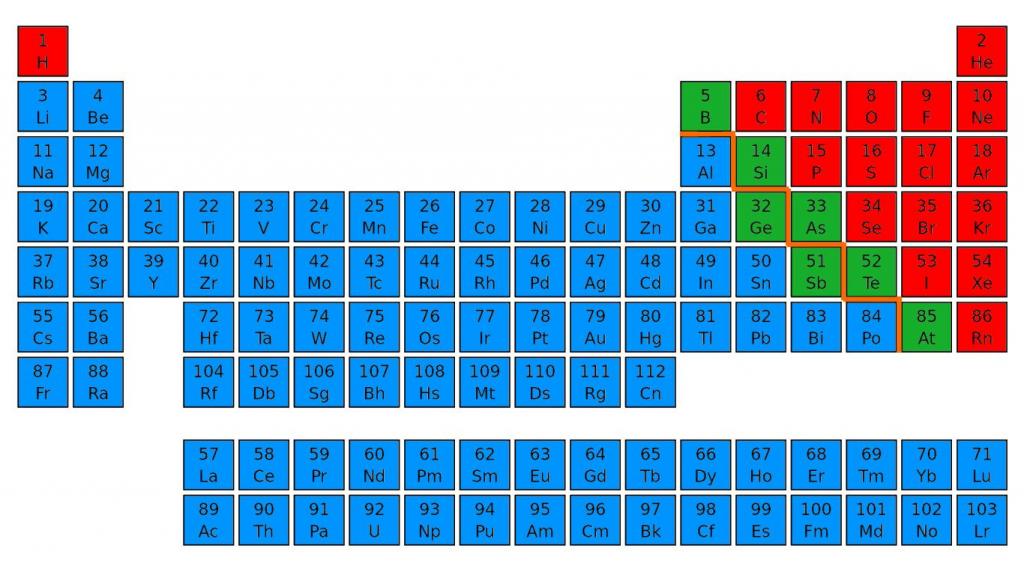
Определить, является простое вещество металлом или неметаллом, можно с помощью периодической таблицы Менделеева. Металлы располагаются ниже диагонали «водород-бор- кремний-мышьяк-теллур-астат», а неметаллы выше.
Красные ячейки – неметаллы, синие – металлы
Элементы, расположенные вблизи диагонали, обладают смешанными свойствами: проявляют как металлические, так и неметаллические свойства. Они называются полуметаллами.
Красные ячейки – полуметаллы
Полуметаллы имеют ковалентную кристаллическую решетку при наличии металлической проводимости (электропроводности). Валентных электронов у них либо недостаточно для образования полноценной ковалентной связи, либо они не удерживаются достаточно прочно из-за больших размеров атома. Поэтому связь в ковалентных кристаллах этих элементов имеет частично металлический характер.
Закономерности в таблице Д.И. Менделеева
Каждый атом состоит из протонов, нейтронов и электронов. Протоны и нейтроны находятся в ядре, который несет положительный заряд. Вокруг ядра движутся отрицательно заряженные электроны. Атомный номер указывает на количество протонов.
Чем больше заряд ядра, тем сильнее к нему притягиваются электроны. Т.о., атому сложнее отдавать электроны. Поэтому в периоде слева направо, с увеличением порядкового номера металлические свойства ослабевают, а неметаллические – усиливаются.
Неметаллы стремятся принять электроны от других атомов. Период в таблице указывает на количество электронных уровней. По мере увеличения числа орбиталей электроны отдаляются от ядра и атому сложнее удерживать электроны на последних уровнях. Т.о., в группе сверху вниз количество орбиталей возрастает, поэтому металлические свойства усиливаются, а неметаллические – уменьшаются.
Способы получения металлов
Большую часть металлов получают из оксидов при нагревании.
Металлы, имеющие на внешнем уровне один-два электрона, получают с помощью электролиза расплавов.
Химические свойства металлов
Все металлы проявляют восстановительные свойства. Легкость в отдачи внешнего электрона применяется в фотоэлементах. Степень активности определяется рядом активности. У самых активных на внешнем уровне располагается по одному электрону.
Общие химические свойства металлов выражаются в реакциях со следующими соединениями.
Активные металлы реагируют с галогенами и кислородом. С азотом взаимодействуют только литий, кальций и магний. Большинство металлов при взаимодействии с кислородом образуют оксиды, а наиболее активные металлы – пероксиды (N2O2).
2 Ca + MnO2 → 2 CaO + Mn(нагревание)
Водород в кислотах вытесняют только те металлы, которые в ряду напряжений стоят до водорода.
Более активные металлы вытесняют из соединений менее активные.
- Химические свойства щелочных и щелочно-земельных металлов (реакции с водой)
2 Na + 2 H2O → 2 NaOH + H2
Способы получения неметаллов
Неметаллы синтезируют из природных соединений с помощью электролиза.
2 KCl → 2 K + Cl2
Также неметаллы получают в результате окислительно-восстановительных реакций.
SiO2 + 2 Mg → 2 MgO + Si
Химические свойства неметаллов
Неметаллы проявляют окислительные свойства. Самый активный неметалл – фтор. Он бурно реагирует со всеми веществами, а некоторые реакции сопровождаются горением и взрывом. В атмосфере фтора горят даже вода и платина. Фтор окисляет кислород и образует фторид кислорода OF2.
Неметаллы вступают в реакции со следующими веществами.
3 F + 2 Al → 2 AlF3 (нагревание)
S + Fe →FeS (нагревание)
Меньшей активностью обладают такие неметаллы как бор, графит, алмаз. Они могут проявлять восстановительные свойства.
2 C + MnO2 → Mn + 2 CO
Коррозия металла
Коррозия – это процесс разрушения металлов или металлических конструкций под действием кислорода, воды и вредных примесей. Не все металлы подвергаются коррозии. Их стойкость зависит от ряда факторов.
- На благородных металлах не образуется коррозия.
- На поверхности алюминия, титана, цинке, хрома и никеля есть оксидная пленка, которая предотвращает процессы коррозии.
Различают несколько видов коррозии – химическую и электрохимическую.
Химическая коррозия
Химическая коррозия сопровождается химическими реакциями. Она образуется под действием газов.
Электрохимическая коррозия
Электрохимическая коррозия – процесс разрушения металлов или металлических конструкций, который сопровождается электрохимическими реакциями. В большинстве металлов находятся примеси. В процессе коррозии электродами могут служить не только металлы, но и его примеси.
Например, в железе могут находиться примеси олова. В этом случае на аноде электроны переносятся от олова к железу и металлы растворяются, т.е. железо подвергаются коррозии. На катоде восстанавливается водород из воды или растворенного кислорода. Электрохимическая коррозия может сопровождаться следующими процессами.
Анод: Fe 2+ - 2e → Fe 0
Катод: 2H + + 2e → H2
Способы защиты от коррозии
В промышленности популярны различные методы защиты металлов от коррозии.
Покрытия защищают поверхности от действия окислителей. Ими служат различные вещества:
- покрытие менее активным металлом (железо покрывают оловом);
- краски, лаки, смазки.
- Создание специальных сплавов
Физические свойства сплавов и чистых металлов отличаются. Поэтому для повышения стойкости в сплав необходимо добавить дополнительные металлы.
Биологическая роль металлов и неметаллов
В организмах содержится множество различных металлов и неметаллов. Различных химических элементов в организме может не хватать, поэтому приходится потреблять их извне.Химические элементы можно разделить на две большие группы – макроэлементы и микроэлементы.
К макроэлементам относятся вещества, содержание которых в организме превышает 0,005 %. Эта группа включает водород, углерод, кислород, азот, натрий, магний, фосфор, сера, хлор, калий, кальций.Микроэлементы – элементы, содержание которых не превышает 0,005%. К ним относятся железо, медь, селен, йод, хром, цинк, фтор, марганец, кобальт, молибден, кремний, бром, ванадий, бор. Каждый макро- и микроэлемент в организме выполняет определенную функцию.
Применение металлов и неметаллов
В синтезе химических препаратов и лекарств применяются чистые металлы и неметаллы. В органической химии металлы используются в качестве катализаторов, а также при получении металлорганических соединений. Неметаллы служат исходным сырьем для получения чистых кислот и других химических соединений.
В чем состоит сходство и различие металлов , неметаллов и амфотерных металлов ?ПГМОГИТЕ СРОЧНО Н…
Металлы и неметаллы: сравнительная характеристика

Все химические элементы условно можно разделить на неметаллы и металлы. Знаете ли вы, по каким признакам они отличаются? Как определить их положение в таблице химических элементов? На эти и другие вопросы вы найдете ответы в нашей статье.
Положение неметаллов и металлов: таблица Менделеева
По внешним признакам и физическим свойствам не всегда можно выяснить, к какой группе относится химический элемент. Свойства металлов и неметаллов можно определить по расположению в периодической таблице.
Для этого нужно зрительно провести диагональ от бора до астата, от 5 до 85 номера. В правом верхнем углу будут преимущественно находиться неметаллы. Их в таблице меньшинство, всего 22 элемента. Металлы находятся в правой части периодической таблицы наверху - в основном в I, II и III группах.
Энергетический уровень
Отличия неметаллов и металлов первоначально обусловлены строением их атомов. Начнем с количества электронов на внешнем энергетическом уровне. У атомов металлов оно варьирует от одного до трех. Как правило, они обладают большим радиусом, поэтому атомы металлов достаточно легко отдают наружные электроны, так как имеют сильные восстановительные свойства.
У неметаллов число электронов на внешнем уровне больше. Это объясняет их окислительную активность. Неметаллы присоединяют недостающие электроны, полностью заполняя энергетический уровень. Самые сильные окислительные свойства проявляют неметаллы второго и третьего периода VI-VII групп.
Заполненный энергетический уровень содержит 8 электронов. Самой большой окислительной способностью обладают галогены с валентностью I. Среди них лидирует фтор, так как у этого элемента нет свободных орбиталей.

Строение металлов и неметаллов: кристаллические решетки
Физические свойства веществ определяются порядком расположения элементарных частиц. Если условно соединить их воображаемыми линиями, то получится структура, которая называется кристаллической решеткой. В ее узлах могут находиться разные структуры: атомы, молекулы или заряженные частицы - ионы.
У некоторых неметаллов формируется атомная кристаллическая решетка, частицы которой соединены ковалентными связями. Вещества с таким строением твердые и нелетучие. К примеру, фосфор, кремний и графит.
В молекулярной кристаллической решетке связь между элементарными частицами слабее. Обычно подобные неметаллы находятся в жидком или газообразном агрегатном состоянии, но в некоторых случаях - это твердые легкоплавкие неметаллы.
В любом образце металла часть атомов теряет наружные электроны. При этом они превращаются в положительно заряженные частицы - катионы. Последние снова соединяются с электронами, образуя нейтрально заряженные частицы - в металлической решетке одновременно находятся катионы, электроны и атомы.

Физические свойства
Начнем с агрегатного состояния. Традиционно принято считать, что все металлы - твердые вещества. Исключением является только ртуть, тягучая жидкость серебристого цвета. Ее пары являются контаминантом - токсичным веществом, вызывающим отравление организма.
Еще одна характерная черта - металлический блеск, который объясняется тем, что поверхность металла отражает световые лучи. Еще одна важная особенность - электро- и теплопроводность. Это свойство обусловлено наличием в металлических решетках свободных электронов, которые в электрическом поле начинают двигаться направленно. Лучше всех проводит тепло и ток ртуть, наименьшими показателями обладает серебро.
Металлическая связь обусловливает ковкость и пластичность. По этим показателям лидирует золото, из которого можно раскатать лист толщиной в человеческий волос.
Чаще всего физические свойства металлов и неметаллов противоположны. Так, последние характеризуются невысокими показателями электро- и теплопроводности, отсутствием металлического блеска. При обычных условиях неметаллы находятся в газообразном или жидком состоянии, а твердые всегда хрупкие и легкоплавкие, что объясняется молекулярным строением неметаллов. Алмаз, красный фосфор и кремний - тугоплавкие и нелетучие, это вещества с немолекулярным строением.

Что такое полуметаллы
В периодической таблице между металлами и неметаллами находится ряд химических элементов, которые занимают промежуточное положение. Их называют полуметаллами. Атомы полуметаллов связаны ковалентной химической связью.
Эти вещества совмещают признаки металлов и неметаллов. К примеру, сурьма является кристаллическим веществом серебристо-белого цвета и вступает в реакцию с кислотами, образуя соли - типичные металлические свойства. С другой стороны, сурьма - очень хрупкое вещество, которое не поддается ковке, а измельчить его можно даже вручную.
Итак, типичные неметаллы и металлы обладают противоположными свойствами, но деление это достаточно условно, поскольку ряд веществ сочетает в себе и те и другие признаки.
Простые вещества
Простые веществаа — химические вещества, состоящие исключительно из атомов одного химического элемента, в отличие от сложных веществ. Являются формой существования химических элементов в свободном виде; или, иначе говоря, химические элементы, не связанные химически ни с каким другим элементом, образуют простые вещества. Известно свыше 400 разновидностей простых веществ.
Химические вещества, состоящие исключительно из атомов одного химического элемента, в отличие от сложных веществ. Являются формой существования химических элементов в свободном виде; или, иначе говоря, химические элементы, не связанные химически ни с каким другим элементом, образуют простые вещества. Известно свыше 400 разновидностей простых веществ.
На странице -> решение задач по химии собраны решения задач и заданий с решёнными примерами по всем темам химии.
Прежде чем приступить к рассмотрению свойств простых веществ, необходимо вспомнить некоторые закономерности, характеризующие способность свободных атомов к перестройке электронной конфигурации. Так, у свободных атомов элементов III периода наблюдаются следующие тенденции:

Результатом реализации отмеченных тенденций, присущих свободным атомам, является образование соответствующих связей в простых веществах. Как известно, в периодах наблюдается постепенный переход от активных металлов (щелочные металлы) к типичным неметаллам (галогены).
При рассмотрении тех же тенденций у свободных атомов в группах периодической системы наблюдаем следующие изменения:

С указанными характеристиками свободных атомов можно связать усиление металлических свойств и ослабление неметаллических с ростом зарядов ядер у элементов одной и той же группы.
Металлы и неметаллы. Относительность деления простых веществ на металлы и неметаллы
Простые вещества, характеризующиеся атомным (ионным) строением и наличием свободных электронов, являются металлами. Эти вещества обладают металлическим блеском, электро- и теплопроводностью. По химическим свойствам металлы являются типичными восстановителями (т. е. легко отдают валентные электроны).
Все простые вещества, образованные атомами элементов дополнительных подгрупп, являются металлами.
Типичными неметаллами являются такие простые вещества^ которые, как правило, состоят из молекул с атомной и ковалентной связью. Не имея свободных электронов, неметаллы по физическим свойствам характеризуются отсутствием электронной проводимости, металлического блеска и т. п. По химическим свойствам многие из них являются энергичными окислителями, так как их атомы обладают сильной склонностью к присоединению электронов.
Рассмотрим фрагмент периодической системы, составленный из элементов главных подгрупп:

Как видно из этой схемы, типичные неметаллы располагаются в правом верхнем углу системы, а металлы — в ее левом нижнем углу.
Валентность перехода, или относительность деления на металлы и неметаллы, выражается в наличии ряда простых веществ, являющихся как бы полуметаллами. При обычных условиях простые вещества, образованные этими элементами, имеют незначительную электропроводность . Поэтому их нельзя отнести ни к неметаллам, ни к металлам. Иногда их называют металлоидами (т. е. неполными металлам). Атомы этих элементов в простом веществе соединяются ковалентными связями. При этом нередко образуются прямые кристаллические структуры, подобные структуре алмаза, в которых каждый атом связан с несколькими другими.
Следовательно, одна из причин относительности деления простых веществ на металлы и неметаллы тесно связана со знанием атомов элементов.
Другая причина относительности такого деления заключается в состоянии внешних условий. Так, при обычных условиях металлы, как известно, характеризуются наличием свободных электронов. Металлическая связь осуществляется и в твёрдом и в жидком состоянии. Но если перевести в пар при определённых условиях (высокие температуры и низкие давления), то он теряет свое характерное свойство — электропроводность. У неметаллов в условии высокого давления наоборот возникает электронная проводимость, что является результатом глубоких изменений в структуре вещества.
Таким образом, структура вещества, тип химической связи, простого вещества могут изменяться под воздействием соответствующих внешних условий. Хорошо известным примером такого рода изменений являются различия физических свойств у различных аллотропных модификаций одного и того же элемента.
Аллотропия
Способность одного и того же элемента существовать в виде нескольких простых веществ называется аллотропией. В настоящее время известно около 400 простых веществ. Причина образования различных аллотропных видоизменений одного элемента кроется в возможности образования новых связей между атомами при изменении внешних условий. В результате образуются молекулы нового состава или новые кристаллические вещества, отличающиеся пространственным расположением атомов.
Так, например, существуют обыкновенный кислород и озон, отличающиеся друг от друга числом атомов в молекуле: кислород О2, и озон О3. Озон образуется при прохождении через воздух электрических разрядов.
Для серы известны два аллотропных видоизменения: ромбическая и призматическая сера. Выше температуры 95,6° С существует призматическая сера, ниже — ромбическая. Изменяется кристаллическая форма (ясно из названия) — изменяются и физические свойства.
Для олова переход одной модификации (серое олово) в другую (белое олово) совершается при температуре 18° С. Здесь также происходит изменение типа кристаллической решетки.
Наличие нескольких аллотропных видоизменений характерно для всех элементов четвертой группы. Рассмотрим, как влияет изменение структуры на физические свойства простых веществ элементов этой группы. Как известно, углерод и кремний принято относить к неметаллам, германий — к полупроводникам, олово и свинец — к металлам. Однако такое деление условно. В этом можно убедиться, рассмотрев, например, аллотропные видоизменения углерода.
В алмазе каждый атом углерода находится в центре правильной треугольной пирамиды (тетраэдр) и соединен ковалентными связями с четырьмя соседними атомами углерода (рис. 6). Таким образом, в таком кристаллическом веществе нет отдельных молекул (это понятие здесь теряет свой смысл). Связи между атомами углерода весьма прочны. Этим объясняется исключительно высокая твердость алмаза, высокая температура плавления и кипения.
В структуре графита плоские слои из атомов углерода расположены шестиугольниками. При этом расстояние между слоями больше расстояния между соседними атомами углерода, находящимися в одном слое (рис. 7). Для образования связей в шестиугольниках от каждого атома углерода требуется три электрона, четвертый же остается «свободным». Этим объясняется электропроводность графита. Поэтому графит используется для изготовления электродов.
Точно так же отличаются физическими свойствами кристаллические модификации олова: белое олово обладает электронной проводимостью, серое является полупроводником.
Выше мы отмечали, что переход одного аллотропного видоизменения в другое происходит при соответствующих условиях. Однако дело в том, что скорость указанного превращения, как правило, незначительна, различные простые вещества одного элемента могут сосуществовать.

рис. 6. Структура алмаза

Если различия между физическими свойствами аллотропных модификаций одного элемента нередко велико, то по химическим свойствам они чаще всего близки. Отличия касаются, главным образом, окислителей (озон — более активный окислитель), скорости реакции с участием простого вещества.
Понятие об окислительно-восстановительных процессах
При первоначальном знакомстве с химией рассматриваются четыре вида химических реакций: реакции соединения, разложения, замещения и двойного обмена.

Цифры над символами элементов означают окислительное число. Мы видим, что одни реакции (1, 3, 5, 6) идут с изменением окислительного числа элементов, другие (2, 4, 7) — без его изменения. На этой основе все химические реакции условно делят на два типа: реакции, идущие с изменением окислительного числа элементов — окислительно-восстановительные реакции — и реакции, течение которых не сопровождается изменением окислительного числа. Первые реакции играют огромную роль в жизни человека, в окружающем нас мире. Окислительно-восстановительные процессы имеют место при горении, дыхании, при получении серной кислоты из серы или сульфидов металлов, при выплавке металлов из руд, при коррозии металлов и сплавов, при работе химических источников электрической энергии.
Что же лежит в основе перечисленных выше процессов? Почему одни простые вещества легко вступают в реакцию друг с другом, тогда как другие нет.
В основе рассматриваемых процессов лежит такая перестройка электронной структуры атомов, составляющих соединение, которая ведет к изменению окислительного числа элементов. Таким образом, в этом случае, как правило, имеет место переход электронов от одних атомов, ионов, молекул к другим. Правда, иногда изменение окислительного числа сопровождается не передачей электронов от одного атома (иона) к другому, а смещением электронных пар:

(вертикальной линией условно обозначена середина межатомного расстояния в рассматриваемых молекулах).
В первом случае из двух простых веществ образуется ионное соединение, во втором — ковалентное полярное. Окислительное число элементов в простых веществах принимается равным нулю.
Окислительное число хлора и в поваренной соли, и в хлористом водороде равно -1, хотя указанные соединения различаются типом химической связи (что и представлено на схеме).
Окислителями называются вещества (атомы, ионы, молекулы), которые в ходе химической реакции присоединяют электроны или оттягивают их от других атомов. В только что рассмотренных примерах в качестве окислителя выступал хлор (С12). В результате реакции окислительное число хлора понизилось.
Восстановителями называются вещества (атомы, ионы, молекулы), вторые в ходе химической реакции отдают электроны для образования ионной или ковалентной связи. В тех же примерах в качестве восстановителей выступали соответственно натрий и водород. В результате реакции окислительное число восстановителей повысилось.
Принципиальная возможность электронной перестройки, наличие потенциального окислителя или восстановителя определяются строением атомов, строением вещества в целом.
Реализация этой возможности в общем случае находится в зависимости от многих факторов: наличия соответствующего партнера, концентрации окислителя и восстановителя, температуры, среды, в котоорой осуществляется реакция, и т. п.
Рассмотрим это на примере реакции взаимодействия двух простых веществ натрия и хлора:
2Na + С12 = 2NaCI
Как известно, для атомов натрия характерно «стремление» к отдаче электрона, для атомов хлора — к присоединению. Следовательно, в данном случае имеет место взаимодействие активного окислителя и активного восстановителя. Реакция осуществляется довольно легко: попаренная соль образуется с большим выделением тепла, в чём легко убедиться на практике. Процессы взаимодействия многих металлов с хлором идут самопроизвольно или при незначительном нагревании (для увеличения скорости реакции). Образовавшиеся при реакции ионы натрия (Na + ) и хлора (СI - ) обладают завершёнными электронными конфигурациями и поэтому, представляет себе возможность течения обратной реакции, мы понимаем, что Na + будет очень плохим окислителем, а СI - — плохим восстановителем. Для осуществления такой реакции потребуется значительная затрата энергии (высокие температуры). При обычных условиях натрий и хлор из поваренной соли получают электролизом расплава поваренной соли.
Ранее, рассматривая вопрос о положении водорода в периодической системы, мы указывали на сходство водорода как со щелочными металлами, так и с галогенами. Это сходство проявляется, в частности в том, что подобно щелочным металлам, водород может выступать в качестве восстановителя, но с другой стороны, подобно галогенам, способен быть и окислителем. Причина двух способов изменения электронной конфигурации нейтрального атома водорода заключается в особенности строения атомов I периода (первый энергетический уровень заполняется двумя электронами). Изменение
окислительного числа водорода можно представить следующим образом:
В первом случае водород выступает как восстановитель, во втором — как окислитель. Например:

Таким образом, мы прежде всего должны учитывать принципиальные возможности присоединять или отдавать электроны, т. е. возможности, прямо вытекающие из строения атомов и окислительного числа элемента в соединении. В нашем примере водород (Н2) может выступать и в роли окислителя и в роли восстановителя. Какая из этих двух возможностей будет реализована, зависит от партнера по реакции, от того, с каким веществом (окислителем или восстановителем) будет взаимодействовать водород.
Как же связать окислительные и восстановительные свойства простых веществ с положением элементов в периодической системе? Рассмотрим конкретные примеры. Например, окислительная способность в ряду галогенов убывает от хлора к йоду:
Восстановительную способность металлов отражает ряд активности (напряжения) металлов который составлен с учетом последовательности вытеснения металлов из растворов их солей.
По-иному будет выглядеть ряд, иллюстрирующий способность металлов образовывать соединения с кислородом или азотом, водородом или фтором и т. д.
В группах периодической системы восстановительные свойства простых веществ, как правило, усиливаются, а окислительные — падают. Однако это общее положение нуждается в уточнении, когда мы приступаем к изучению некоторых конкретных примеров. Число реакций, в которых данный элемент может выступать, скажем, в качестве восстановителя, достаточно велико, а процесс окисления— восстановления зависит от многих факторов, которые мы пока еще не рассматривали.
Услуги по химии:
Лекции по химии:
Лекции по неорганической химии:
Лекции по органической химии:
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
Читайте также:
