Семь металлов известные человеку с глубокой древности
Презентация на тему: " Семь «доисторических металлов» А втор : К ожина А. Преподаватель : Кудрявцева Н. В." — Транскрипт:
1 Семь «доисторических металлов» А втор : К ожина А. Преподаватель : Кудрявцева Н. В.
2 Уже в глубокой древности человеку были известны семь металлов : золото, медь, серебро, олово, свинец, железо, ртуть. Эти металлы можно назвать « доисторическими », так как они применялись человеком еще до изобретения письменности. Часы истории человечества стали отсчитывать время быстрее, когда в его жизнь вошли металлы и, что важнее всего их сплавы. Каменный век Медный век Бронзовый век Железный век
3 « Содержание » 1.« Царь металлов » 2.« Некоторые светлые тяжелые камни » 3.« Серебро в медицине » 4.« Живое серебро » 5.« Железо » 6.« Медь » 7.« Олово » 8.« Свинец »
4 « Царь металлов » Его мерцающий блеск возбуждал людскую алчность, манил вдаль бесчисленных искателей приключений, становился причиной кровавых войн. Еще в глубокой древности золотистый цвет металла ассоциировался в сознании людей с цветом солнца. Так, по одной из версий, русское название металла происходит от слова « солнце ». Латинское название ( AURUM) в переводе « жёлтый » « О, если бы оно могло быть совсем изгнано из жизни !» Плиний Старший
5 З олото н е м еняющееся п ри х ранении н а в оздухе, н е поддающееся р жавлению, я влялось с имволом в ечности. В природе з олото в стречается в в иде м елких з ерен, перемешанных с п еском. Н о и ногда н аходят и к рупные самородки - м ассой н есколько д есятков к илограммов. В н аше в ремя о коло половины п роизводимого золота и спользуют в ювелирном д еле. Ю велиры никогда н е р аботают с чистым м еталлом. З олото с п римесями и меет р азные о ттенки : о т желтого и к расно - коричневого о р озоватого и ли д аже зеленоватого. « М ечта а лхимика »
6 Д ревнейшие л атинское н азвание с еребра ( a r g e n t u m ) « белый », « блестящий ». Р усское ж е с лово « серебро » происходит о т с лова « серп » л уны. «НЕКОТОРЫЕ ТЯЖЁЛЫЕ И СВЕТЛЫЕ КАМНИ. » И з с еребра ч еканили м онеты – ч еловечество и здана отвело э тим м еталлам р оль м ерила с тоимости т овара. Древние р имляне н ачали ч еканить с еребряные м онеты с 269 г. д о н. э. – н а п олстолетия р аньше ч ем з олотые. С еребро б лестящий, с еребристо - белый м еталл (tm = 962 ° С ), к овкий и пластичный, л учший с реди м еталлов п роводник т епла и э лектричества. В с тарину и з н его и зготовляли м онеты, в азы, к убки, ю велирные и зделия, тончайшими с еребряными п ластинами у крашали л арцы и о деяния. Н а Руси и з с еребра д елали ц ерковные с осуды, о клады и кон.
7 СЕРЕБРО В М ЕДИЦИНЕ Серебро с д авних в ремён и спользуют д ля л ечения различных б олезней. В н аши д ни в м едицинской п рактике применяют н итрат с еребра, в к отором э тот м еталл находится в р астворе в в иде м ельчайших т вёрдых частиц. Ч тобы о н н е в ыпадал в о садок, в н его в водят специальные с табилизирующие д обавки. Использование н итрата с еребра о бусловлено его а нтимикробной а ктивностью. В небольших к онцентрациях п репарат оказывает п ротивовоспалительное действие, а в б олее к репких р астворах прижигает т кани. Ч аше в сего н итрат серебра в в иде в одных р астворов п рименяют наружно д ля л ечения г лазных з аболеваний. Сплав о дной ч асти н итрата с еребра и д вух частей н итрата к алия п од н азванием « ляпис » п рименяют д ля н аружного прижигания.
8 Н азывали е ё и Mercurius, п одчёркивая т ем с амым е ё близость к ц арю м еталлов з олоту.( М еркурий б лижайшая к Солнцу п ланета. С имвол р тути с овпадает с о бозначением планеты М еркурий у а строномов. « ЖИВОЕ С ЕРЕБРО » Ртуть - argentum vivum ( ж ивое с еребро ) hydrar-girum (« жидкое с еребро ») Р туть б ыла и звестна л юдям уже в о II т ысячелетии д о н. э. Алхимики с читали е ё ж енским началом в еществ, м атерью металлов, о сновой ф илософского камня.
9 . Р туть (t. к ип = 357 ° С ) с амая т яжёлая и з в сех и звестных жидкостей л итр е ё п ри 20 ° С в есит 13,6 к г. О бычная с теклянная б анка п од т яжестью р тути р аскалывается. Поэтому б ольшие к оличества р тути х ранят в с пециальных с осудах либо в ж елезных ё мкостях. Н изкая т емпература п лавления р тути (-39 ° С ) о бъясняется т ем, ч то а томы Hg п рочно у держивают с вои валентные э лектроны и с т рудом п редоставляют и х в « общее пользование *. К ристаллическая р ешётка р тути н еустойчива. П оэтому р туть п лохо проводит т епло и э лектрический т ок. « Тяжелая в ода »
10 Многие х орошо р астворяются в р тути с о бразованием а мальгам жидких и т вёрдых с плавов. Э тим с войством р тути п ользовались для п олучения з еркал п утем н анесения п а с текло а мальгамы о лова. Способность р тути р астворять н атрий и к алий и спользуют п ри электролитическом п олучении щ елочей. Жидкая р туть р авномерно р асширяется п ри н агревании, п оэтому ею з аполняют т ермометры. Ртуть, в о тличие о т с воих с оседей п о п одгруппе, м алоактивный металл. Р астворить е ё м ожно в ц арской в одке и ли концентрированной а зотной к ислоте : Hg 4 IHN'O, = Hg(NO;), + 2NO, Н, О, ' Почти в се м еталлы, к роме з олота, с еребра и п латины, с пособны вытеснять р туть и з р астворов е ё с олей «Волк, пожирающий царя» аллегория, отражающая способность ртути растворять золото. Раскрашенная гравюра. XVII в.
11 Одна часть железа приравнивалась к десяти частям золота. Во-первых, оно было самым прочным из известных тогда металлов, незаменимым при изготовлении оружия и орудий труда. Вторая причина сложность добычи железа. (Железо в старину получали «сыродутным» способом. Железную руду и уголь загружали в печи, имевшие форму длинной трубы. Уголь поджи- 1~али, а ветер, дующий в трубу, поддерживал высокую температуру (около 1400°С), необходимую для восстановления железа из оксидной руды. Полученный металл (крипу) ковали, в процессе ковки от него отделялись куски шлака, и оставалось чистое железо. В некоторых странах этим способом металл выплавляли вплоть до XVIII в.) с 269 С в о б о д н о к о н в е р т и р у е м а я в а л ю т а в о в с е н е п р и з н а к т о л ь к о н а ш е г о в р е м е н и Н о п р е д с т а в и т ь с е б е, ч т о в с е о б щ е й м е р о й ц е н н о с т е й к о г д а - т о б ы л о ж е л е з о, м ы м о ж е м с б о л ь ш и м т р у д о м. А м е ж д у т е м в о в р е м е н а Г о м е р а « о д н и п о к у п а л и в е щ и н а б ы ч ь и ш к у р ы, д р у г и е н а ж е л е з о и п л е н н ы х *, к а к « Ж ЕЛЕЗО » Свободно к онвертируемая в алюта в овсе н е признак т олько н ашего в ремени. Но представить с ебе, ч то в сеобщей м ерой ценностей к огда - то б ыло ж елезо, м ы м ожем с большим т рудом. А м ежду т ем в о в ремена Гомера « одни п окупали в ещи н а б ычьи ш куры, другие н а ж елезо и п ленных. Железные слитки.
12 « Медь » Л атинское н аименование м еди Cuprum п роисходит о т названия о строва К ипр, г де у же в III в. д о н. э. с уществовали медные р удники. Р усское « медь » в осходит к с лову « смида », обозначавшему м еталл у д ревних г ерманцев. Х отя м едь и ногда в стречается в п рироде в в иде самородков ( самый б ольшой и з н айденных в есил 420 т ), основная е ё ч асть в ходит в с остав с ульфидных р уд. В п ервых м еталлургических п роцессах и спользовались н е сульфид ные р уды, а и менно м алахит, н е т ре бующий предварительного о бжига
13 Оно известно человечеству по крайней мере с середины III тысячелетия до н, э. В природе встречается в виде минерала касситерита (от грвч. «касситерос» «олово») месторождения которого довольно редки: в древности его добывали лишь в Испании, на Кавказе и в Китае. Олово ценилось ещё во времена Троянской войны. И называлось - «белый свинец» « Олово »
14 Олово мягкий серебристо-белый блестящий металл, пластичный и ковкий. Отлитая из олова палочка сгибается с характерным хрустом, вызванным трением друг о друга отдельных кристаллов. Но 13,2 "С устойчива другая модификация серое олово, которое имеет структуру алмаза. (Переход белого олова в серое при низкой температуре часто происходит спонтанно, хотя для проведения его в лабораторных условиях требуется ввести небольшую затравку серого олова. Этот переход называют «оловянной чумой»: металл рассыпается в серый порошок, утрачивая металлические свойства. Она послужила причиной гибели в 1912 г. английской экспедиции под руководством Роберта Скотта, направленной к Южному полюсу: керосин путешественники хранили в сосудах, паянных оловом.)
15 Сильный восстановитель.. Около 60 % всего производимого олова сплавы..Используется для производства подшипников используют баббиты сплавы на основе олова, содержащие около 10 % сурьмы и около 5 % меди. Первый подобный сшив был создан в 1839 г. американским изобретателем Исааком Баббиттом. Плёнку из олова наносят на железо, чтобы предохранить его от ржавления. Такая обработка называется лужением. Для защиты от действия органических кислот, содержащихся в пищевых продуктах, жестяные банки для хранения консервов тоже покрывают слоем олова. « Олово »
16 «Свинец» Свинцовые самородки крайне редко встречается в природе. (Однако в виде соединения с серой свинцового блеска, свинец был известен уже древним мастерам. Красивые, блестящие кристаллы этого вещества привлекли внимание. Если положить их в костёр, разведенный в неглубокой яме, на дно её вскоре стечёт расплавленный металл, ведь температура плавления свинца невысока 327 °С.) Интересно, что и в наши дни в основе промышленного производ ства свинца лежат те же химические реакции прокаливание свинцового блеска на воздухе.
Древнейшие металлы человечества
“Семь металлов создал свет по числу семи планет” — в этих немудреных стишках был заключен один из важнейших постулатов средневековой алхимии. В древности и в средние века и было известно лишь семь металлов и столько же небесных тел (Солнце, Луна и пять планет, не считая Земли). По мнению тогдашних светил науки, не увидеть в этом глубочайшую философскую закономерность могли только глупцы да невежды. Стройная алхимическая теория гласила, что золото представлено на небесах Солнцем, серебро — это типичная Луна, медь, несомненно, связана родственными узами с Венерой, железо олицетворяется Марсом, ртуть соответствует Меркурию, олово — Юпитеру, свинец — Сатурну. До XVII века металлы и обозначались в литературе соответствующими символами.
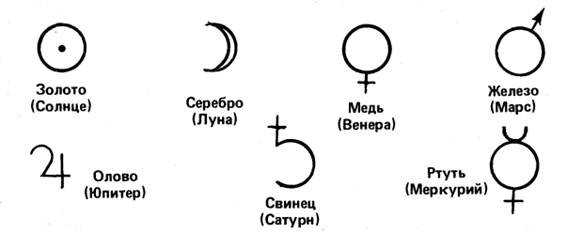
Рисунок 1 - Алхимические знаки металлов и планет
В 1789 г. французский химик Лавуазье дает перечень известных тогда 17 металлов: к перечисленным выше добавились - сурьма, мышьяк, висмут, кобальт, марганец, молибден, никель, платина, вольфрам, цинк.
В настоящее время известно более 80 металлов, большинство которых используется в технике.
С 1814 г. по предложению шведского химика Берцелиуса для обозначения металлов используются буквенные знаки.
Первым металлом, который человек научился обрабатывать, было золото. Самые древние вещи из этого металла изготовлены в Египте примерно 8 тыс. лет назад. В Европе 6 тыс. лет тому назад первыми начали изготовлять из золота и бронзы ювелирные украшения и оружие фракийцы, жившие на территории от Дуная до Днепра.
Историки выделяют три этапа в развитии человечества: каменный век, бронзовый и железный.
В 3 тыс.до н.э. люди начали широко применять в своей хозяйственной деятельности металлы. Переход от каменных орудий к металлическим имел колоссальное значение в истории человечества. Пожалуй, никакое другое открытие не привело к таким значительным общественным сдвигам.
Первым металлом, получившим широкое распространение, была медь (рисунок 2).
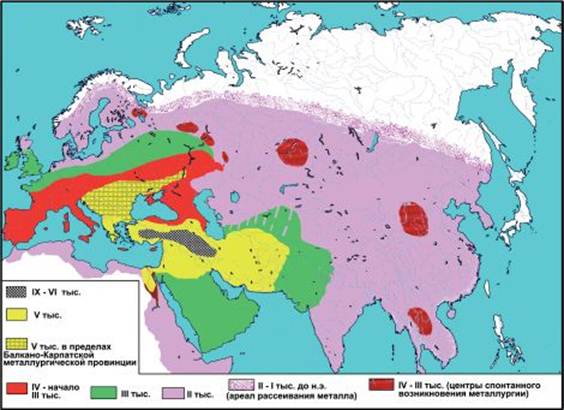
Рисунок 2 - Карта-схема территориально-хронологического распространения металлов в Евразии и Северной Африке
На карте хорошо видно расположение древнейших находок металлических изделий. Почти все известные артефакты, относящиеся к периоду с конца IX по VI тыс. до н.э. (т.е. до того, как в Месопотамии широко распространилась культура типа Урук), происходят всего из трех десятков памятников, рассеянных по обширной территории в 1 млн. км 2 . Отсюда извлечено около 230 мелких образцов, причем 2/3 из них принадлежат двум поселениям докерамического неолита — Чайоню и Ашикли.
Постоянно разыскивая необходимые им камни, наши предки, надо думать, уже в древности обратили внимание на красновато-зеленые или зеленовато-серые куски самородной меди. В обрывах берегов и скал им попадались медный колчедан, медный блеск и красная медная руда (куприт). Поначалу люди использовали их как обыкновенные камни и обрабатывали соответствующим способом. Вскоре они открыли, что при обработке меди ударами каменного молотка ее твердость значительно возрастает, и она делается пригодной для изготовления инструментов. Таким образом, вошли в употребление приемы холодной обработки металла или примитивной ковки.
Затем было сделано другое важное открытие — кусок самородной меди или поверхностной породы, содержавшей металл, попадая в огонь костра, обнаруживал новые, не свойственные камню особенности: от сильного нагрева металл расплавлялся и, остывая, приобретал новую форму. Если форму делали искусственно, то получалось необходимое человеку изделие. Это свойство меди древние мастера использовали сначала для отливки украшений, а потом и для производства медных орудий труда. Так зародилась металлургия. Плавку стали осуществлять в специальных высокотемпературных печах, представлявших собой несколько измененную конструкцию хорошо известных людям гончарных печей (рисунок 3).
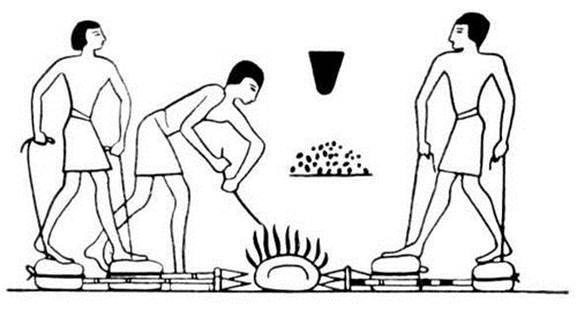
Рисунок 3 - Плавка металла в Древнем Египте (дутьё подаётся мехами, сшитыми из шкур животных)
В Юго-Восточной Анатолии археологи открыли очень древнее поселение докерамического неолита Чайоню Тепеси (рисунок 4), которое поразило неожиданной сложностью каменной архитектуры. Ученые обнаружили среди руин около сотни мелких кусочков меди, а также множество осколков медного минерала — малахита, некоторые из них были обработаны в виде бусин.

Рисунок 4 - Поселение Чайоню Тепеси в Восточной Анатолии: IX-VIII тысячелетия до н.э. Здесь был обнаружен древнейший металл планеты
Вообще говоря, медь — мягкий металл, сильно уступающий в твердости камню. Но медные инструменты можно было быстро и легко затачивать. (По наблюдениям С.А. Семенова, при замене каменного топора на медный, скорость рубки увеличивалась примерно в три раза.) Спрос на металлические инструменты стал быстро расти.
Люди начали настоящую «охоту» за медной рудой. Оказалось, что она встречается далеко не везде. В тех местах, где обнаруживались богатые залежи меди, возникала их интенсивная разработка, появлялось рудное и шахтное дело. Как показывают открытия археологов, уже в древности процесс добычи руды был поставлен с большим размахом. Например, вблизи Зальцбурга, где добыча меди началась около 1600 году до Р.Х., шахты достигали глубины 100 м, а общая длина отходящих от каждой шахты штреков составляла несколько километров.
Древним рудокопам приходилось решать все те задачи, которые стоят и перед современными шахтерами: укрепление сводов, вентиляция, освещение, подъем на гора добытой руды. Штольни укрепляли деревянными подпорками. Добытую руду плавили неподалеку в невысоких глиняных печах с толстыми стенками. Подобные центры металлургии существовали и в других местах (рисунки 5,6).

Рисунок 5 – Древние рудники

Рисунок 6 – Орудия древних рудокопов
В конце 3 тыс.до н.э. древние мастера начали использовать свойства сплавов, первым из которых стала бронза. На открытие бронзы людей должна была натолкнуть случайность, неизбежная при массовом производстве меди. Некоторые сорта медных руд содержат незначительную (до 2%) примесь олова. Выплавляя такую руду, мастера заметили, что медь, полученная из нее, намного тверже обычной. Оловянная руда могла попасть в медеплавильные печи и по другой причине. Как бы то ни было, наблюдения за свойствами руд привели к освоению значения олова, которое и стали добавлять к меди, образуя искусственный сплав — бронзу. При нагревании с оловом медь плавилась лучше и легче подвергалась отливке, так как становилась более текучей. Бронзовые инструменты были тверже медных, хорошо и легко затачивались. Металлургия бронзы позволила в несколько раз повысить производительность труда во всех отраслях человеческой деятельности (рисунок 7).
Само производство инструментов намного упростилось: вместо того, чтобы долгим и упорным трудом оббивать и шлифовать камень, люди наполняли готовые формы жидким металлом и получали результаты, которые и во сне не снились их предшественникам. Техника литья постепенно совершенствовалась. Сначала отливку производили в открытых глиняных или песчаных формах, представлявших собой просто углубление. Их сменили открытые формы, вырезанные из камня, которые можно было использовать многократно. Однако большим недостатком открытых форм было то, что в них получались только плоские изделия. Для отливки изделий сложной формы они не годились. Выход был найден, когда изобрели закрытые разъемные формы. Перед литьем две половинки формы крепко соединялись между собой. Затем через отверстие заливалась расплавленная бронза. Когда металл остывал и затвердевал, форму разбирали и получали готовое изделие.

Рисунок 7 – Бронзовые инструменты
Такой способ позволял отливать изделия сложной формы, но он не годился для фигурного литья. Но и это затруднение было преодолено, когда изобрели закрытую форму. При этом способе литья сначала лепилась из воска точная модель будущего изделия. Затем ее обмазывали глиной и обжигали в печи.
Воск плавился и испарялся, а глина принимала точный слепок модели. В образовавшуюся таким образом пустоту заливали бронзу. Когда она остывала, форму разбивали. Благодаря всем этим операциям мастера получили возможность отливать даже пустотелые предметы очень сложной формы. Постепенно были открыты новые технические приемы работы с металлами, такие как волочение, клепка, пайка и сварка, дополнявшие уже известные ковку и литье (рисунок 8).

Рисунок 8 – Золотая шляпа кельтского жреца
Пожалуй, самую крупную отливку из металла удалось сделать японским мастерам. Было это 1200 лет назад. Весит она 437 т и представляет собой Будду в позе умиротворения. Высота скульптуры вместе с пьедесталом — 22 м. Длина одной руки — 5м. На раскрытой ладони могли бы свободно танцевать четыре человека. Добавим, что знаменитая древнегреческая статуя — Колосс Родосский — высотой 36 м весила 12 т. Отлита она была в III в. до н. э.
С развитием металлургии бронзовые изделия, повсюду стала вытеснять каменные. Но не нужно думать, что это произошло очень быстро. Руды цветных металлов имелись далеко не везде. Причем олово встречалось гораздо реже, чем медь. Металлы приходилось транспортировать на далекие расстояния. Стоимость металлических инструментов оставалась высокой. Все это мешало их широкому распространению. Бронза не могла до конца заменить каменные инструменты. Это оказалось под силу только железу.
Кроме меди и бронзы широко использовались и другие металлы.
Древнейшими изделиями из свинца считаются найденные в Малой Азии при раскопках Чатал-Хююка бусы и подвески и обнаруженные в Ярым-Тепе (Северная Месопотамия) печати и фигурки. Эти находки датируются VI тыс. до н. К тому же времени относятся и первые железные раритеты, представляющие собой небольшие крицы, найденные в Чатал-Хююке. Старейшие серебряные изделия обнаружены на территории Ирана и Анатолии. В Иране их нашли в местечке Тепе-Сиалк: это пуговицы, датируемые началом V тыс. до н. В Анатолии, в Бейджесултане, найдено серебряное кольцо, датируемое концом того же тысячелетия.
В доисторические времена золото получали из россыпей путем промывки. Оно выходило в виде песка и самородков. Затем начали применять рафинирование золота (удаление примесей, отделение серебра), во второй половине 2-го тысячелетия до н.э. В 13-14 веках научились применять азотную кислоту для разделения золота и серебра. А в 19 веке был развит процесс амальгамации (хоть он и был известен в древности, но нет доказательств, что его использовали для добычи золота из песков и руд).
Серебро добывали из галенита, вместе со свинцом. Затем, через столетия, их начали выплавлять совместно (примерно к 3-му тысячелетию до н.э. в Малой Азии), а широкое распространение это получило еще спустя 1500-2000 лет.
Около 640 г. до н. э. начали чеканить монеты в Малой Азии, а около 575 г. до н. э. — в Афинах. По сути дела, это начало штамповочного производства.
Олово когда-то давно выплавляли в простых шахтных печах, после чего делалась его очистка специальными окислительными процессами. Сейчас в металлургии олово получают путем переработки руд по сложным комплексным схемам.
Ну, а ртуть производили путем обжига руды в кучах, при котором она конденсировалась на холодных предметах. Затем уже появились керамические сосуды (реторты), на смену которым пришли железные. А с ростом спроса на ртуть ее стали получать в специальных печах.
Железо было известно в Китае уже в 2357 г. до н. э., а в Египте — в 2800 г. до н. э., хотя еще в 1600 г. до н. э. на железо смотрели как на диковинку. “Железный век” в Европе начался приблизительно за 1000 лет до н. э., когда в государства Средиземноморья проникло от скифов Причерноморья искусство выплавки железа.
Использование железа началось намного раньше, чем его производство. Иногда находили куски серовато-черного металла, который, перекованный в кинжал или наконечник копья, давал оружие более прочное и пластичное, чем бронза, и дольше держал острое лезвие. Затруднение состояло в том, что этот металл находили только случайно. Теперь мы можем сказать, что это было метеоритное железо. Поскольку железные метеориты представляют собой железоникелевый сплав, можно предположить, что качество отдельных уникальных кинжалов, например, могло соперничать с современным ширпотребом. Однако, та же уникальность, приводила к тому, что такое оружие оказывалось не на поле боя, а в сокровищнице очередного правителя.
Железные орудия решительно расширили практические возможности человека. Стало возможным, например, строить рубленные из брёвен дома — ведь железный топор валил дерево уже не в три, как медный, а в 10 раз быстрее, чем каменный. Широкое распространение получило и строительство из тесаного камня. Он, естественно, употреблялся и в эпоху бронзы, но большой расход сравнительно мягкого и дорогого металла решительно ограничивал такие эксперименты. Значительно расширились также и возможности земледельцев.
Впервые железо научились обрабатывать народы Анатолии. Древнегреческая традиция считала открывателем железа народ халибов, для которых в литературе использовалось устойчивое выражение «отец железа», и само название народа происходит именно от греческого слова Χ?λυβας («железо»).
«Железная революция» началась на рубеже I тысячелетия до н. э. в Ассирии. С VIII века до н. э сварное железо быстро стало распространяться в Европе, в III веке до н. э. вытеснило бронзу в Галлии, во II веке новой эры появилось в Германии, а в VI веке нашей эры уже широко употреблялось в Скандинавии и в племенах, проживающих на территории будущей Руси. В Японии железный век наступил только в VIII веке нашей эры.
Вначале получали только маленькие партии железа, и в течение нескольких столетий оно стоило порой в сорок раз дороже серебра. Торговля железом восстановила процветание Ассирии. Открылся путь для новых завоеваний (рисунок 9).

Рисунок 9 - Печь для выплавки железа у древних персов
Увидеть же железо жидким металлурги смогли только в XIX веке, однако, ещё на заре железной металлургии — в начале I тысячелетия до новой эры — индийские мастера сумели решить проблему получения упругой стали без расплавления железа. Такую сталь называли булатом, но из-за сложности изготовления и отсутствия необходимых материалов в большей части мира эта сталь так и осталась индийским секретом на долгое время.
Более технологичный путь получения упругой стали, при котором не требовались ни особо чистая руда, ни графит, ни специальные печи, был найден в Китае во II веке нашей эры. Сталь перековывали очень много раз, при каждой ковке складывая заготовку вдвое, в результате чего получался отличный оружейный материал, называемый дамаском, из которого, в частности, делались знаменитые японские катаны.
§ 7. Век медный, бронзовый, железный
С глубокой древности человеку были известны семь металлов: золото, серебро, медь, олово, свинец, железо и ртуть. Эти металлы можно назвать «доисторическими», так как они применялись человеком ещё до изобретения письменности.
Очевидно, что из семи металлов человек вначале познакомился с теми, которые в природе встречаются в самородном виде. Это золото, серебро и медь. Остальные четыре металла вошли в жизнь человека после того, как он научился получать их из руд с помощью огня.
Часы истории человечества стали отсчитывать время быстрее, когда в его жизнь вошли металлы и, что важнее всего, их сплавы. Век каменный сменился веком медным, потом — бронзовым, а затем веком железным:

История цивилизаций Древнего Египта, Древней Греции, Вавилона и других государств неразрывно связана с историей металлов и их сплавов. Установлено, что египтяне за несколько тысячелетий до нашей эры уже умели изготавливать изделия из золота, серебра, олова, меди. В египетских гробницах, сооружённых за 1500 лет до н. э., найдена ртуть, а самые древние предметы из железа имеют возраст 3500 лет.
Из серебра, золота и меди чеканили монеты — человечество издавна отвело этим металлам роль мерила стоимости товара, мировых денег (рис. 18).

Рис. 18.
Древние монеты из золота, серебра и меди:
1 — золотая с изображением Александра Македонского и орла (символа власти императора) (Греция);
2 — серебряная с изображением богини Афины и совы (птицы, посвящённой Афине) (Греция);
3 — медная в виде дельфина (Причерноморье)
Древние римляне начали чеканить серебряные монеты в 269 г. до н. э. — на полстолетия раньше, чем золотые. Родиной золотых монет стала Лидия, расположенная в западной части Малой Азии и торговавшая с Грецией и другими странами посредством таких монет.
Рассмотрим кратко смену эпох в ранней истории человечества.
В поэме древнегреческого поэта Лукреция Кара «О природе вещей» установлен следующий порядок вхождения металлов в быт человека: «. Всё-таки в употребление вошла раньше медь, чем железо, так как была она мягче, причём изобильней гораздо. »
Самородная медь нередко встречается в природе, она легко обрабатывается, поэтому предметы из меди пришли на смену каменным орудиям. И даже там, где ещё господствовал камень, медь играла немалую роль. Например, одно из чудес света — пирамида Хеопса, сложенная из 2 миллионов 300 тысяч каменных глыб массой по 2,5 т каждая, была сооружена с помощью инструмента, изготовленного из камня и меди.
При выплавке меди человек однажды использовал не чистую медную руду, а руду, содержавшую одновременно и медь, и олово. В результате была получена бронза — сплав двух металлов: меди и олова, который гораздо твёрже своих компонентов. Наступил бронзовый век.
Слово «бронза» произошло от названия небольшого итальянского городка Бриндизи на берегу Адриатического моря, который славился своими бронзовыми изделиями.
В Египте уже в IV тысячелетии до н. э. умели примитивным способом получать бронзу. Из неё изготавливали оружие и различные декоративные изделия. У египтян, ассирийцев, финикийцев, этрусков литьё из бронзы достигло значительного развития. В VII в. до н. э., когда были разработаны способы отливки статуй из бронзы, наступает расцвет художественного применения бронзы.
Гигантская бронзовая статуя Колосса Родосского (32 м) — ещё одно чудо света — возвышалась над входом во внутреннюю гавань древнего порта Родоса. Даже самые крупные морские суда свободно проходили под ней (рис. 19).

Рис. 19.
Колосс Родосский (бронза)
Позже были созданы уникальные бронзовые творения: конная статуя Марка Аврелия, «Дискобол», «Спящий Сатир» и др. А великолепные бронзовые скульптуры «Медный всадник» и четыре скульптурные группы «Укрощение коня» на Аничковом мосту в Санкт-Петербурге — красноречивое свидетельство того, что бронза продолжает оставаться одним из основных материалов скульпторов.

Рис. 20.
Царь-колокол (бронза)
Знаменитые Царь-колокол и Царь-пушка в Московском Кремле — ещё два примера художественной ценности меди и её важнейшего сплава — бронзы (рис. 20 и 21).

Рис. 21.
Царь-пушка (бронза)
Бронзовый век сменился железным только после того, как человечество смогло поднять температуру пламени в металлургических печах до 1540 °С, т. е. до температуры плавления железа. Однако первые изделия из железа имели низкую механическую прочность. И только когда древние металлурги открыли способ изготовления из железных руд сплавов — чугуна и стали — более прочных, чем само железо, материалов, началось широкое распространение этого металла и его сплавов, стимулировавшее развитие человеческой цивилизации.
Наступил железный век, который, очевидно, длится и по сей день, так как примерно 9/10 всех используемых человеком металлов и сплавов — это сплавы на основе железа.
Изменилась и стоимость железа. В IX—VII вв. до н. э., когда начался железный век, этот металл ценился дороже золота. Именно с железом, а не с золотом сравнивали сердца выдающихся людей. Так, герои «Илиады» Гомера облачались в «меднокованые доспехи» и имели «сердца твёрдые, как железо», а героев его «Одиссеи», победителей игр, награждали куском золота и куском железа.
С развитием металлургии стоимость железа снижалась, но всё более возрастала его роль в жизни человеческого общества. Железные сплавы — чугун и сталь — не только основа развития техники, но и важнейший материал искусства. Так, из чугуна отлит узор «кружев чугунных» Санкт-Петербурга, ограды его мостов и решётка Летнего сада (рис. 22). Великолепные произведения искусства из чугуна созданы мастерами Каслинского чугунолитейного завода. Вспомните хотя бы замечательную «Чугунную бабушку» П. Бажова.

Рис. 22.
Решётка ограды Летнего сада
Знаменитый булат, из которого оружейники Дамаска, а затем и нашего Златоуста делали лучшие в мире клинки, — это сталь. Из стали тульские оружейники создавали непревзойдённое по качествам оружие.
Из стали сделаны барельефы, светильники и опоры метро, а также скульптуры, например «Рабочий и колхозница» скульптора В. И. Мухиной (рис. 23).

Рис. 23.
Скульптура «Рабочий и колхозница» (нержавеющая хромоникелевая сталь)
Семь металлов в древности соотносили с семью известными тогда планетами (табл. 3). Даже открытые в XIX в. палладий и церий были названы в честь небесных тел — астероидов Паллада и Церера.
Таблица 3
Металлы и небесные тела

Сейчас у металлов имеются очень серьёзные «конкуренты» в виде продуктов современной химии — пластмасс, синтетических волокон, керамики и стекла. Но ещё многие и многие годы человечество будет использовать металлы, которые продолжают играть ведущую роль в жизни человека.
Семь доисторических металлов

Цитата по теме исследований
Периодический закон и Периодическая система химических элементов Д. И. Менделеева - основа современной химии. Они относятся к таким научным закономерностям, которые отражают явления, реально существующие в природе, и поэтому никогда не потеряют своего значения.
Их открытие было подготовлено всем ходом истории развития химии, однако потребовалась гениальность Д. И. Менделеева, его дар научного предвидения, чтобы эти закономерности были сформулированы и графически представлены в виде таблицы.

Олимпиодр (VI в.), греческий философ и астролог, профессор Александрийской школы. Он соотнес 7 планет древности с 7 металлами и ввел обозначение этих металлов символами планет (Золото—Солнце, Серебро—Луна, Ртуть—Меркурий, Медь—Венера, Железо—Марс, Олово—Юпитер, Свинец-Сатурн).
Термин "металл" произошёл от греческого слова metallon (от metalleuo - выкапываю, добываю из земли). По алхимическим представлениям, металлы зарождались в земных недрах под влиянием лучей планет и постепенно крайне медленно совершенствовались, превращаясь в серебро и золото. Алхимики полагали, что металлы - вещества сложные, состоящие из "начала металличности" (ртути) и "начала горючести" (серы).
Введение

Золото (лат.Aurum)
Золото-элемент редкий, его содержание в земной коре составляет всего 4,310-7%. В природе золото встречается почти всегда в чистом виде: в самородках или в виде мелких зерен и чешуек, вкрапленных в твердые породы или рассредоточенных в золото-носных песках. В наши дни основным источником золота служат руды, в которых на тонну пустой породы приходятся считанные граммы драгоценного металла.
Золото добывают и попутно- при переработке полиметаллических и медных руд. Есть оно и в морской воде – в крайне малых концентрациях.
В представлении алхимиков золото считалось «царем металлов». Причиной тому, очевидно, его эффектный внешний вид, неизменный блеск и устойчивость к действию подавляющего большинства реагентов. Золото при нагревании не реагирует с кислородом, водородом, углеродом, азотом, щелочами и большинством кислот. Растворяется золото лишь в хлорной воде, смеси соляной и азотной кислот (царской водке), в растворах цианидов щелочных металлов, продуваемых воздухом, а также в ртути.
В ювелирных и технических изделиях применяют не чистое золото, а его сплавы, чаще всего с медью и серебром, а его сплавы, чаще всего с медью и серебром. Чистое золото – металл слишком мягкий, ноготь оставляет на нем след, износостойкость его невысока. Проба, стоящая на золотых изделиях отечественного производства, означает содержание золота в сплаве из расчета на тысячу его весовых частей.
Золотой самородок «Мефистофель» массой 20,25 г, найденный в Сибири. Алмазный фонд. Москва.

Серебро (лат. Argentum)
Серебро – драгоценный металл, известный с глубокой древности. Серебренные самородки люди находили еще до того, как научились выплавлять металлы из руд. Серебро встречается на нашей планете и почти чистым, самородным, и в виде соединений (например, Ag2S, Ag3SbS3 и др.) На Земле этого элемента в 20 раз больше, чем золота,- примерно 7×10-6% от массы земной коры, но значительно меньше, чем меди.
Чистое серебро – блестящий белый металл, очень мягкий, по ковкости уступает лишь золоту. Лучше всех металлов проводит тепло и электрический ток.
Как и другим благородным металлам, серебру свойственна высокая химическая стойкость. Серебро не вытесняет водород из растворов обычных кислот, не изменяется на чистом и сухом воздухе, но, если в воздухе содержатся сероводород и другие летучие соединения серы, серебро темнеет. Азотная и концентрированная серная кислоты медленно реагируют с серебром, растворяя его.
Бромид серебра (в меньшей степени и другие галогениды) чрезвычайно важен для фото- и кинопромышленности как важнейший компонент светочувствительной пленки.
Поскольку мировые запасы этого металла уменьшаются, серебро стараются заменить везде, где только можно. Для этого химики-технологи ищут рецептуры бессеребренных светочувствительных кинофотоматериалов. Из похожих на серебро сплавов на никелевой основе делают монеты, посуду и художественные изделия.

Медь (лат. Cuprum)
Медь входит более чем в 170 минералов, из которых для промышленности важны лишь 17. Иногда встречается и самородная медь. Содержание меди в земной коре 4,7×10-3% по массе.
Каменные глыбы пирамиды Хеопса были обработаны медным инструментом. Целый период истории человечества назван медным веком.
Чистая медь – тягучий, вязкий металл красного, в изломе розового цвета, в очень тонких слоях на просвет медь выглядит зеленовато-голубой. В соединениях медь обычно проявляет степень окисления +1 и +2, известны также немногочисленные соединения трехвалентной меди.
Медь-металл сравнительно мало активный. В сухом воздухе и кислороде при нормальных условиях медь не окисляется. Она достаточно легко вступает в реакции с галогенами, серой, селеном. А вот с водородом, углеродом и азотом медь не взаимодействует даже при высоких температурах.
Особенно важна медь для электротехники. По электропроводности медь занимает II место среди всех металлов - после серебра. Однако в наши дни во всем мире электрические провода, на которые раньше уходила почти половина выплавляемой меди, все чаще делают из алюминия. Он хуже проводит ток, но легче и доступнее.
Чаще всего медь вносят в почву в виде пятиводного сульфата – медного купороса. В значительных количествах он ядовит. В малых дозах медь совершенно необходима всему живому.
Медная сковорода, ок.3000г до н.э.
«Медный всадник». Санкт-Петербург.

Железо (лат.Ferrum)
Железо можно назвать главным металлом нашего времени. Это химический элемент очень хорошо изучен. Тем не менее ученые не знают, когда и кем открыто железо: слишком давно это было. Использовать железные изделия человек начал еще в начале I тысячелетия до н.э. На смену бронзовому веку пришел железный. Металлургия железа на территории Европы и Азии начала развиваться еще в IX-VII в.в. до н.э.
Первое железо, попавшее в руки человека, вероятно, неземного происхождения. Ежегодно на Землю падает больше тысячи метеоритов, часть их железные, состоящие в основном из никелистого железа. Самый большой из обнаруженных железных метеоритов весит около 60 т. Он найден в 1920 г. В юго-западной части Африки. У «небесного» железа есть одна важная технологическая особенность: в нагретом виде этот металл не поддается ковке, ковать можно лишь холодное метеоритное железо. Оружие из «небесного» металла долгие века оставалось чрезвычайно редким и драгоценным.
Железо- металл войны, но это и важнейший металл мирной техники. Из железа, как полагают ученые, состоит ядро Земли, и вообще на Земле это один из самых распространенных элементов. На Луне железо найдено в больших количествах в двухвалентном состоянии и самородное. В таком же виде железо существовало и на Земле, пока на ней восстановительная атмосфера не сменилась на окислительную, кислородную. Еще в глубокой древности было открыто замечательное явление – магнитные свойства железа, которые объясняются особенностями строения электронной оболочки атома железа. В древности железо ценилось очень высоко.
Основная масса железа находится в месторождениях, которые можно разрабатывать промышленным способом. По запасам в земной коре железо занимает 4 место среди всех элементов, после кислорода, кремния и алюминия. Намного больше железа в ядре планеты. Но это железо недоступно и вряд ли станет доступным в обозримом будущем. Больше всего железа – 72,4% - в магнетите. Крупнейшие в СССР железорудные месторождения – Курская магнитная аномалия, Криворожское железорудное месторождение, на Урале (горы Магнитная, Высокая, Благодать), в Казахстане – Соколовское и Сарбайское месторождения.
Железо – блестящий серебристо-белый металл, его легко обрабатывать: резать, ковать, прокатывать, штамповать.
Древние предметы из железа,бронзы,
меди датированы 1300г. до н.э.

Ртуть (лат. Hydrargyrum)
В египетских гробницах, сооруженных за 1500 лет до н.э. найдены также изделия из железа, свинца, олова, ртути. Железо в те времена ценилось во много раз дороже золота. В гробнице фараона Тутанхамона (14 век до н.э.) найдено лишь несколько предметов из железа: маленькие лезвия, подголовник, амулет и небольшой кинжал.
Ртуть – элемент редкий и рассеянный, его содержание примерно 4,5×10-6% от массы земной коры. Тем не менее известна ртуть с глубокой древности.
Ртуть – тяжелый (плотность 13,52 г/см3) металл серебристо-белого цвета, единственный металл, жидкий при обычных условиях. Затвердевает ртуть при -38,9°С, закипает – при +357,25°С. При нагревании ртуть довольно сильно (всего в 1,5 раза меньше воды) расширяется, плохо проводит электрический ток и тепло – в 50 раз хуже серебра.
Как и благородные металлы, ртуть на воздухе не изменяется- не окисляется кислородом, не реагирует с другими компонентами атмосферы. С галогенами ртуть реагирует легче, чем с кислородом; взаимодействует с азотной кислотой, а при нагревании и с серной. В соединении ртуть всегда двухвалентна.
Соединения ртути весьма ядовиты. Работа с ними требует не меньшей осторожности, чем работа с самой ртутью.
В промышленности и в технике ртуть используют очень широко и разнообразно. Каждый из нас держал в руках ртутный термометр. Ртуть работает и в других приборах- барометрах, расходомерах. Важны ртутные катоды в производстве хлора и едкого натра, щелочных и щелочноземельных металлов, известны ртутные выпрямители переменного тока, ртутные лампы.

Олово (лат. Stannum)
Колокольчик из бронзы, середина второго тысячелетия до н. э.
Олово – один из металлов, известных людям с древности. Сплав олова с медью – бронза – был впервые получен более 4000 лет назад. Бронза и в наши дни остается главным сплавом олова. Олово – средний по распространенности элемент, в природе он встречается в составе 24 минералов, 2 из них – касситерит и станин – имеют промышленное значение.
Олово – достаточно пластичный серебристо-белый металл, плавится при 231,9°С, кипит при 2270°С. Существует в двух аллотропических модификациях- альфа и бета-олово.
При комнатной температуре олово обычно существует в бета-форме. Это всем известное белое олово – знакомый и привычный металл, из которого раньше отливали оловянных солдатиков, делали посуду и которым до сих пор покрывают изнутри консервные банки. При температуре ниже +13,2°С более устойчиво альфа-олово-серый мелкокристаллический порошок. Процесс превращения белого олова в серое быстрее всего идет при -33°С. Это превращение получило образное название «оловянной чумы». В прошлом оно не раз приводило к драматическим последствиям.
Химическая стойкость олова достаточно высока. При температуре до 100°С оно практически не окисляется кислородом воздуха – лишь поверхность покрывается тонкой оксидной пленкой состава SnO2. Растворяет олово и азотная кислота, даже разбавленная, и на холоде.
Большая часть олова идет на производство припоев и сплавов, главным образом типографских и подшипниковых.

Свинец (лат. Plumbum)
Свинец – это синевато-серый мягкий и тяжелый металл, это цветной металл.
Содержание свинца в земной коре 1,6×10-3% по массе. Самородный свинец встречается крайне редко. Чаще всего свинец встречается в виде в виде сульфида PbS. Этот хрупкий блестящий минерал серого цвета называют галенитом, или свинцовым блеском.
Плавится свинец при температуре 327,4°С, а кипит при 1725°С. Плотность его 11,34 г/см. Свинец – пластичный, мягкий металл: он режется ножом, царапается ногтем.
На воздухе он быстро покрывается тонким слоем оксида PbO. Разбавленные соляная и серная кислоты на свинец почти не действуют, но он растворяется в концентрированных серной и азотной кислотах. С середины XIV в. из свинца отливали пули для огнестрельного оружия, в XV в. Гуттенберг в Германии приготовил знаменитый типографский сплав сурьмы, свинца и олова, или гарт, и положил начало книгопечатанию.
Легкоплавкий, удобный в переработке, свинец широко применяется в наши дни. Свинец хорошо поглощает рентгеновское и радиоактивное излучение
Топор - секира из бронзы, второе тысячелетие до н. э.

Список литературы
Крицман В.А., Станцо В.В. Энциклопедический словарь юного химика 1982г.
Дибров И.А. Неорганическая химия. СПб.: Изд. «Лань», 2001*.
Краткий справочник физико-химических величин / Под ред.К.П.Мищенко А.А. Равделя. Л.: Химия, 1999 *.
Нейгебауэр О. Точные науки в древности. - М.: "Наука", 1968.
Рабочие листы и материалы для учителей и воспитателей
Более 3 000 дидактических материалов для школьного и домашнего обучения
Элективный курс • 9 класс
Предлагаемый элективный курс предназначен для учащихся 9-х классов. Направленность курса общеразвивающая и носит межпредметный характер. Учащиеся получат не только более глубокие знания по теме «Металлы», которые понадобятся при дальнейшем обучении в профильных классах с расширенным или углубленным изучением химии, но и значительно расширят свой кругозор и повысят эрудицию в области культуры и истории развития мировых цивилизаций.
Содержание курса знакомит учащихся с историей алхимии, поисками и разгадками «философского камня», с семью металлами древности: железом, золотом, серебром, медью, свинцом, ртутью и оловом. В курсе достаточно подробно рассматриваются физические и химические свойства этих металлов, их применение и роль в развитии человечества (бронзовый век, железный век и т.д.). При изучении курса внимание школьников акцентируется на связи химии с литературой, историей, географией. Для создания положительной мотивации к обучению приводится обширный историко-искусствоведческий материал (иллюстрации, гравюры, фотографии произведений искусства, изготовленных из металлов и их сплавов).
Цель курса. Интеллектуальная сфера: расширение кругозора, формирование представлений о причинно-следственных связях явлений, о познаваемости мира явлений; формирование на многочисленных исторических фактах понимания единства всех наук, повышение мотивации к изучению предмета.
Эмоционально-волевая сфера: развитие эмоциональной сферы и эстетического чувства на многочисленных примерах историко-искусствоведческого материала курса.
Действенно-практическая сфера: обогащение словарного запаса, развитие эмоций, творческих способностей, развитие умения выделять главное, существенное, сравнивать, обобщать изученные факты.
Задачи курса.
• Показать, что развитие химии происходило во взаимодействии со смежными науками (физикой, минералогией, биологией), а также в связи с практической необходимостью получения веществ с полезными свойствами.
• Ознакомить с основными направлениями развития химии.
• Ознакомить с особенностями свойств изучаемых в курсе металлов, обуславливающих применение их в той или иной области.
• Закрепить приемы безопасной экспериментальной работы в химической лаборатории.
• Способствовать развитию речи и дикции школьников.
• Дать представление об использовании металлов и их сплавов в создании памятников мировой художественной культуры.
• Показать, что полученные знания можно и нужно применять в повседневной жизни.
Предполагаемый результат. В конце изучения данного курса учащиеся должны:
• уметь характеризовать основные направления исторического развития химии как науки;
• знать наиболее важные свойства изученных металлов, уметь приводить примеры применения металлов и их сплавов в технике, безопасного использования в быту;
• проводить качественные реакции по определению ионов металлов в растворах;
• производить расчеты по определению содержания металлов в рудах;
• закрепить навыки экспериментальной работы, правила техники безопасности при работе с химическими веществами;
• приводить примеры исторических памятников, произведений искусства, созданных из металлов.
Каждое занятие включает в себя познавательную часть, практические занятия и материал для закрепления в занимательной игровой форме. Итоговое занятие представляет собой конкурс газет с материалами, найденными учащимися в разных информационных источниках за время изучения курса, и заключительную игру «Брейн-ринг», где участвуют все слушатели курса.
Учебно-тематический план
Лабораторная работа «Изучение перехода олова из одной аллотропной модификации в другую».
Краткое содержание курса
Занятие 1. Введение. Металлы и сплавы, известные в древности и в средние века. Алхимия – прообраз химии (2 ч)
Т е о р и я (1 ч). Век медный, век бронзовый. Использование металлов в древнем мире и в средние века. Алхимия и алхимики. Характеристика уровня химических знаний в период алхимии. Алхимические представления о металлах. «Философский камень», алхимические знаки. Открытия алхимиков.
П р а к т и к а (1 ч). Изучение рисунков-репродукций с изображением древних металлических орудий труда, украшений, предметов обихода и мастерских алхимиков с целью ознакомления с лабораторным оснащением и производимыми химическими операциями. Работа с коллекциями «Металлы и сплавы», «Горные породы и минералы», шкалой твердости.
Лабораторная работа «Изучение некоторых физических свойств сплавов».
Занятие 2. Общие свойства металлов (2 ч)
Т е о р и я (1 ч). Общая характеристика металлов, строение кристаллических решеток, особенности металлической связи. Физические и химические свойства металлов.
П р а к т и к а (1 ч). Изучение кристаллических решеток металлов на моделях. Изучение физических свойств металлов на образцах.
Лабораторная работа «Электрохимический ряд металлов».
Занятие 3. Главный металл современности – железо (2 ч)
Т е о р и я (1 ч). Железо – «небесный металл». Железо в древней мифологии. Самородное железо, железосодержащие минералы. Железный век. История развития металлургии. Краски на основе железа. Железо и здоровье человека.
П р а к т и к а (1 ч). Лабораторная работа «Исследование свойств руд железа (магнитный, бурый, красный железняки)». Качественное определение ионов железа.
Занятие 4. «Царь металлов» – золото (2 ч)
Т е о р и я (1 ч). Золото в природе. Золото – металл ювелиров и банковских кладовых. Особенности физических и химических свойств золота. Черное и разноцветное золото. Древняя профессия золота связана с медициной (имплантанты).
П р а к т и к а (1 ч). Работа с печатными материалами по современному применению золота. Мини-конференция.
Лабораторная работа: 1) приготовление «алхимического золота»; 2) растворение золота в «царской водке».
Занятие 5. Музыкальный металл с острова Кипр – медь (2 ч)
Т е о р и я (1 ч). «Кипрская руда». Особенности свойств меди и ее сплавов. Художественная бронза (Царь-колокол, Царь-пушка, бронзовые памятники). «Певкая медь» – колокольная бронза. Малахит. «Ярь-медянка».
П р а к т и к а (1 ч). Лабораторная работа: 1) закладка опыта по выращиванию кристаллов медного купороса; 2) чернение меди; 3) «медная шуба» – реакция замещения; 4) качественные реакции на ион меди.
Занятие 6. «Хрустальный» металл – свинец (2 ч)
Т е о р и я (1 ч). Применение свинца в древнем мире. Свинцовые водопроводы, возможно, явились причиной гибели Римской империи. Свинец – яд! Свинец – лучший радиопротектор. Почему чернеют со временем шедевры мировой живописи? Свинцовые письма. Хрусталь.
П р а к т и к а (1 ч). Решение задач на получение металлов из руд.
Занятие 7. Металл, болеющий чумой, а также повелитель консервной банки – олово (2 ч)
Т е о р и я (1 ч). Особенности физических и химических свойств. Аллотропные видоизменения. Белое и серое олово. Почему погибла полярная экспедиция Роберта Скотта? Проделки «оловянной чумы». Проблема консервных банок. Оловянная бронза. «Сусальное золото».
П р а к т и к а (1 ч). Лабораторная работа «Изучение перехода олова из одной аллотропной модификации в другую».
Занятие 8. Ртуть – «растворитель» металлов (2 ч)
Т е о р и я (1 ч). Ртуть в природе. Самородная ртуть. Амальгамы металлов. «Гремучая ртуть». Ртуть – яд, она же – лекарство. Почему Иван был Грозным?
П р а к т и к а (1 ч). Работа с информационными источниками, консультации по подбору материала для оформления газет.
Занятие 9. «Доктор» от металлов – серебро (2 ч)
Т е о р и я (1 ч). Серебро в природе, физические и химические свойства. Аргентина и аргентум. Серебро – лучший проводник тепла и электрического тока. «Гремучее серебро». О зеркалах. Фотография началась с серебра. Почему армия Александра Македонского была «вооружена» серебряными ложками и кубками. «Серебряная» вода.
П р а к т и к а (1 ч). Лабораторная работа: 1) проведение реакции «серебряного зеркала»; 2) качественные реакции на ион серебра.
Занятие 10. Подведение итогов (2 ч)
Выставка газет по теме «Многоликие металлы».
Проведение игры «Брейн-ринг» по теме «Металлы».
Методическое обеспечение курса
Формы учебных занятий. Лекция, семинар, мини-конференция, практические занятия – расчетные, экспериментальные, игровые.
Техническое обеспечение.
1. Коллекции «Металлы и сплавы», «Горные породы и минералы», шкала твердости Мооса.
2. Модели кристаллических решеток металлов.
3. Реактивы: металлы (магний, цинк, железо, медь, свинец, олово), кислоты (серная, азотная, соляная, фосфорная), соли (сульфаты, хлориды, нитраты вышеуказанных металлов, нитрат серебра, ацетат свинца, тиоцианат калия).
4. Оборудование: спиртовки, штативы, пробирки, мерная посуда.
5. Иллюстрации, рисунки, репродукции картин, фотографии с изображениями мастерских алхимиков, художественными изделиями из металлов.
Статья подготовлена при поддержке компании «РусМетГрупп». Если Вы решили избавиться от старой чугунной ванны или прочего металлолома, то оптимальным решением станет обратиться в компанию «РусМетГрупп». Перейдя по ссылке: «приём металлолома в Москве», вы сможете, не отходя от экрана монитора, заказать демонтаж и вывоз металлолома по выгодной цене. В компании «РусМетГрупп» работают только высококвалифицированные специалисты с огромным опытом работы демонтажа металлоконструкций.
Л и т е р а т у р а
Малышкина В.А. Занимательная химия. СПб.: Тригон, 2001; Штремплер Г.И. Химия на досуге. М.: Просвещение, 1993; Габриелян О.С., Остроумов И.Г. Настольная книга учителя. Химия. 9 класс. М.: Дрофа, 2002; Книга для чтения по неорганической химии. Сост. В.А.Крицман. М.: Просвещение, 1984; Николаев Л.А. Первые в рядах элементов. М.: Просвещение, 1983; Гофман К. Можно ли сделать золото? Л.: Химия, Ленингр. отд-ние, 1987; Потемкин С.В. 79-й. Благородный. М.: Недра, 1988; Венецкий С.И. В мире металлов. М.: Металлургия, 1988; Хомченко Г.П., Хомченко И.Г. Задачи по химии для поступающих в вузы. М.: Высшая школа, 1995; Габриелян О.С., Воскобойникова Н.П., Яшукова А.В. Настольная книга учителя. М.: Дрофа, 2002.
Читайте также:
