Реакция с металлами находящимися в ряду активности до водорода глюкоза
1. Реакции спиртов с металлами, находящимися в ряду активности до водорода
2. Реакция спирта с оксидом меди ( || )
3. Реакция спирта с гидроксидом меди ( || ) при обычных условиях
4. Реакция спирта с гидроксидом меди ( || ) при нагревании
5. Реакция спирта с гидроксидом натрия
6. Реакция спирта с солями
7. Гидролиз
Запишем кинетическое уравнение для реакции до повышения давления в системе. Обозначим концентрацию HI
C(HI) = a, концентрация йода С(I2) = b
υ = к1 а^2·b
При повышении давления в 5 раз, объём уменьшается в 5 раз, следовательно концентрация газа йода и HI увеличится в 5 раз и кинетическое уравнение примет вид:
υ' = к1 (5а)^2·5b = к1 25а2·5b= к1 125а2·b
Определяем, во сколько раз возрастёт скорость реакции:
υ' /υ = к1 125а2·b / к1 а2·b = 125 раз
Ответ:
Кислород (О) стоит в 1 периоде, VI группе, в главной подгруппе. р-элемент. Электронная конфигурация 1s22s22p4. Число электронов на внешнем уровне – 6. Кислород может принять 2 электрона и в редких случаях отдать. Валентность кислорода 2, степень окисления -2.
Физические свойства: кислород (О2) – бесцветный газ, без запаха и вкуса; в воде малорастворим, немного тяжелее воздуха. При -183 °C и 101,325 Па кислород сжижается, приобретая голубоватый цвет. Строение молекулы: молекула кислорода двухатомна, в обычных условиях прочная, обладает магнитными свойствами. Связь в молекуле ковалентная неполярная. Кислород имеет аллотропную модификацию – озон (О3) – более сильный окислитель, чем кислород.
Химические свойства: до завершения энергетического уровня кислороду нужно 2 электрона, которые он принимает проявляя степень окисления -2, но в соединении со фтором кислород ОF2 -2 и О2F2 -1. Благодаря химической активности кислород взаимодействует почти со всеми простыми веществами. С металлами образует оксиды и пероксиды:
Кислород не реагирует только с платиной. При повышенных и высоких температурах реагирует со многими неметаллами:
Непосредственно кислород не взаимодействует с галогенами. Кислород реагирует со многими сложными веществами:
Кислороду характерны реакции горения:
В кислороде горят многие органические вещества:
При окислении кислородом уксусного альдегида получают уксусную кислоту:
Получение: в лаборатории: 1) электролизом водного раствора щелочи: при этом на катоде выделяется водород, а на аноде – кислород; 2) разложением бертолетовой соли при нагревании: 2КСlО3?2КСl + 3О2?; 3) очень чистый кислород получают: 2КМnO4?К2МnO4 + МnО2 + О2?.
Применение: используется в химической, металлургической промышленности, в медицине.
Реакция спиртов с металлами находящимися в ряду активности до водорода?
Реакция спиртов с металлами находящимися в ряду активности до водорода.

Может не совсем то но все таки
При составлении уравнений реакций не забывать, что водород выделяется в виде двухатомных молекул H2!
Осуществимость — необходимо выполнение двух условий :
1) с кислотами (кроме азотной и концентрированной серной) реагируют только металлы, находящиеся в ряду активностей металлов до водорода (см.
2)при реакции металлов с азотной и концентрированной серной кислотами водород не выделяется, эти кислоты действуют на металлы по своим законам.
Кремниевая кислота вообще не реагирует с металлами, потому что не растворяется в воде.


Помогите Реакции замещение и обмена?
Помогите Реакции замещение и обмена.
Ряд активности металлов, готовлюсь к экзамену!
Идёт ли реакция глюкозы с солями?
Идёт ли реакция глюкозы с солями?
И идет ли реакция глюкозы с металлами, находящимися в ряду активности до водорода?

Металл вытесняет из растворов солей другие (?
Металл вытесняет из растворов солей другие (.
), находящееся в ряду активности металлов (.
)его, а сам может быть вытеснен из растворов солей металлами, расположенными(.

Найдите в ряду активности металлов металл по следующим признакам : а)он не вытесняет водород из растворов кислот ; б)он вытесняет ртуть из растворов ее солей?
Найдите в ряду активности металлов металл по следующим признакам : а)он не вытесняет водород из растворов кислот ; б)он вытесняет ртуть из растворов ее солей.

Алкоголятоми называются продукты взаимодействия : а) спиртов с гологеноводородами б) спиртов с карбоновыми кислотами в)спиртов с активными металлами?
Алкоголятоми называются продукты взаимодействия : а) спиртов с гологеноводородами б) спиртов с карбоновыми кислотами в)спиртов с активными металлами.

Ряд активности металлов?
Ряд активности металлов.
Напишите пожалуйста для этилового спирта(этанола) : 1?
Напишите пожалуйста для этилового спирта(этанола) : 1.
Реакцию горения 2.
Реакцию с активными металлами 3.
Реакцию с металлами, находящимися в ряду активности до водорода 4.
Реакцию с оксидом меди (II) 5.
Реакцию с гидроксидом меди (ll) при обычных условиях 6.
Реакцию с гидроксидом меди (ll) при нагревании 7.
Реакцию с гидроксидом натрия 8.
Реакцию с солями 9.

Каждый металл вытесняет из растворов(?
Каждый металл вытесняет из растворов(.
) металлы, находящиеся в ряду напряжений (.
) его ; в результате реакция должна образоваться (.
) соль для таких реакций не рекомендуется использовать щелочные металлы(.
) так как они взаимодействуют с водой.
При взаимодействии || валентного металла массой 16 г (стоящего в ряду активности до водорода) с соляной кислотой выделилось 8, 96 л водорода?
При взаимодействии || валентного металла массой 16 г (стоящего в ряду активности до водорода) с соляной кислотой выделилось 8, 96 л водорода.

Водород взаимодействует с активными металлами?
Водород взаимодействует с активными металлами.
Нужно написать реакция.
Я про алюминийАлюминий – легкий, прочный и пластичный металл. Это один из самых востребованных металлов, и по темпам роста потребления он давно и с большим отрывом оставил позади сталь, никель, медь и цинк. Алюминий без преувеличений можно назвать ..

Тому що рН показує ступінь концентрації катіонів гідрогену у воді, що є дуже важливим для косметики.
1. дано N(NH3) = 4. 816 * 10 ^ 23 - - - - - - - - - - - - - - - - - - - - - - - - - - - - - V(NH3) - ? N(NH3) / N(A) = V(NH3) / Vm V(NH3) = N(NH3) * Vm / N(A) = 4. 816 * 10 ^ 23 * 22. 4 / 6. 02 * 10 ^ 23 = 15. 58 L ответ 15. 58 л 2) дано m(O2)..

Соотвественно правильным ответом будет являться : 4) KCl ; 5) AgCl ; 6) NH4Cl.
Дано W(O) = 47 % - - - - - - - - - - - - - - - - E - ? Е - это неизвестный элемент W(O) = Ar(O) * n / M(X2O3) * 100% 47% = 16 * 3 / 2x + 48 * 100% 94x + 2256 = 4800 X = 27 - это алюминий Al2O3 ответ алюминий.
Напиши нормально не понятно или сфоткай.
В SO3 32 / (32 + 3 * 16) = 0, 4 или 40 %.
Реакции есть на фотографии.
4HCl + MnO2 = MnCl2 + Cl2 + 2H2O соляная кислота отдаёт в свободном виде половину имеющегося хлора. M(Cl общ. ) = 1000 * 0, 365 * 0, 9726 = 355 г масса выделившегося хлора = 355 / 2 = 177, 5 г.
Типы химической реакции соединение, разложение замещение.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
Да, идёт, меня заставляют писать 20 символов.
Реакция фотосинтеза с образованием глюкозы?
Реакция фотосинтеза с образованием глюкозы.
Помогите?
Надо вставить слова в определение!
- металлы, стоящие в ряду активности до .
, вытесняют его из растворов солей!
Глюкоза окисление и восстановление реакции?
Глюкоза окисление и восстановление реакции.
Напишите пожалуйста уравнение реакции : взаимодействие глюкозы с водородом в присутствии катализатора?
Напишите пожалуйста уравнение реакции : взаимодействие глюкозы с водородом в присутствии катализатора?
На этой странице находится вопрос Идёт ли реакция глюкозы с солями?, относящийся к категории Химия. По уровню сложности данный вопрос соответствует знаниям учащихся 5 - 9 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Химия. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.
Помогите, пожалуйста : Реакция глюкозы с : 1) металлом, находящимся в ряду активности до водорода 2) оксидом меди 2 3) гидроксидом меди 2 при обычных условиях 4) гидроксидом натрия 5) солями?
Помогите, пожалуйста : Реакция глюкозы с : 1) металлом, находящимся в ряду активности до водорода 2) оксидом меди 2 3) гидроксидом меди 2 при обычных условиях 4) гидроксидом натрия 5) солями.
Глюкоза проявляет свойства многоатомного спирта и альдегида = > ; с Na, Cu(OH)2 по гидроксогруппе, а с NaHSO3 - по карбонильной.
2CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHO + 2Na = 2CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(ONa) - CHO + H₂↑ CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHO + CuO ≠ CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHO + Cu(OH)₂ при н.
У. во вложениях CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHO + NaOH ≠ CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHO + NaHSO₃ = CH₂(OH) - CH(OH) - CH(OH) - CH(OH) - CH(OH) - CHOH - (OSO₂Na).

При взаимодействии сульфата меди(2) с гидроксидом натрия получили 49 г гидроксида меди (2) рассчитайте массу гидроксида натрия, необходимую для проведения реакции?
При взаимодействии сульфата меди(2) с гидроксидом натрия получили 49 г гидроксида меди (2) рассчитайте массу гидроксида натрия, необходимую для проведения реакции.
Запишите уравнения химических реакций по следующим схемам : а) фосфорная кислота + гидроксид натрия = фосфат натрия + вода б) оксид натрия + вода = гидроксид натрия в) оксид железа(2) + алюминий = (t)?
Запишите уравнения химических реакций по следующим схемам : а) фосфорная кислота + гидроксид натрия = фосфат натрия + вода б) оксид натрия + вода = гидроксид натрия в) оксид железа(2) + алюминий = (t)оксид алюминия + железо г) гидроксид меди(2) = (t)оксид меди(2) + вода.
Медь - оксид меди - сульфат меди - гидроксид меди - оксид меди?
Медь - оксид меди - сульфат меди - гидроксид меди - оксид меди.
Составте химические уравнения реакций.
Напишите уравнения реакций, с помощью которых можно осуществить цепочку превращений веществ : а) натрий→ гидроксид натрия→ нитрат натрия б) калий→ гидроксид калия→ карбонат калия в) медь→ оксид меди(2?
Напишите уравнения реакций, с помощью которых можно осуществить цепочку превращений веществ : а) натрий→ гидроксид натрия→ нитрат натрия б) калий→ гидроксид калия→ карбонат калия в) медь→ оксид меди(2)→ хлорид меди(2)→ гидроксид меди(2)→ оксид меди(2) г)кальций→ оксид кальция→ гидроксид кальция→ хлорид кальция д) цинк→ оксид цинка→ нитрат цинка→ гидроксид цинка→ сульфат цинка е) барий→ гидроксид бария→ ацетат бария.
В реакцию с раствором гидроксида натрия вступает : 1) оксид меди(II) 2) водород 3) серебро 4) соляная кислота?
В реакцию с раствором гидроксида натрия вступает : 1) оксид меди(II) 2) водород 3) серебро 4) соляная кислота.
Карбонат натрия + гидроксид калия = Сульфат меди (2) + гидроксид натрия = Гидроксид меди (2) =?
Карбонат натрия + гидроксид калия = Сульфат меди (2) + гидроксид натрия = Гидроксид меди (2) =.
Пропанол вступает в реакцию с : оксидом меди 2, гидроксидом меди 2, гидроксидом калия, аммиачным раствором оксида серебра?
Пропанол вступает в реакцию с : оксидом меди 2, гидроксидом меди 2, гидроксидом калия, аммиачным раствором оксида серебра.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : водород→вода→гидроксид натрия→гидроксид меди (II)→оксид меди (II)?
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : водород→вода→гидроксид натрия→гидроксид меди (II)→оксид меди (II).
1. В реакцию с гидроксидом бария вступает магний оксид серы(VI) гидроксид железа(II) нитрат натрия2?
1. В реакцию с гидроксидом бария вступает магний оксид серы(VI) гидроксид железа(II) нитрат натрия
С гидроксидом бария реагирует оксид серы(VI) хлорид калия оксид кальция гидроксид меди(II)
Гидроксид алюминия реагирует с оксидом углерода(II) фосфатом кальция серной кислотой гидроксидом меди(II)
При нагревании разлагается гидроксид калия цезия алюминия натрия
Гидроксид бария вступает в реакцию c хлоридом натрия оксидом бария серной кислотой магнием
С раствором гидроксида бария реагирует каждое из двух веществ : оксид меди(II) и гидроксид натрия оксид углерода(IV) и соляная кислота сероводород и серебро кремниевая кислота и водород
В результате реакции гидроксида железа(III) с соляной кислотой образуются хлорид железа(III) и вода хлорид железа(II) и вода хлорид железа(III) и водород хлорид железа(II), хлор и вода
Химическая реакция возможна между гидроксидом лития и углеродом соляной кислотой оксидом магния серебром
Гидроксид железа(II) реагирует с оксидом натрия сульфатом натрия соляной кислотой гидроксидом магния
Гидроксид натрия реагирует с каждым из двух веществ : гидроксидом алюминия и оксидом углерода(IV) оксидом кальция и сульфатом бария магнием и аммиаком оксидом меди(II) и кремниевой кислотой
Практически осуществима реакция между гидроксидом кальция и оксидом натрия железом водородом oксидом углерода(IV)
Соль и вода образуются в результате взаимодействия гидроксида меди(II) c серой водородом соляной кислотой сульфитом натрия сульфидом натрия
Гидроксид железа(II) реагирует с оксидом углерода(IV) фосфатом кальция гидроксидом меди(II) хлороводородной кислотой
При взаимодействии раствора гидроксида натрия с оксидом фосфора(V) образуются оксид натрия и фосфорная кислота фосфат натрия и вода фосфат натрия и водород оксид фосфора(III), оксид натрия и водород
При взаимодействии хлорида меди(II) c гидроксидом натрия, кроме хлорида натрия, образуются( - ется) оксид меди(II) и водород вода и оксид меди(II) гидроксид меди(II) медь и вода
Реакция с металлами находящимися в ряду активности до водорода глюкоза
Химические свойства глюкозы, как и других альдоз, обусловлены присутствием в ее молекуле: а)альдегидной группы; б) спиртовых гидроксилов; в) полуацетального (гликозидного) гидроксила.
Специфические свойства
1. Брожение (ферментация) моносахаридов
Важнейшим свойством моносахаридов является их ферментативное брожение, т.е. распад молекул на осколки под действием различных ферментов. Брожению подвергаются в основном гексозы в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
1) Спиртовое брожение
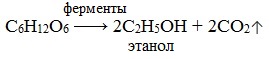
2) Молочнокислое брожение
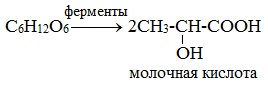
(образуется в организмах высших животных при мышечных сокращениях).
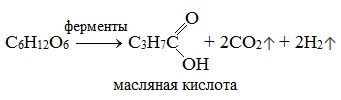
3) Маслянокислое брожение
4) Лимоннокислое брожение
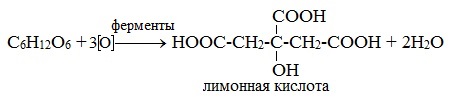
Реакции с участием альдегидной группы глюкозы (свойства глюкозы как альдегида)
1. Восстановление (гидрирование) с образованием многоатомного спирта
В ходе этой реакции карбонильная группа восстанавливается и образуется новая спиртовая группа:
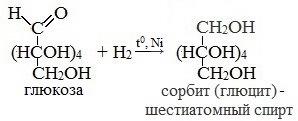
Cорбит содержится во многих ягодах и фруктах, особенно много сорбита в плодах рябины.
2. Окисление
1) Окисление бромной водой
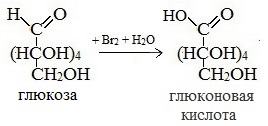
Качественные реакции на глюкозу как альдегид!
Протекающие в щелочной среде при нагревании реакции с аммиачным раствором Ag2O (реакция серебряного зеркала») и с гидроксидом меди (II) Cu (OH)2 приводят к образованию смеси продуктов окисления глюкозы.
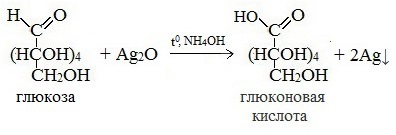
2) Реакция серебряного зеркала
Соль этой кислоты – глюконат кальция – известное лекарственное средство.
Видеоопыт «Качественная реакция глюкозы с аммиачным раствором оксида серебра (I)»
3) Окисление гидроксидом меди (II)
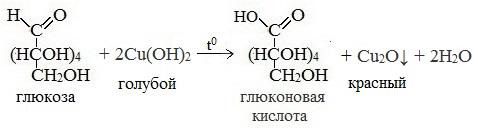
В ходе этих реакций альдегидная группа – СНО окисляется до карбоксильной группы – СООН.
Реакции глюкозы с участием гидроксильных групп (свойства глюкозы как многоатомного спирта)
1. Взаимодействие с Cu (ОН)2 с образованием глюконата меди (II)
Качественная реакция на глюкозу как многоатомный спирт!
Подобно этиленгликолю и глицерину, глюкоза способна растворять гидроксид меди (II), образуя растворимое комплексное соединение синего цвета:
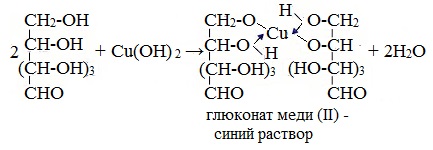
Прильём к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет.
В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт, образуя комплексное соединение.
Видеоопыт «Качественная реакция глюкозы с гидроксидом меди (II)»
2. Взаимодействие с галогеналканами с образованием простых эфиров
Являясь многоатомным спиртом, глюкоза образует простые эфиры:
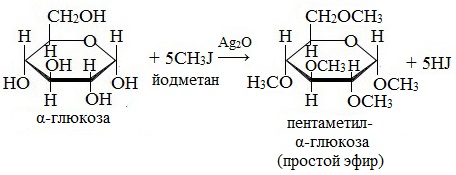
Реакция происходит в присутствии Ag2O для связывания выделяющегося при реакции НI.
3. Взаимодействие с карбоновыми кислотами или их ангидридами с образованием сложных эфиров.
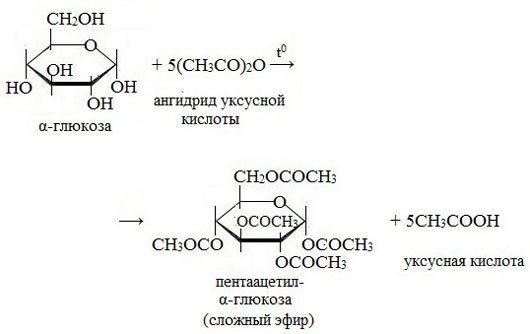
Например, с ангидридом уксусной кислоты:
Реакции с участием полуацетального гидроксила
1. Взаимодействие со спиртами с образованием гликозидов
Гликозиды – это производные углеводов, у которых гликозидный гидроксил замещен на остаток какого-либо органического соединения.
Содержащийся в циклических формах глюкозы полуацетальный (гликозидный) гидроксил является очень реакционноспособным и легко замещается на остатки различных органических соединений.
В случае глюкозы гликозиды называются глюкозидами. Связь между углеводным остатком и остатком другого компонента называется гликозидной.
Гликозиды построены по типу простых эфиров.
При действии метилового спирта в присутствии газообразного хлористого водорода атом водорода гликозидного гидроксила замещается на метильную группу:
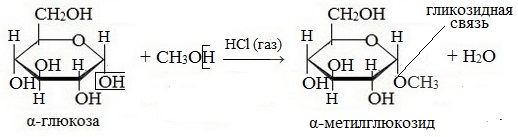
В данных условиях в реакцию вступает только гликозидный гидроксил, спиртовые гидроксильные группы в реакции не участвуют.
Гликозиды играют чрезвычайно важную роль в растительном и животном мире. Существует огромное число природных гликозидов, в молекулах которых с атомом С (1) глюкозы остатки самых различных соединений.
Реакции окисления
Более сильный окислитель – азотная кислота НNO3 – окисляет глюкозу до двухосновной глюкаровой (сахарной) кислоты:
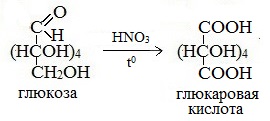
В ходе этой реакции и альдегидная группа – СНО и первичная спиртовая группа — СН2ОН окисляются до карбоксильных – СООН.
Видеоопыт «Окисление глюкозы кислородом воздуха в присутствии метеленового голубого»
Читайте также:
