Реакция с металлами для фосфорной кислоты
В степени окисления +5 фосфор способен образовывать определенные кислоты:
- орто-фосфорную H 3 P O 4 ;
- мета-фосфорную H P O 3 ;
- пиро-фосфорную H 4 P 2 O 7 .
Ортофосфорная кислота (фосфорная кислота) является неорганической трехосновной кислотой средней силы. Чистое вещество представляет собой прозрачные гигроскопические кристаллы.
Химическая формула фосфорной кислоты:
Во многих случаях в химии фосфорной кислотой называют ее водный раствор с концентрацией 85%. Такая жидкость напоминает сироп и не обладает запахом. Соединение характеризуется высокой степенью растворимости в этаноле и других растворителях. Строение фосфорной кислоты выражает структурная формула:
При стандартных условиях, то есть температуре 25 °C и давлении 1 атм, фосфорная кислота характеризуется классом опасности Н 290 , Н 314 .
Фосфорная кислота не обладает специфическим токсическим эффектом. Показатели системной токсичности вещества достаточно невысокие. Раствор фосфорной кислоты оказывает раздражающее воздействие на органы зрения и дыхания, слизистые оболочки. Если концентрация соединения превышает 10%, смесь характеризуется раздражающим эффектом, а при 25% содержания вещества раствор вызывает коррозию.
Диссоциация фосфорной кислоты в водных растворах протекает ступенчато:
H 3 P O 4 ⇄ H + + H 2 P O 4 - ,
H 2 P O 4 - ⇄ H + + H P O 4 2 - ,
H P O 4 2 - ⇄ H + + P O 4 3 - .
С каждой новой ступенью диссоциация ослабевает. Полного распада на ионы у фосфорной кислоты не наблюдается. Вещество характеризуется меньшей активностью в процессе химического взаимодействия, по сравнению с серной, азотной, соляной кислотами.
Химические и физические свойства
Физические свойства фосфорной кислоты:
- твердое агрегатное состояние;
- молярная масса 98 г/моль;
- в чистом виде кристаллическое вещество не имеет окраски;
- температура плавления 42,35 °С;
- температура кипения +158 °C;
- кристаллизуется в моноклинной сингонии.
В твердом состоянии вещество гигроскопично и способно расплываться в воздушной среде. Фосфорная кислота смешивается с водой в любых соотношениях. Наиболее распространены следующие концентрации раствора:
- 75 % H 3 P O 4 (с температурой плавления −20 °С).
- 80 % H 3 P O 4 (с температурой плавления 0 °С).
- 85 % H 3 P O 4 (с температурой плавления 20 °С).
Используя 85% раствор фосфорной кислоты, получают безводную кислоту путем испарения жидкости в вакуумной среде при температурном режиме 80 °С. В концентрированных растворах выпадает осадок в виде гемигидрата H 3 P O 4 · 0 , 5 H 2 O .
Молекулы фосфорной кислоты, находящейся в твердом состоянии или в виде концентрированного раствора, соединены водородными связями.
Фосфорная кислота является трехосновной кислотой средней силы. В водных растворах соединение диссоциирует по трем ступеням c константами диссоциации:
Сопровождается выделением теплоты только диссоциация по первой ступени (экзотермическая). По второй и третьей ступени теплота поглощается, то есть процесс является эндотермическим:
H 3 P O 4 ( a q ) + H 2 O ( l ) ⇌ H 3 O ( a q ) + + H 2 P O 4 ( a q ) -
H 2 P O 4 ( a q ) - + H 2 O ( l ) ⇌ H 3 O ( a q ) + + H P O 4 ( a q ) 2 -
H P O 4 ( a q ) 2 - + H 2 O ( l ) ⇌ H 3 O ( a q ) + + P O 4 ( a q ) 3 -
В результате фосфорная кислота может образовывать как средние соли (фосфаты), так и кислые (гидрофосфаты и дигидрофосфаты).
Соединение проявляет свойства кислоты, не являющейся окислителем, при вступлении в реакции с такими веществами, как:
- соли;
- гидроксиды металлов;
- оксиды;
- металлы.
Нагрев фосфорной кислоты сопровождается отщеплением воды. В результате образуются пирофосфорная кислота и метафосфорная кислота:
2 H 3 P O 4 → H 2 O + H 4 P 2 O 7 ;
H 4 P 2 O 7 → H 2 O + 2 H P O 3 .
Ортофосфорная кислота отличается от других фосфорных кислот взаимодействием с нитратом серебра. В результате этой реакции можно наблюдать выпадение осадка с желтой окраской. Если в реакции участвуют другие фосфорные кислоты, то цвет осадка будет белым:
H 3 P O 4 + 3 A g N O 3 → A g 3 P O 4 + 3 H N O 3 .
Качественная реакция на ион H 2 Р О 4 представляет собой процесс формирования молибденофосфата аммония в виде осадка с ярко-желтой окраской:
H 3 P O 4 + 12 [ N H 4 ] 2 M o O 4 + 21 H N O 3 → [ N H 4 ] 3 P M o 12 O 40 · 6 H 2 O ↓ + 21 N H 4 N O 3 + 6 H 2 O
Основные способы получения
Первым фосфорную кислоту синтезировал Роберт Бойль в 1694 году, используя в реакции оксид фосфора(V).
В лабораторных условиях соединение получают в процессе окисления фосфора с помощью азотной кислоты:
3 P + 5 H N O 3 + 2 H 2 O → 3 H 3 P O 4 + 5 N O .
Основные промышленные методы синтеза фосфорной кислоты:
Технология производства фосфорной кислоты, основанная на термическом методе, предполагает сжигание фосфора до оксида фосфора(V), который затем взаимодействует с водой:
4 P + 5 O 2 → 2 P 2 O 5 ;
P 2 O 5 + 3 H 2 O → 2 H 3 P O 4 .
На практике используют разные способы для реализации данного химического взаимодействия.
IG-процесс (по названию компании IG) предполагает проведение этих реакций в одной реакционной колонне. В нее с помощью сжатого воздуха или пара под давлением 1,5 МПа сквозь сопло перекачивают фосфор, температура сгорания которого составляет больше 2000 °C.
Полученный в результате процесса оксид фосфора(V) поглощается фосфорной кислотой, стекающей с верхней части по стенкам колонны. Таким образом, стенки колонны полностью покрываются кислотой. Вещество выполняет сразу несколько функций:
- растворение оксида фосфора(V);
- отвод тепла от химического процесса сгорания;
- защита конструкции колонны от воздействия огня.
Образованная фосфорная кислота концентрируется в отсеке в нижней части колонны. Соединение транспортируется по теплообменнику, поступает в верхнюю часть колонны и вновь стекает по стенкам.
Оборудование, используемое в химической промышленности для синтеза фосфорной кислоты, изготовлено из нержавеющей низкоуглеродной стали. Этот материал стабилен и не вступает в реакции с концентрированной фосфорной кислотой при температуре, не превышающей 100 °C.
Особенностью синтезированной с помощью данной методики фосфорной кислоты является минимальная концентрация примесей соединений в низших степенях окисления. К примеру, в соединении присутствует фосфористая кислота H 3 P O 3 , доля которой составляет 0,1 %.
Полученную кислоту очищают от примесного мышьяка, для которого характерно присутствие в небольших концентрациях даже в очень чистом фосфоре. Такая очистка производится с помощью воздействия сероводорода (его получают путем добавления сульфида натрия в фосфорную кислоту) и фильтрования после выпадения в осадок сульфида мышьяка.
Данные химические реакции лежат и в основе TVA-процесса (от Tennessee Valley Authority). Отличие от предыдущей технологии заключается в том, что сжигание фосфора и поглощение оксида фосфора(V) реализуются по отдельности.
Фосфор и воздух подают в стальную камеру сгорания, которая дополнена внешним охлаждением. Затем продукты сгорания транспортируют через верхнюю часть камеры в отсек поглощения для дальнейшего образования фосфорной кислоты.
В Хехст-процессе (по названию компании Hoechst) реакции сгорания и поглощения разделены. Отличие данной технологии синтеза фосфорной кислоты от других методов заключается в использовании теплоты, которая выделяется в процессе сгорания фосфора, для генерирования пара.
При реализации экстракционного метода синтеза фосфорной кислоты природные фосфаты обрабатывают с помощью неорганических кислот. В распространенных случаях с этой целью используют хибинский апатитовый концентрат и фосфориты Каратау.
Обработка фосфатов активно применялась в промышленности еще в середине 1880-х годов. Данное направление начало развиваться после Второй мировой войны, что объяснялось высоким спросом на минеральные удобрения в сельском хозяйстве.
Процесс экстракционного получения фосфорной кислоты. Уравнение схемы разложения сырья, где параметр x может быть равен от 0,1 до 2,2:
C a 5 ( P O 4 ) 3 F + 5 H 2 S O 4 + 5 x H 2 O → 5 C a S O 4 · x H 2 O + 3 H 3 P O 4 + H F .
В результате образуется побочный продукт в виде сульфата кальция. Данное вещество при определенной температуре и концентрации фосфорной кислоты способно выпадать в осадок в виде дигидрата ( C a S O 4 · 2 H 2 O ) или гемигидрата ( C a S O 4 · 0 , 5 H 2 O ) . Исходя из этого признака, различают следующие типы экстракционных процессов синтеза фосфорной кислоты:
- дигидратный;
- гемигидратный;
- комбинированный (дигидратно-гемигидратный и гемигидратно-дигидратный).
Существует также ангидритный метод, который предполагает выпадение в осадок безводного сульфата кальция. Технология не применяется в промышленном производстве фосфорной кислоты, что объясняется возникновением серьезных коррозийных проблем.
Классическая технология синтеза фосфорной кислоты — дигидратный процесс. Достоинство данного метода заключается в относительно низкой температуре, что исключает образование коррозии. При реализации технологии допустимо использовать разное фосфатное сырье и осуществлять его переработку в больших объемах.
На первой стадии происходит измельчение сырья до размера частиц меньше 150 мкм. Фосфат и серная кислота поступают в реактор отдельными потоками. Таким образом, сформированный слой сульфата кальция на частицах не препятствует дальнейшему разложению. Температурный режим процесса поддерживается в пределах от 70°С до 80°С. При этом концентрация фосфорной кислоты в системе составляет 28—31 % в пересчете на P 2 O 5 .
Данные условия позволяют получить сульфат кальция в виде дигидрата. Недостатком технологии является необходимость в измельчении начального сырья и дополнительном концентрировании синтезированной фосфорной кислоты до 40–55 % и даже до 70 % P 2 O 5 .
Гемигидратный процесс был разработан с целью исключить необходимость концентрировать образованную фосфорную кислоту. Отличием этого метода синтеза является более высокая температура, которая достигает 80–100 °С. При этом создаются условия для более стабильной формы продукта, образующегося в виде гемигидрата сульфата кальция. Концентрация полученной фосфорной кислоты составляет в результате 40–48 %.
Гемигидратно-дигидратный процесс является разработкой японских ученых. С помощью данной технологи удается получить почти чистый гипс, залежи которого в Японии отсутствуют. Сырье обрабатывают при высокотемпературном воздействии. В результате формируется гемигидрат сульфата кальция, который в дальнейшем перекристаллизовывают в дигидрат.
Процесс концентрирования фосфорной кислоты, которую получают по дигидратной технологии, заключается в вакуумном испарении. На устаревших производствах применяют погружное горение. В некоторых случаях в определенной последовательности применяют несколько испарителей. В результате пары с одного испарителя используются, чтобы нагревать раствор в следующем испарителе.
В процессе испарения воды из фосфорной кислоты также удаляется фтор в виде смеси S i F 4 и H F . Таким образом, когда концентрация фосфорной кислоты увеличивается с 30 до 50 % P 2 O 5 , из нее удаляется 50–60 % фтора. Так как выбросы фтора загрязняют окружающую среду, выделяемые вещества сразу используют в производстве кремнефтористоводородной кислоты H 2 S i F 6 .
Способы удаления разных неорганических примесей:
В осадке остаются примеси мышьяка (в виде сульфида мышьяка), кадмия (в виде комплекса с эфирами дитиофосфорной кислоты) и некоторые другие металлы.
Процесс экстракции основан на переходе фосфорной кислоты в органическую фазу. Далее вещество промывают водой. В результате происходит удаление катионных и анионных примесей. Отделение фосфорной кислоты от растворителя достигается перегонкой.
Спрос в мире на фосфорную кислоту на 1989 г. составил 40,6 млн тонн в год в пересчете на P 2 O 5 . Экстракционный метод синтеза наиболее распространен в промышленности (95 % от общего количества). Это объясняется экономичным потреблением энергетических ресурсов. Остальные 5 % объема фосфорной кислоты получают термическим способом.
Основным поставщиком (и потребителем) экстракционной фосфорной кислоты являются США. В данном случае доля от общего объема производства соединения равна 90 %. В 1980-е годы отмечено снижение запасов производимой фосфорной кислоты в результате отказа от фосфорсодержащих детергентов и минеральных удобрений. Данное решение объясняется загрязнением фосфатными удобрениями грунтовых вод и эвтрофикацией водоемов.
Экстракционная технология синтеза фосфорной кислоты предполагает формирование отвалов сульфата кальция: на 1000 килограмм P 2 O 5 получают 4,5—5,5 тонны загрязненного сульфата кальция, который нуждается в утилизации. По состоянию на 2008 год существовало несколько способов:
- затопление в водоемах (10 %);
- сваливание на суше (около 88 %);
- применение в качестве сырья.
В процессе погружения в водоемы растворение сульфата кальция протекает активно. Показатели растворимости вещества в морской воде составляют 3,5 г/л, а природное содержание равно 1,6 г/л. Примеси оксида кремния и оксида алюминия не растворяются.
Где используется, области применения
Фосфорную кислоту используют в качестве флюса в процессе пайки (по окисленной меди, по черному металлу, по нержавеющей стали).
Соединение применяют для проведения научных экспериментов в лабораторной практике.
С помощью вещества удаляют ржавчину с металлических поверхностей. В результате такой обработки образуется защитная пленка, которая служит барьером для коррозионных процессов.
Фосфорную кислоту используют в составе фреонов, в промышленных морозильных установках в качестве сильного связующего компонента.
В авиации ортофосфорная кислота входит в состав гидрожидкости НГЖ-5У и ее иностранных аналогов.
В пищевой промышленности вещество используют, как пищевую добавку E 338 . Ортофосфорная кислота регулирует уровень кислотности в газированных напитках таких, как Кока-Кола. На вкус слабый водный раствор ортофосфорной кислоты с небольшим содержанием сахара похож на крыжовник.
В области звероводства, в частности, на фермах, где разводят норок, путем подкормки раствором ортофосфорной кислоты предотвращают повышение кислотности в желудке и развитие мочекаменной болезни.
Вещество при использовании в гидропонных системах позволяет контролировать уровень pH питательного раствора.
Ортофосфорная кислота нашла широкое применение в стоматологии. С помощью этого вещества протравливают эмаль и дентин, то есть снимают смазанный слой, перед наложением пломбы на зубы.
Фосфорная кислота
Фосфор в степени окисления +5 образует несколько кислот: орто-фосфорную H3PO4, мета-фосфорную HPO3, пиро-фосфорную H4P2O7.
Фосфорная кислота H3PO4 – это кислота средней силы, трехосновная, прочная и нелетучая. При обычных условиях фосфорная кислота – твердое вещество, хорошо растворимое в воде и гигроскопичное.

Валентность фосфора в фосфорной кислоте равна V.
При температуре выше +213 °C орто-фосфорная кислота переходит в пирофосфорную H4P2O7.

При взаимодействии высшего оксида фосфора с водой на холоде образуется метафосфорная кислота HPO3, представляющая собой прозрачную стекловидную массу.

Способы получения
Наибольшее практическое значение из фосфорных кислот имеет ортофосфорная кислота.
1. Получить орто-фосфорную кислоту можно взаимодействием оксида фосфора (V) с водой:
2. Еще один способ получения фосфорной кислоты — вытеснение фосфорной кислоты из солей (фосфатов, гидрофосфатов и дигидрофосфатов) под действием более сильных кислот (серной, азотной, соляной и др.) .
Промышленный способ получения фосфорной кислоты обработка фосфорита концентрированной серной кислотой:
3. Фосфорную кислоту также можно получить жестким окислением соединений фосфора в водном растворе в присутствии кислот.
Например , концентрированная азотная кислота окисляет фосфор до фосфорной кислоты:
Химические свойства
Фосфорная кислота – это кислота средней силы (по второй и третьей ступени слабая) .
1. Фосфорная кислота частично и ступенчато диссоциирует в водном растворе.
HPO4 2– ⇄ H + + PO4 3–
2. Фосфорная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , фосфорная кислота взаимодействует с оксидом магния:
Еще пример : при взаимодействии фосфорной кислоты с гидроксидом калия образуются фосфаты, гидрофосфаты или дигидрофосфаты:
3. Фосфорная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов и др.). Также фосфорная кислота вступает в обменные реакции с солями.
Например , фосфорная кислота взаимодействует с гидрокарбонатом натрия:
4. При нагревании H3PO4 до 200°С происходит отщепление от нее молекулы воды с образованием пирофосфорной кислоты H2P2O7:
5. Фосфорная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Например , фосфорная кислота реагирует с магнием:
Фосфорная кислота взаимодействует также с аммиаком с образованием солей аммония:
7. Качественная реакция на фосфат-ионы и фосфорную кислоту — взаимодействие с нитратом серебра. При этом образуется ярко-желтый осадок фосфата серебра:

Видеоопыт взаимодействия фосфата натрия и нитрата серебра в растворе (качественная реакция на фосфат-ион) можно посмотреть здесь.
Фосфор. Химия фосфора и его соединений

Фосфор расположен в главной подгруппе V группы (или в 15 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение фосфора
Электронная конфигурация фосфора в основном состоянии :

Атом фосфора содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом фосфора может образовывать 3 связи по обменному механизму. Однако, в отличие от азота, за счет вакантной 3d орбитали атом фосфора может переходить в возбужденное энергетическое состояние.
Электронная конфигурация фосфора в возбужденном состоянии:

При этом один электрон из неподеленной электронной пары на 3s-орбитали переходит на переходит на 3d-орбиталь. Для атома фосфора в возбужденном энергетическом состоянии характерна валентность V.
Таким образом, максимальная валентность фосфора в соединениях равна V (в отличие от азота). Также характерная валентность фосфора в соединениях — III.
Степени окисления атома фосфора – от -3 до +5. Характерные степени окисления -3, 0, +1, +3, +5.
Физические свойства и нахождение в природе
Фосфор образует различные простые вещества (аллотропные модификации).
Белый фосфор — это вещество состава P4. Мягкий, бесцветный, ядовитый, имеет характерный чесночный запах. Молекулярная кристаллическая решетка, а следовательно, невысокая температура плавления (44°С), высокая летучесть. Очень реакционно способен, самовоспламеняется на воздухе.


Покрытие бумаги раствором белого фосфора в сероуглероде. Спустя некоторое время, когда сероуглерод испаряется, фосфор воспламеняет бумагу (процесс лег в основу различных фокусов с самовозгоранием или получением огня из ничего):
Белый фосфор можно расплавить в ёмкости с тёплой водой, поскольку он имеет температуру плавления в 44,15 °C.
Красный фосфор – это модификация с атомной кристаллической решеткой . Формула красного фосфора Pn, это полимер со сложной структурой. Твердое вещество без запаха, красно-бурого цвета, не ядовитое. Это гораздо более устойчивая модификация, чем белый фосфор. В темноте не светится. Образуется из белого фосфора при t=250-300 о С без доступа воздуха.


Черный фосфор – то наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Чёрный фосфор — это чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, полностью нерастворимое в воде или органических растворителях.

Известны также такие модификации, как желтый фосфор и металлический фосфор. Желтый фосфор – это неочищенный белый фосфор. При очень высоком давлении фосфор переходит в новую модификацию – металлический фосфор , который очень хорошо проводит электрический ток.

В природе фосфор встречается только в виде соединений. В основном это апатиты (например, Ca3(PO4)2), фосфориты и др. Фосфор входит в состав важнейших биологических соединений —фосфолипидов.
Азотная кислота
Азотная кислота является одной из самых сильных минеральных кислот, в концентрированном виде выделяет пары желтого цвета с резким запахом. За исключением золота и платины растворяет все металлы.
Применяют азотную кислоту для получения красителей, удобрений, органических нитропродуктов, серной и фосфорной кислот. В результате ожога азотной кислотой образуется сухой струп желто-зеленого цвета.

В промышленности азотную кислоту получают в результате окисления аммиака на платино-родиевых катализаторах.
Чистая азотная кислота впервые была получена действием на селитру концентрированной серной кислоты:
Является одноосновной сильной кислотой, вступает в реакции с основными оксидами, основаниями. С солями реагирует при условии выпадения осадка, выделения газа или образования слабого электролита.

При нагревании азотная кислота распадается. На свету (hv) также происходит подобная реакция, поэтому азотную кислоту следует хранить в темном месте.
Азотная кислота способна окислить все неметаллы, при этом, если кислота концентрированная, азот обычно восстанавливается до NO2, если разбавленная - до NO.

В любой концентрации азотная кислота проявляет свойства окислителя, при этом азот восстанавливается до степени окисления от +5 до -3. На какой именно степени окисления остановится азот, зависит от активности металла и концентрации азотной кислоты.
Для малоактивных металлов (стоящих в ряду напряжений после водорода) реакция с концентрированной азотной кислотой происходит с образованием нитрата и преимущественно NO2.
С разбавленной азотной кислотой газообразным продуктом преимущественно является NO.
В реакциях с металлами, стоящими левее водорода в ряду напряжений, возможны самые разные газообразные (и не газообразные) продукты: бурый газ NO2, NO, N2O, атмосферный газ N2, NH4NO3.
Помните о закономерности: чем более разбавлена кислота и активен металл, тем сильнее восстанавливается азот. Ниже представлены реакции цинка с азотной кислотой в различных концентрациях.

Посмотрите на таблицу ниже, в которой также отражены изученные нами закономерности.
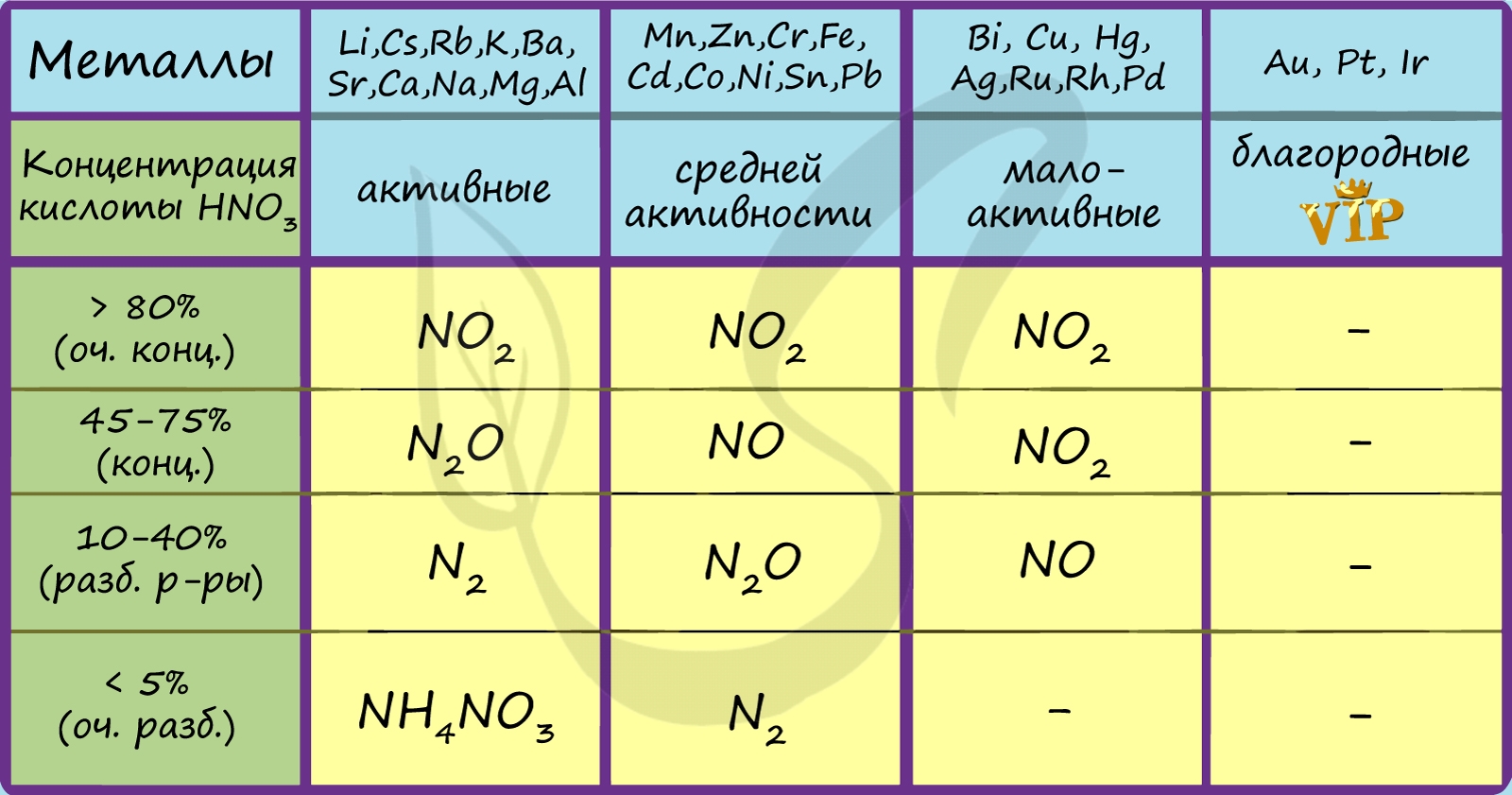
Концентрированная холодная азотная кислота пассивирует хром, железо, алюминий, никель, свинец и бериллий. Это происходит за счет оксидной пленки, которой покрыты данные металлы.
Al + HNO3(конц.) ⇸ (реакция не идет)
При нагревании или амальгамировании (покрытие ртутью) перечисленных металлов реакция с азотной кислотой идет, так как оксидная пленка на поверхности металлов разрушается.
Соли азотной кислоты - нитраты NO3 -
Получают нитраты в ходе реакции азотной кислоты с металлами, их оксидами и основаниями.
В реакциях с оксидами и основаниями газообразный продукт обычно не выделяется.

Нитрат аммония получают реакция аммиака с азотной кислотой.
Обратите внимание на следующую закономерность: концентрированная азотная кислота, как правило, окисляет железо и хром до +3. Разбавленная кислота - до +2.
- Реакции с металлами, основаниями и кислотами
Как и для всех солей, из нитратов можно вытеснить металл другим более активным. Соли реагируют с основаниями и кислотами, если в результате реакции выпадает осадок, выделяется газ или образуется слабый электролит (вода).

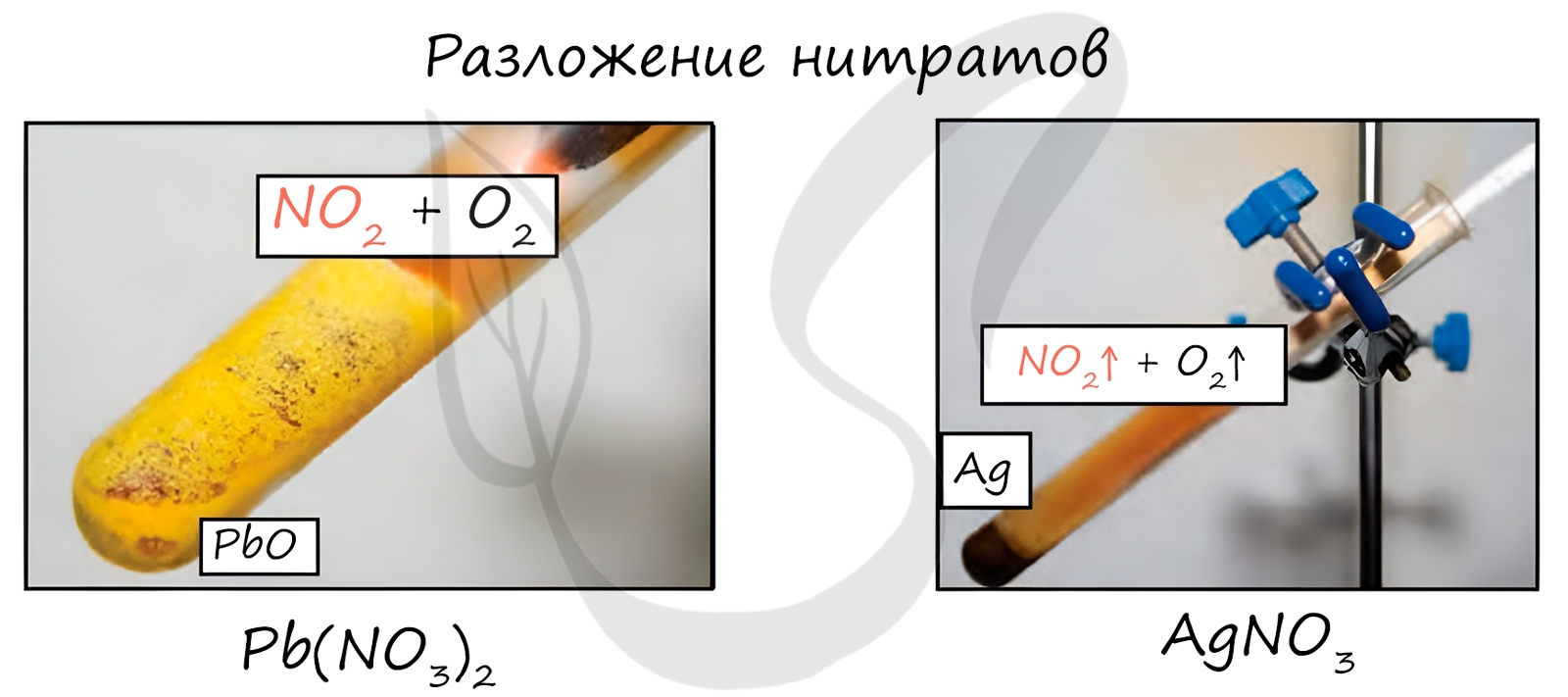
Нитраты разлагаются в зависимости от активности металла, входящего в их состав.

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Блиц-опрос по теме Азотная кислота
Холодная концентрированная азотная кислота не вступает в реакцию с алюминием, происходит пассивирование.
2. Реакция концентрированной азотной кислоты с малоактивными металлами сопровождается выделением газа
В реакциях концентрированной азотной кислоты и малоактивных металлов преимущественно выделяется NO2.
3. Если в результате реакции активного металла с азотной кислотой выделилось твердое вещество, то речь идет о
Твердый продукт, образовавшийся в ходе реакции с азотной кислотой, нитрат аммония - NH4NO3
Разложение нитрата аммония протекает по схеме: AgNO3 → Ag + NO2 + O2
Азотной кислотой окрашивает пораженную в результате ожога кожу в желтый цвет.
Фосфор
Фосфор (греч. phos - свет + phoros - несущий) - химический элемент, принадлежащий к Vа группе и 3 периоду. Простое желтоватое вещество, легко воспламеняющееся и светящееся.

Основное и возбужденное состояние фосфора
При возбуждении атома фосфора электроны на s-подуровне распариваются и переходят на d-подуровень.

Природные соединения
- 3Ca3(PO4)2*CaCO3*Ca(OH,F)2 - фосфорит
- Ca10(PO4)6(F,Cl,OH)2 - апатит

В промышленности фосфор получают в ходе сплавления фосфата кальция, песка и угля.
Химическая активность фосфора значительно выше, чем у азота. Активность также определяется аллотропной модификацией: наиболее активен белый фосфор, излучающий видимый свет из-за окисления кислородом.
В жидком и газообразном состоянии до 800 °C фосфор состоит из молекул P4. Свыше 800 °C молекулы P4 распадаются до P2.
- Реакции с неметаллами
C неметаллами фосфор часто проявляет себя как восстановитель и окислитель. Легко окисляется кислородом.
Схожим образом происходит взаимодействие фосфора и хлора.
2P + 3Cl2 → 2PCl3 (недостаток хлора)
2P + 5Cl2 → 2PCl5 (избыток хлора)
Реакции с водородом крайне затруднена. Тем не менее, в ходе разложения фосфидов металлов можно получить ядовитый газ - фосфин - боевое отравляющее вещество.

2P + 3Ca → Ca3P2 (фосфид кальция)
При взаимодействии с водой фосфор вступает в реакцию диспропорционирования (так называются реакции, в которых одно и то же вещество является и окислителем, и восстановителем).
При добавлении фосфора в растворы щелочей также происходит реакция диспропорционирования.
При поджигании спичек происходит реакция между фосфором и бертолетовой солью, которая выступает в качестве окислителя.

Оксид фосфора V - P2O5
Кислотный оксид, пары которого имеют формулу P4O10. Твердый оксид характеризуется белым цветом.
Активно реагирует с водой с образованием фосфорной кислоты. При недостатке воды образует метафосфорную кислоту.
Реагирует с основными оксидами и основаниями, образуя соли фосфорной кислоты. Какая именно получится соль - определяет соотношение основного оксида/основания и кислотного оксида.
6KOH + P2O5 = 2K3PO4 + 3H2O (фосфат калия, избыток щелочи - соотношение 6:1)
4KOH + P2O5 = 2K2HPO4 + H2O (гидрофосфат калия, незначительный избыток кислотного оксида - соотношение 4:1)
2KOH + P2O5 = 2KH2PO4 + H2O (дигидрофосфат калия, избыток кислотного оксида - соотношение 2:1)

Обладает выраженным водоотнимающим (дегидратационным) свойством: легко извлекает воду из других соединений.
Фосфорные кислоты
- Ортофосфорная кислота - H3PO4 (трехосновная кислота, соли - фосфаты PO4 3- )
- Метафосфорная кислота - HPO3 (одноосновная кислота, соли - метафосфаты PO3 - )
- Фосфористая - H3PO3 (двухосновная кислота, соли - фосфиты HPO3 2- )
- Фосфорноватистая - H3PO2 (одноосновная кислота, соли гипофосфиты - H2PO2 - )
Фосфорноватистая кислота способна вытеснять из солей малоактивные металлы, при этом превращаясь в ортофосфорную кислоту.
Ортофосфорная кислота
В твердом виде представляет собой кристаллы белого цвета, хорошо растворимые в воде.
Фосфорную кислоту получают из фосфатов, воздействуя на них серной кислотой. Также известны способы гидролиза пентахлорида фосфора, взаимодействия оксида фосфора V с водой.
Фосфорная кислота может образоваться при окислении фосфора сильной кислотой:

За счет кислотных свойств отлично реагирует с основными оксидами, основаниями. При различных соотношениях кислоты и основания получаются различные соли (фосфаты, гидрофосфаты и дигидрофосфаты).
Реакции идут, если выделяется газ, выпадает осадок или образуется слабый электролит (вода). Например, характерный осадок желтого цвета - фосфат серебра - образуется в результате реакции с нитратом серебра.
В реакции с карбонатами образуется нестойкая угольная кислота, которая распадается на воду и углекислый газ.
Металлы, стоящие в ряду напряжений до водорода, способны вытеснить водород из фосфорной кислоты.
При сильном нагревании ортофосфорная кислота теряет воду и переходит в метафосфорную кислоту.
Соли фосфорной кислоты
Соли фосфорной кислоты получаются в ходе реакции ортофосфорной кислоты и оснований.
- Фосфоритная мука - Ca3(PO4)2
- Простой суперфосфат - смесь Ca(H2PO4)2*H2O и CaSO4
- Двойной суперфосфат - Ca(H2PO4)2*H2O
- Преципитат - CaHPO4*2H2O
- Костная мука - продукт переработки костей домашних животных Ca3(PO4)2
- Аммофос - в основном состоит из моноаммонийфосфата - NH4H2PO4

Читайте также:
