Простые вещества металлы химия 8 класс презентация
В презентации рассматриваются следующие вопросы: краткая историческая справка, положение элементов металлов в Периодической системе Д.И. Менделеева, нахождение простых веществ-металлов в природе в зависимости от их активности, общие способы получения металлов и их общие физичесие свойства. Так как презентация не сжимается до нужного размера, она прдставлена в 3-х частях.
| Вложение | Размер |
|---|---|
| prostye_veshchestva_metally.pptx | 2.95 МБ |
Подтяните оценки и знания с репетитором Учи.ру
За лето ребенок растерял знания и нахватал плохих оценок? Не беда! Опытные педагоги помогут вспомнить забытое и лучше понять школьную программу. Переходите на сайт и записывайтесь на бесплатный вводный урок с репетитором.
Вводный урок бесплатно, онлайн, 30 минут
Предварительный просмотр:
Подписи к слайдам:
Тема «Простые вещества металлы» Рассматриваемые вопросы: Характеристика металлов по положению в ПСХЭ. 2. Нахождение металлов в природе. 3. Способы получения металлов. 4. Общие физические свойства металлов 1
Краткая историческая справка Каменный век ↓ М едный век (3 -4 тысячелетия до н.э.) ↓ Б ронзовый век (конец 4- начало 1 тысячелетия до н.э.) ↓ Железный век (1 тысячелетие до н.э.)
Каменный век Пирамида Хеопса построена с помощью каменных инструментов
Медный век В начале медного века из меди делали лишь мелкие орудия, украшения , предметы домашней утвари, поскольку этот металл слишком мягок в чистом виде. Именно с открытие меди и других металлов и стала зарождаться профессия кузнеца. Медь «старше» железа на 1,5 – 2 тысячи лет.
Бронзовый век При выплавке меди человек однажды использовал не чистую медную руду, а содержащую одновременно и медь, и олово. В результате была получена бронза – сплав меди с оловом, который гораздо твёрже своих компонентов. Наступил бронзовый век. Слово «бронза» произошло от названия небольшого итальянского городка Бриндизи на берегу Адриатического моря, который славился своими бронзовыми изделиями Колосс Родосский - грандиозная статуя бога солнца - была воздвигнута в портовом городе на острове Родос в Эгейском море, у берегов современной Турции.
Железный век Бронзовый век сменился железным только тогда, когда человечество смогло поднять температуру пламени в металлургических печах до 1540 ° С, т.е. до температуры плавления железа. Было освоено производство железных изделий. Древние металлурги открыли способ изготовления из железных руд сплавов – чугуна и стали, более прочных, чем само железо. Они - основа развития техники и важнейший материал искусства. История железа насчитывает 4 – 4.5 тыс лет. Первое железо, попавшее в руки человека, очевидно, было небесного происхождения, т.е. метеоритное. Об этом говорит наличие изделий из железа у жителей Гренландии, не имевших никакого понятия о железной руде.
Металлы в представлении алхимиков Еще в Древнем Египте семь известных металлов считались представителями семи планет на Земле: Ртуть - Меркурий Олово – Юпитер Свинец – Сатурн Медь - Венера Золото – Солнце Серебро – Луна Железо - Марс 7
Презентация "Простые вещества металлы"
презентация к уроку по химии (8 класс) на тему
Данная презентация может быть полезна при изучении темы "Простые вещества металлы" в 8 , а также при повторении в 9 классе.
| Вложение | Размер |
|---|---|
| prostye_veshchestva_me.pptx | 1 МБ |
Простые вещества Металлы Работу выполнила Круглова И.А. учитель химии МОУ « Глажевская СОШ » Киришского р-на Ленинградской обл.
Цели урока: Повторить особенности строения атомов металлов и металлическую химическую связь Познакомить с общими физическими свойствами металлов Дать понятие об аллотропии
содержание Положение металлов в Периодической системе Д.И.Менделеева особенности строения атомов металлов металлическая химическая связь общие физические свойства металлов понятие аллотропии на примере олова проверим знания
Положение в Периодической системе Д.И.Менделеева Из 110 элементов – 88 металлы Li B Ниже диагонали B –At и элементы побочных подгрупп Fr At
Особенности строения атомов металлов 1-3 е на внешнем уровне большой R a Ме 0 – n е Ме + n
Химическая связь Металлическая в металлах и сплавах Ионная между ионами металла и неметалла
Общие физические свойства металлов Твердость Электропроводность Теплопроводность Металлический блеск Ковкость и пластичность Звон Цвет
Общие физические свойства металлов 1. Твердость ( кроме Hg ) Ртуть- жидкий металл Самый твердый - хром Cr ( царапает стекло) Мягкие – щелочные металлы Li , Na , K , Rb , Cs
2.Электропроводность и теплопроводность Ag Cu Au Al Mg Zn Fe Pb Hg Электропроводность уменьшается Хорошие проводники Ag Cu Au Al Плохие - Pb Hg
3.Металлический блеск Самый блестящий- Hg Венецианские зеркала Менее блестящий- А g Современные зеркала
4.Ковкость и пластичность Наиболее пластичные металлы- Au Ag Cu Sn Pb Zn Подсвечники из золота Очень хрупкие- Cr Mn Хром
5.Звон Самые звонкие- Ag Cu Au Царь-колокол
6.Цвет Черные – Fe и сплавы Чугунная решетка Цветные среди них драгоценные Au Ag Pt Золотые яйца работы К.Фаберже
Аллотропия олова Белое олово b- Sn (металл) Серое олово a- Sn (неметалл)
Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно». Ломоносов
Проверим знания: Вариант 1 1. Какие свойства подчеркивал М. В. Ломоносов, характеризуя металлы как "светлые тела, которые ковать можно"? Выберите правильный ответ: а) теплопроводность, б) обычно серый цвет с металлическим блеском, в) электрическую проводимость, г) пластичность. 2. Выберите самый пластичный драгоценный металл: а) золото, б) серебро, в) платина. 3. Причина электрической проводимости металлов заключается в характерном для них строении: а) наличие в узлах кристаллической решетки ионов, б) наличие в узлах кристаллической решетки атомов, в) присутствие подвижных обобществленных электронов. Вариант 2 1. Как на практике используют пластичность металлов? Выберите правильный ответ: а) делают зеркала, б) используют в качестве проводника электрического тока, в) выковывают изделия разной формы, . г) прокатывают в листы, д ) производят легкие сплавы для конструирования самолетов, ракет, е) вытягивают в проволоку. 2. Выберите самые электропроводные металлы: а) золото, б) серебро, в) натрий, г) железо, д ) медь е) марганец ж) алюминий з ) магний Буквы ответа расположите в порядке убывания электропроводности металлов. 3. Причина пластичности металлов заключается в их строении: а) присутствие подвижных обобществленных электронов, б) наличие в узлах кристаллической решетки ионов, в) наличие в узлах кристаллической решетки атомов.
Презентация по химии для 8 класса по теме "Простые вещества - металлы"

Презентация по химии для 8 класса по теме "Простые вещества - металлы" соответствует программе О.С. Габриеляна.
Просмотр содержимого документа
«Презентация по химии для 8 класса по теме "Простые вещества - металлы"»

Простые вещества-

Цели урока:
- Повторить особенности строения атомов металлов и металлическую химическую связь
- Познакомиться с общими физическими свойствами металлов
Положение в Периодической системе Д.И.Менделеева
Ниже диагонали
B –At и элементы побочных подгрупп

Особенности строения атомов металлов
Химическая связь
в металлах и

Общие физические свойства металлов

Как раньше люди использовали свои знания о металлах?

Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно».
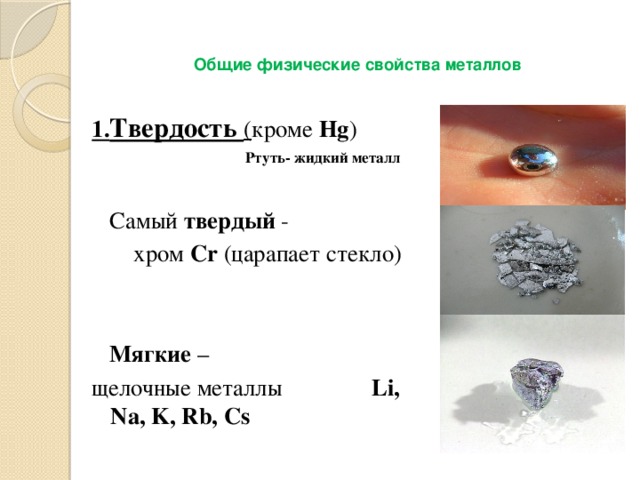
1. Твердость ( кроме Hg )
Ртуть- жидкий металл
Самый твердый -
хром Cr (царапает стекло)
щелочные металлы Li, Na, K, Rb, Cs

2.Электропроводность и теплопроводность Ag Cu Au Al Mg Zn Fe Pb Hg Электропроводность уменьшается
Ag Cu Au Al
3.Металлический блеск
4.Ковкость и пластичность
- Очень хрупкие-
- Наиболее пластичные металлы- Au Ag Cu Sn Pb Zn
Подсвечники из золота

Пластичность - важнейшее свойство металлов изменять свою форму при ударе, прокатываться в тонкие листы и вытягиваться в проволоку.

Царь-колокол

Fe и сплавы
Чугунная решетка
Золотые яйца работы К.Фаберже
Вариант 2
1. Как на практике используют пластичность металлов?
Выберите правильный ответ:
а) делают зеркала,
б) используют в качестве проводника электрического тока,
в) выковывают изделия разной формы, .
г) прокатывают в листы,
д) производят легкие сплавы для конструирования самолетов, ракет,
е) вытягивают в проволоку.
2. Выберите самые электропроводные металлы:
а) золото, б) серебро, в) натрий, г) железо,
д) медь е) марганец ж) алюминий з) магний
Буквы ответа расположите в порядке убывания электропроводности металлов.
3. Причина пластичности металлов заключается в их строении:
а) присутствие подвижных обобществленных электронов,
б) наличие в узлах кристаллической решетки ионов,
в) наличие в узлах кристаллической решетки атомов.
Вариант 1
1. Какие свойства подчеркивал М. В. Ломоносов, характеризуя металлы как "светлые тела, которые ковать можно"? Выберите правильный ответ:
а) теплопроводность,
б) обычно серый цвет с металлическим блеском,
в) электрическую проводимость,
г) пластичность.
2. Выберите самый пластичный драгоценный металл:
а) золото, б) серебро, в) платина.
3. Причина электрической проводимости металлов заключается в характерном для них строении:
а) наличие в узлах кристаллической решетки ионов,
б) наличие в узлах кристаллической решетки атомов,
в) присутствие подвижных обобществленных электронов.
Презентация по химии на тему "Простые вещества - металлы" (8 класс)

«Оловянная чума»
Роберт Скотт
(англ.),
полярный исследователь
Весной 1912 года погибла экспедиция Р.Скотта к Южному полюсу. Причина гибели – «оловянная чума». Экспедиция осталась без горючего из-за того, что топливо просочилось из запаянных оловом баков, поражённых «оловянной чумой»
При t=-33°С белое олово максимально быстро переходит в серое

«Оловянная чума»
Наполеон Бонапарт
Возможно «Оловянная чума» как на одна из причин поражения армии Наполеона в России в 1812 г. — рассыпались оловянные пуговицы на мундирах.
При t=-33°С белое олово максимально быстро переходит в серое

«Оловянная чума»
Музей
А.В. Суворова
г. С-Петербург
«Оловянная чума» погубила ценнейшие коллекции оловянных солдатиков. В петербургском музее А.Суворова, в подвале, где они хранились, лопнули зимой батареи отопления.
При t=-33°С белое олово максимально быстро переходит в серое

Агрегатное состояние – твердые в-ва
искл.:
От сереблисто-белого до темно-серого, искл. Au (желтый) и Cu (красно-коричневый).
Цвет
Электро- и теплопроводность
Причина – относительно
свободные е
_
Hg – жидкий металл

Как правило пластичные (Au, Ag, Cu, Al и др.), искл. Sn (серое),
Твердые (Cr, Fe) и мягкие (Au, Na, K).
Изменяется в широком интервале
Самая высокая:
Tпл.(W)= +3380°С
Самая низкая?
Tпл.(Hg)= − 38,8°С
Пластичность/хрупкость
Твердость/мягкость
Температура плавления

Искл.:
золото и медь
От серебристо-белого до серого
бериллий
германий
литий
Металлический блеск



Температура плавления
Легкоплавкие tТугоплавкие t >1000ºC

Плотность металлов
Легкие (pТяжелые(p>0,5г/мл)

Домашнее задание
Спасибо за внимание!
Белый учебник 8Г, 8К
§ 14, с.85 №1,4
Синий учебник 8А,8Б
§ 13, с. №

Фотографии металлов и неметаллов, изображения кристаллических решеток взяты из ресурсов ИНТЕРНЕТ:
Краткое описание документа:
Данную презентацию учащиеся могут использовать для самостоятельного изучения нового материала, если пропустили урок по какой-либо причине (болезнь, соревнования и т.п.). Возможно использование презентации для повторения материала, например при подготовке к контрольной работе.
Элементы данной презентации можно использовать при введении в тему "Металлы в 9 классе.
Презентация содержит информацию об отличительных физических свойствах металлов, о их возможном применении, а также об аллотропных модификациях на прмере олова.
Рабочие листы и материалы для учителей и воспитателей
Более 3 000 дидактических материалов для школьного и домашнего обучения

Читайте также:
