Олово цветной или черный металл
Цветные металлы — особый класс нержавеющих металлов и сплавов, в составе которых нет железа. Сюда входят олово, медь, цинк, никель, серебро, золото. Металлы называются цветными, потому что каждый из них имеет определенный окрас. Они отличаются прочностью и долговечностью, поскольку формируют на своей поверхности защитную оксидную пленку и проявляют устойчивость к негативным факторам внешней среды.
В начале XX века насчитывалось около 20 наименований нежелезных металлов, а сегодня их количество уже превышает 70. Добычей, обогащением руд и выплавкой таких материалов занимается цветная металлургия. Способ производства — высокотемпературная плавка. За каждым изделием стоит долгая и кропотливая работа — металлы подвергаются механической обработке и проходят через ковку, сварку, прессование, штамповку, грунтование и прочие процессы.
Свойства
Цветные металлы обладают высокой тепло– и электропроводностью, коррозионной стойкостью, стабильностью в температурном диапазоне и инертностью к воздействию агрессивной среды. В отличие от железа, они не реагируют на влагу и кислород, растворяют газы при нагревании (кроме интертных) и с легкостью взаимодействуют с ними.
Группы
Ученые подразделяют цветные металлы на несколько групп:
- Тяжелые. Олово, медь, никель, цинк, свинец и т.п. Добываются из сульфидных и окисленных полиметаллических руд. Мировое производство металлов данной категории достигает нескольких миллионов тонн в год.
- Легкие. Алюминий, титан, магний, натрий, калий, кальций, бериллий, стронций, барий и другие элементы этой группы имеют самую низкую удельную массу среди остальных нежелезных металлов.
- Благородные. Золото, серебро, платина, рутений, родий, палладий, осмий и иридий входят в число редких драгоценных металлов и отличаются повышенной стойкостью к окислению и коррозии.
- Малые. Представители группы — ртуть, кобальт, мышьяк, сурьма, висмут и т.п. Добываются в небольшом количестве вместе с тяжелыми металлами.
- Тугоплавкие. Известны как самые износостойкие металлы. К ним относится цирконий, ванадий, хром, вольфрам, молибден и другие элементы с высокой плотностью и температурой плавления.
- Редкоземельные. Представлены 17 металлами серебристо–белого цвета: гольмий, тулий, скандий, самарий, европий, диспрозий, лютеций, прометий и т.д. Обладают одинаковыми химическими свойствами.
Применение
В последние годы спрос на цветные металлы резко увеличился. Они влияют на развитие многих отраслей промышленности и широко применяются в авиа– и машиностроении, радиоэлектронике, ракетной и атомной технике, сфере высоких технологий, а также в быту.
Нежелезные металлы — незаменимое сырье в производстве металлопроката, крупных конструкций и небольших изделий.
Вы можете заказать цветные металлы и сплавы на нашем сайте. На странице каталога представлен широкий ассортимент товаров с подробным описанием и ценами. Стоимость за 1 кг зависит от вида материала и варьируется от 135 до 2200 рублей. Денежные средства принимаем на расчетный счет. Подробнее об условиях покупки цветного металла в Москве и регионах России читайте здесь.
ОЛОВО — разноликий металл
Металл олово был открыт раньше железа, а его сплав с медью — самый первый, созданный людьми.
Люди отметили значимость бронзы, назвав эпоху своего развития Бронзовым веком.
Неизвестная история
История открытия олова и сплавов из него покрыта пылью времен. Никто не назовет имени первооткрывателя металла, никто не знает — кто догадался первым сплавить олово с медью. Зато известно, что еще 6000 лет назад люди пользовались изделиями из металла.

Происхождение латинского названия ученые выводят из санскритского sta — прочный.
Русское наименование относят к греческим корням. Alophoys по-гечески белый, что указывает на цвет металла.
Свойства Sn

Stannum (Sn) — латинское наименование этого гибкого, пластичного, легкоплавкого металла. Имеет № 50 в периодической таблице Менделеева.
По химическим свойствам металл подобен своим «соседям» — германию и свинцу.
В реакциях проявляет степени окисления +2, +4.
С водой или воздухом не реагирует. Причина этому — пленка оксида на поверхности металла.
Растворяется в разбавленных кислотах; с неметаллами реагирует при нагреве.
Физические свойства олова:
- плотность β-Sn 7,3 г/см3;
- плотность жидкого олова 6,98 г/см³;
- удельная электропроводность 8,69 МСм/м.
Металл обладает редким свойством: плавится при низкой температуре (232°С), а кипит при высокой (2620°С).
| Свойства атома | |
|---|---|
| Название, символ, номер | О́лово / Stannum (Sn), 50 |
| Атомная масса (молярная масса) | 118,710(7)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Kr] 4d10 5s2 5p2 |
| Радиус атома | 162 пм |
| Химические свойства | |
| Ковалентный радиус | 141 пм |
| Радиус иона | (+4e) 71 (+2) 93 пм |
| Электроотрицательность | 1,96 (шкала Полинга) |
| Электродный потенциал | −0,136 |
| Степени окисления | +4, +2 |
| Энергия ионизации (первый электрон) | 708,2 (7,34) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 7,31 г/см³ |
| Температура плавления | 231,91 °C[2] |
| Температура кипения | 2893 K, 2620 °C[3] |
| Уд. теплота плавления | 7,19[2]; кДж/моль |
| Уд. теплота испарения | 296[4] кДж/моль |
| Молярная теплоёмкость | 27,11[4] Дж/(K·моль) |
| Молярный объём | 16,3 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | тетрагональная |
| Параметры решётки | a=5,831; c=3,181 Å |
| Отношение c/a | 0,546 |
| Температура Дебая | 170,00 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 66,8 Вт/(м·К) |
| Номер CAS | 7440-31-5 |
Аллотропные свойства олова
Аллотропия — свойство элемента менять свою кристаллическую решетку при изменении температуры. Модификация альфа (серое олово) устойчиво при низких температурах (ниже 13 °С). Имеет кубическую решетку, по типу алмаза. Практического применения не имеет.
Бета-модификация (белое, металлическое олово), из которого делают солдатиков, им же покрывают консервные банки. Кристаллическая структура тетрагональная.

В гамма-модификацию металл переходит при температуре 161-232°С.
Печально: в музее А.В. Суворова случилось несчастье. В запаснике, где хранилась ценная коллекция оловянных солдатиков, зимой лопнули трубы отопления, и коллекция просто рассыпалась в пыль.
Маркировка металла
Промышленность выпускает металл в проволоке, чушках, прутках.
Месторождения оловянных руд
Д.И. Менделеев писал:
«Олово встречается в природе редко, в жилах древних пород, почти исключительно в виде окиси SnO2, называемой оловянным камнем».
Олово относится к редким рассеянным металлам. В природе среди элементов занимает 47-е место по распространенности.
Мировые запасы оловянных руд расположены в:
- Китае;
- Малайзии;
- Индонезии;
- Бразилии;
- Перу;
- Австралии.
Значимые месторождения российских оловянных руд сосредоточены на Дальнем Востоке (в Приморском крае, в Якутии, в Хабаровском крае). Добыча металла большей частью происходит в подземных шахтах.
Основные руды:
- оловянный камень, касситерит — содержит до 78% металла;

Печально: по подсчетам ученых, оловосодержащих минералов на Земле осталось лет на 30. Потом придется добывать его из лома, или искать замену…
Сплавы
По своей классификации оловянные сплавы делятся на припои, подшипниковые и легкоплавкие.
- Баббиты. В них добавляют свинец, медь, сурьма. Баббиты могут иметь легирующие присадки. Маркировки баббитов: Б88, Б83, Б83С.
- Бронза — сплав меди с оловом. Любая бронза содержит небольшие добавки фосфора, цинка, свинца, никеля и других элементов. Марки бронзы: Бр ОФ 6,5-0,15; Бр.ОЦ 4-3; Бр.ОЦ10-2; Бр.ОФ 10-1; Бр.ОНС 11-4-3.
- Пьютер. Сплав с висмутом, сурьмой, медью, изредка со свинцом.
- Припои. Бывают твердые и легкоплавкие. В сплав добавляют свинец и другие элементы. Марки припоев: ПОС-30, ПОС-40, ПОС-90.
Плюсы и минусы олова
К достоинствам относим:
- Нетоксичность, это позволяет использовать металл в пищевой промышленности, в производстве посуды.
- Достойная антикоррозионная устойчивость в агрессивных средах.
- Не реагирует с серой; поэтому используют везде, где металл «завернут» в резиновую или пластиковую изоляцию.
- Подвержен «оловянной чуме».
- Довольно высокая стоимость ограничивает широкое применение металла.
- Невысокая температура плавления (всего 232°С).
Производство изделий из олова и его сплавов
Продукция из олова была востребована с давних времен. Дети играют в оловянных солдатиков уже 4000 лет.
- Электроника с ее платами сейчас повсюду, и любые контакты соединяются припоем из олова и его сплавов. Оловянное напыление для медных проводов полезно, это защита от воздействия серы (она входит в состав резиновой изоляции).
- Оловянные сплавы баббиты обладают прекрасными антифрикционными свойствами. Ни один из механизмов (от велосипеда до могучего КРАЗа) не обходится без подшипников.
- Используют металл в типографском сплаве гарте. Полиграфическое производство невозможно без оловянных сплавов.

Воздействие на организм оловянных изделий минимально. Поэтому применение металла в пищевой промышленности вполне оправдано.
Простая консервная банка и гибель полярной экспедиции
Французский повар Франсуа Аппер придумал, как долго хранить пищу. Он предложил герметично закрывать продукты в банки из белой жести (это тонкий лист из железа, покрытый оловянным напылением). Теперь мы не можем представить жизни без баночки вкусных консервов.
Но те же консервные банки (вернее, «оловянная чума») способствовали гибели экспедиции Р. Скотта к Южному полюсу. Из баков, запаянных оловянным припоем, вылилось горючее. Металл перешел в альфа-модификацию и просто раскрошился на морозе.
Стоимость олова
Главная мировая площадка инвесторов в металлы находится в Лондоне. Это LME (Лондонская биржа металлов).
Цена тонны олова на LME составляла 15590,0 US$ за тонну (данные на 28.05.2020).

Мне 42 года и я специалист в области минералогии. Здесь на сайте я делюсь информацией про камни и их свойства — задавайте вопросы и пишите комментарии!
Какие металлы и сплавы относятся к чёрным, а какие к цветным?
К цветным металлам* и сплавам относятся практически все металлы и сплавы, за исключением железа и его сплавов, образующих группу чёрных металлов. Цветные металлы встречаются реже, чем железо и часто их добыча стоит значительно дороже, чем добыча железа. Однако цветные металлы часто обладают такими свойствами, какие у железа не обнаруживаются, и это оправдывает их применение.
Выражение «цветной металл» объясняется цветом некоторых тяжёлых металлов: так, например, медь имеет красный цвет.
Если металлы соответствующим образом смешать (в расплавленном состоянии) , то получаются сплавы. Сплавы обладают лучшими свойствами, чем металлы, из которых они состоят. Сплавы, в свою очередь, подразделяются на сплавы тяжёлых металлов, сплавы лёгких металлов и т. д.
Цветные металлы по ряду признаков разделяют на следующие группы:
- тяжёлые металлы — медь, никель, цинк, свинец, олово;
- лёгкие металлы — алюминий, магний, титан, бериллий, кальций, стронций, барий, литий, натрий, калий, рубидий, цезий;
- благородные металлы — золото, серебро, платина, осмий, рутений, родий, палладий;
- малые металлы — кобальт, кадмий, сурьма, висмут, ртуть, мышьяк;
- тугоплавкие металлы — вольфрам, молибден, ванадий, тантал, ниобий, хром, марганец, цирконий;
- редкоземельные металлы — лантан, церий, празеодим, неодим, самарий, европий, гадолиний, тербий, иттербий, диспрозий, гольмий, эрбий, тулий, лютеций, прометий, скандий, иттрий;
- рассеянные металлы — индий, германий, таллий, таллий, рений, гафний, селен, теллур;
- радиоактивные металлы — уран, торий, протактиний, радий, актиний, нептуний, плутоний, америций, калифорний, эйнштейний, фермий, менделевий, нобелий, лоуренсий.
Чаще всего цветные металлы применяют в технике и промышленности в виде различных сплавов, что позволяет изменять их физические, механические и химические свойства в очень широких пределах. Кроме того, свойства цветных металлов изменяют путём термической обработки, нагартовки, эа счёт искусственного и естественного старения и т. д.
К черным металлам относятся железо и его сплавы (сталь, чугун и ферросплавы)
Наибольшее распространение в технике получили черные металлы. Это обусловлено большими запасами железных руд в земной коре, сравнительной простотой технологии выплавки черных металлов, их высокой прочностью.
Основными металлическими материалами современной
техники являются сплавы железа с углеродом. В зависимости
от содержания углерода эти сплавы делятся на стали и
ч у г у н ы.
Сталь — железоуглеродистый сплав, в котором углерода содержится до 2%. Стали присущи свойства, делающие ее незаменимым материалом в машиностроении. Она обладает высокой прочностью и твердостью, хорошо сопротивляется ударным нагрузкам. Сталь можно ковать, прокатывать, легко обрабатывать на металлорежущих станках. Стальные изделия хорошо свариваются.
Чугун — железоуглеродистый сплав с содержанием углерода свыше 2%. В технике наибольшее применение получили чугуны, имеющие от 2,5 до 3,5% углерода.
Чугун более хрупок, чем сталь, он хуже сваривается, но обладает лучшими литейными свойствами. Поэтому изделия из чугуна получают исключительно литьем. Около 80% чугуна идет на переплавку в сталь.
ЦВЕТНЫЕ МЕТАЛЛЫ — всё, кроме железа
Цветные металлы отличаются от черных. Цветных металлов много, а к черным относятся только железо, его сплавы. Часто к черным металлам относят ванадий, марганец, хром.
В Европе цветные металлы называют нежелезными, происхождение этих названий точнее отражает суть и свойства наших героев.
- Англичане называют их non-ferrous metals.
- Для немцев их название — Nichteisenmetalle, Buntmetalle.
- Французы обозначили цветные металлы как меtaux non-ferreux.
Разделяем металлы по свойствам и группам
Условно цветные металлы различают на 2 большие группы — тяжелые и легкие.

Более подробная классификация проводится по свойствам (физико-химическим). Есть разделение на 5 и 7 групп.
Виды цветных металлов:
- Легкие цветные металлы.
- Тяжелые металлы. .
- Редкие и малые.
- Рассеянные.
- Радиоактивные.
- Тугоплавкие.
Свойства цветных металлов разнообразны. Это устойчивость к коррозии, высокие электро-и теплопроводность, устойчивость во многих агрессивных средах.
Где применяются
Представьте мир без цветных металлов. Выбросите телефон и компьютер, вместе с ними ключи от машины. Отключите свет — ведь ток течет по проводам из цветмета. Газовую и электрическую плиту тоже придется выбросить, а готовить на костре или построить печку. Поэтому к этим разным и таким нужным человечеству металлам давайте относиться уважительно.
Невозможно представить современный мир без использования цветных металлов.
Некоторые из них добываются миллионами тонн в год, другие по несколько тонн в год. Но все они абсолютно необходимы современной промышленности и нам, потребителям.
Электротехника, легировка сталей, сенсоры, диоды, термопары, инфракрасная оптика, военно-промышленный комплекс.
Знакомство с нежелезными металлами
Список цветных металлов обширен. Руд цветных металлов в разы больше.

Важными рудами на медь являются халькозин, борнит, халькопирит. Встречается и самородная медь, но редко. Про медь читайте здесь.

Добычу медных руд производят:
Познавательно: крупнейшее месторождение в мире находится в знойной пустыне Атакама, его пока не разрабатывают.
Алюминий
Главное сырье на алюминий — бокситы. Руды бокситов — диаспор (его ювелирная разновидность султанит подробно описана здесь), гетит, бемит, каолинит. Подробнее про этот металл читайте на этой странице.

Российские месторождения бокситов находятся в областях:
- Архангельской;
- Белгородской;
- Свердловской;
- Челябинской.
Богатые запасы бокситов расположены в Корее, Венгрии, Югославии, Китае.
Значительные запасы бокситовых руд в Австралии, Бразилии, США, Франции.
Свинец
Главная руда на свинец — галенит, кроме него церуссит и англезит.

Галенит образует полиметаллические руды со сфалеритом и халькопиритом.
48 стран мира могут добывать на своей территории свинец.
Основная цинковая руда — сфалерит. Это сульфид цинка, и в природе его естественными спутниками являются галенит и халькопирит.

Главные мировые запасы цинка находятся в Канаде, немногим отстают Китай, Австралия, США.
В России цинк добывают на Каменном Поясе. Есть месторождения в Сибири и Приморье.
Магний
Этого цветного металла в земной коре около 2%.

Руд, содержащих магний, около 60, но для промышленной добычи используют:
- доломит;
- магнезит;
- брусит;
- карналлит;
- морская вода.
Каждая страна обладает запасами магния. Магнезит находят в США, Испании, Австралии, Канаде, Югославии, Греции. Карналлит используют в странах СНГ.
Огромные запасы магния находятся в воде залива Кара-Богаз-Гол.
Никель
Никелевые руды могут быть сульфидные и силикатные. Подробнее о металле читайте здесь.

- халькопирит;
- пирротин;
- магнетит;
- пентландит.
Силикатные никелевые руды:
- гарниерит;
- гетит;
- ревдинскит;
- контронит;
- асболан.
Кобальт
В природе немного кобальтсодержащих руд, особенно пригодных для промышленного использования. Среди них кобальтин, скуттерудит, линнеит, шмальтин, эритрин.

По минеральному и химическому составу кобальтовые руды делятся на сульфидные, арсенидные, оксидные. В основном все руды комплексные, собственно кобальтовые встречаются только среди мышьяковых (арсенидных) руд.
За рубежом кобальтосодержащие месторождения находятся в Канаде, Финляндии, Австралии, Африке.
В России — на Урале, в Красноярском крае, на Кольском полуострове.
Основные добытчики кобальта — Заир и Замбия.
Олово
Главные минералы для добычи олова — касситерит и станнин. Половина добычи олова приходится на месторождения Юго-Восточной Азии. Подробнее про олово написано здесь.

Немного отстает Китай, за ним идут Индонезия, Малайзия, Бразилия, Россия.
Молибден
Основной рудный минерал на молибден — молибденит. В природе «дружит» с сульфидами меди и касситеритом.

В добыче металла первенствуют США, следом идут Чили и Китай, на третьем месте — Канада.
В России тоже есть молибденовые руды, в Забайкалье, на Северном Кавказе, на юге Западной Сибири.
Вольфрам
Основные руды на вольфрам — вольфрамит и шеелит.

Китаю повезло, у него более 40% мировых запасов вольфрамита. Россия отстала не сильно, у нас шеелит есть на Кавказе, в Забайкалье, на Чукотке.
Есть месторождения в Германии, Канаде, Турции, США.
Висмут
Существует самородный висмут. В Боливии и Австралии его добывают вместе с висмутином. Подробнее о нём читайте здесь.

Боливия единственная страна, где металл добывают прямо из висмутовой руды. В основном висмут извлекают из полиметаллических руд.
Мировые лидеры по запасам:
- Перу;
- Мексика;
- Китай;
- Австралия;
- Канада.
Месторождения висмутовых руд редки и невелики по масштабам.
Сурьма
Главный источник сурьмы — антимонит. Кроме него, рудой на сурьму могут служить бертьерит, джемсонит, ливингстонит, стибиконит.

Австралия, Россия и Китай обладают залежами антимонита, остальные страны могут только облизываться на такое богатство. Среди завидующих США, КНР, ЮАР. У них есть полиметаллические месторождения.
Ртуть
Киноварь — единственный минерал для качественной добычи ртути.

Основные производители жидкого металла:
Россия обладает небольшими запасами киновари на Чукотке, Алтае, Камчатке.
У Америки с этим и того хуже — маленький рудничок в Неваде.
А вот на юге Испании известно ртуть добывают почти две тысячи лет.
Вторичное сырье
Уже понятно, что добыча цветмета не всегда обеспечивает потребности промышленности. Приходится изворачиваться. То есть организовывать пункты приема вторсырья, собирать металлолом для сдачи в этих пунктах. Кстати, за лом цветных металлов платят довольно неплохо.
Стоимость металлических отходов формируется, исходя из нескольких компонентов:
- Металл (тип, редкость).
- Габариты.
- Размер партии.
- Чистота металла, его качество.
Охотникам за металлоломом
Большим спросом у приемщиков пользуются медь, алюминий, свинец, титан.
- Медь содержат сплавы меди (латунь).
- Олово гораздо дороже меди, особенно в чистом виде, но и в виде посуды, баббита (в подшипниках, например).
- Никель металл дорогостоящий, но в чистом виде попадается редко. В мельхиоровой посуде, отработанных электродах, ТЭНах бытовых приборов.
- Свинец сдают «в виде» аккумуляторов, типографского оборудования, оплетки кабелей.
- Алюминий стоит недорого.
- Чистый цинк найти проблематично, сдают его в виде сплавов.
- Самые дорогие металлы — молибден и вольфрам.
Плюсы и минусы переработки вторсырья
Перерабатывать металлолом выгодно, это понижает себестоимость продукции.
Цветмет приходится сортировать — это самый нудный и трудоемкий этап работы.
Рассортированное сырье измельчают. Для этого применяют газовые резки, шредеры, а потом прессуют для уменьшения объемов и удобства транспортировки.
Далее подготовленное сырье отправляют на металлургические комбинаты, или продают (чаще всего на экспорт).
14 различных типов металлов

Термин "металл" происходит от греческого слова "metalléuō", что означает выкапываю или добываю из земли. Наша планета содержит много металла. На самом деле из 118 элементов периодической системы порядка 95 являются металлами.
Это число не является точным, потому что граница между металлами и неметаллами довольно расплывчата: нет стандартного определения металлоида, как нет и полного согласия относительно элементов, соответствующим образом классифицированных как таковые.
Сегодня мы используем различные виды металлов, даже не замечая их. Начиная с зажимов в сантехнике и заканчивая устройством, которое вы используете для чтения этой статьи, все они сделаны из определенных металлов. Фактически, некоторые металлические элементы необходимы для биологических функций, таких как приток кислорода и передача нервных импульсов. Некоторые из них также широко используются в медицине в виде антацидов.
Все металлы в периодической таблице можно классифицировать по их химическим или физическим свойствам. Ниже мы перечислили некоторые различные типы металлов вместе с их реальным применением.
Классификация по физическим свойствам
14. Легкие металлы

Сплав титана 6AL-4V
Примеры: Алюминий, титан, магний
Легкие металлы имеют относительно низкую плотность. Формального определения или критериев для идентификации этих металлов нет, но твердые элементы с плотностью ниже 5 г/см³ обычно считаются легкими металлами.
Металлургия легких металлов была впервые развита в середине 19 века. Хотя большинство из них происходит естественным путем, значительная их часть образуется при электротермии и электролизе плавленых солей.
Их сплавы широко используются в авиационной промышленности благодаря их низкой плотности и достаточным механическим свойствам. Например, сплав титана 6AL-4V составляет почти 50 процентов всех сплавов, используемых в авиастроении. Он используется для изготовления роторов, лопастей компрессоров, мотогондол, компонентов гидравлических систем.
13. Тяжелые металлы

Окисленные свинцовые конкреции и кубик размером 1 см3
Примеры: железо, медь, кобальт, галлий, олово, золото, платина.
Тяжелые металлы - это элементы с относительно высокой плотностью (обычно более 5 г/см³) и атомным весом. Они, как правило, менее реактивны и содержат гораздо меньше растворимых сульфидов и гидроксидов, чем более легкие металлы.
Эти металлы редки в земной коре, но они присутствуют в различных аспектах современной жизни. Они используются в солнечных батареях, сотовых телефонах, транспортных средствах, антисептиках и ускорителях частиц.
Тяжелые металлы часто смешиваются в окружающей среде из-за промышленной деятельности, ухудшая качество почвы, воды и воздуха, а затем вызывая проблемы со здоровьем у животных и растений. Выбросы транспортных средств, горнодобывающие и промышленные отходы, удобрения, свинцово-кислотные батареи и микропластики, плавающие в океанах, являются одними из наиболее распространенных источников тяжелых металлов в этом контексте.
12. Белый металл

Подшипники из белого металла
Примеры: Обычно изготавливается из олова, свинца, висмута, сурьмы, кадмия, цинка.
Белые металлы - это различные светлые сплавы, используемые в качестве основы для украшений или изделий из серебра. Например, многие сплавы на основе олова или свинца используются в ювелирных изделиях и подшипниках.
Белый металлический сплав изготавливается путем объединения определенных металлов в фиксированных пропорциях в соответствии с требованиями конечного продукта. Основной металл для ювелирных изделий, например, формуется, охлаждается, экстрагируется, а затем полируется, чтобы придать ему точную форму и блестящий вид.
Они также используются для изготовления тяжелых подшипников общего назначения, подшипников внутреннего сгорания среднего размера и электрических машин.
11. Хрупкий металл

Хрупкое разрушение чугуна
Примеры: сплавы углеродистой стали, чугуна и инструментальной стали.
Металл считается хрупким, если он твердый, но не может противостоять ударам или вибрации под нагрузкой. Такие металлы под воздействием напряжения ломаются без заметной пластической деформации. Они имеют низкую прочность на разрыв и часто издают щелкающий звук при поломке.
Многие стальные сплавы становятся хрупкими при низких температурах, в зависимости от их обработки и состава. Чугун, например, твердый, но хрупкий из-за высокого содержания углерода. Напротив, керамика и стекло гораздо более хрупки, чем металлы, из-за их ионных связей.
Галлий, висмут, хром, марганец и бериллий также хрупки. Они часто используются в различных гражданских и военных целях, связанных с высокими деформационными нагрузками. Чугун, устойчивый к повреждениям в результате окисления, используется в машинах, трубах и деталях автомобильной промышленности, таких как корпуса коробок передач и головки цилиндров.
10. Тугоплавкий металл
Микроскопическое изображение вольфрамовой нити в лампе накаливания
Примеры: молибден, вольфрам, тантал, рений, ниобий.
Тугоплавкие металлы имеют чрезвычайно высокие температуры плавления (более 2000 °С) и устойчивы к износу, деформации и коррозии. Они являются хорошими проводниками тепла и электричества и имеют высокую плотность.
Другой ключевой характеристикой является их термостойкость: они не расширяются и не растрескиваются при многократном нагревании и охлаждении. Однако они могут деформироваться при высоких нагрузках и окисляться при высоких температурах.
Благодаря своей прочности и твердости они идеально подходят для сверления и резки. Карбиды и сплавы тугоплавких металлов используются почти во всех отраслях промышленности, включая горнодобывающую, автомобильную, аэрокосмическую, химическую и ядерную.
Металлический вольфрам, например, используется в ламповых нитях. Сплавы рения используются в гироскопах и ядерных реакторах. А ниобиевые сплавы используются для форсунок жидкостных ракетных двигателей.
9. Черные и цветные металлы

Валы-шестерни из (черной) нержавеющей стали
Черные металлы: Сталь, чугун, сплавы железа.
Цветные металлы: Медь, алюминий, свинец, цинк, серебро, золото.
Термин "железо" происходит от латинского слова "Ferrum", что переводится как "железо". Таким образом, термин "черный металл" обычно означает "содержащий железо", тогда как "цветной металл" означает металлы и сплавы, которые не содержат достаточного количества железа.
Поскольку черные металлы могут иметь широкий спектр легирующих элементов, которые значительно изменяют их характеристики, очень трудно поместить свойства всех черных металлов под один зонт. Тем не менее некоторые обобщения могут быть сделаны, например, большинство черных металлов являются твердыми и магнитными.
Черные металлы используются для применения с высокой нагрузкой и низкой скоростью, в то время как цветные металлы предпочтительны для применения с высокой скоростью и нулевой нагрузкой для применения с низкой нагрузкой.
Сталь является наиболее распространенным черным металлом. Она составляет около 80% всего металлического материала благодаря своей доступности, высокой прочности, низкой стоимости, простоте изготовления и широкому спектру свойств. Она широко используется в строительстве и обрабатывающей промышленности. Фактически, рост производства стали показывает общее развитие промышленного мира.
8. Цветные и благородные металлы

Ассортимент благородных металлов
Цветные металлы: медь, алюминий, олово, никель, цинк
Благородные металлы: родий, ртуть, серебро, рутений, осмий, иридий
Цветные металлы - это обычные и недорогие металлы, которые корродируют, окисляются или тускнеют быстрее, чем другие металлы, когда подвергаются воздействию воздуха или влаги. Они в изобилии встречаются в природе и легко добываются.
Они широко используются в промышленных и коммерческих целях и имеют неоценимое значение для мировой экономики благодаря своей полезности и повсеместности. Некоторые цветные металлы обладают отличительными характеристиками, которые не могут быть продублированы другими металлами. Например, цинк используется для гальванизации стали, чтобы защитить ее от коррозии, а никель - для изготовления нержавеющей стали.
Благородные металлы, с другой стороны, устойчивы к окислению и коррозии во влажном воздухе. Согласно атомной физике, благородные металлы имеют заполненный электрон d-диапазона. В соответствии с этим строгим определением, медь, серебро и золото являются благородными металлами.
Они находят применение в таких областях, как орнамент, металлургия и высокие технологии. Их точное использование варьируется от одного элемента к другому. Некоторые благородные металлы, такие как родий, используются в качестве катализаторов в химической и автомобильной промышленности.
7. Драгоценные металлы

Родий: 1 грамм порошка, 1 грамм прессованного цилиндра и 1 г аргонодуговой переплавленной гранулы
Примеры: палладий, золото, платина, серебро, родий.
Драгоценные металлы считаются редкими и имеют высокую экономическую ценность. Химически они менее реакционноспособны, чем большинство элементов (включая благородные металлы). Они также пластичны и имеют высокий блеск.
Несколько веков назад эти металлы использовались в качестве валюты. Но сейчас они в основном рассматриваются как промышленные товары и инвестиции. Многие инвесторы покупают драгоценные металлы (в основном золото), чтобы диверсифицировать свои портфели или победить инфляцию.
Серебро - второй по популярности драгоценный металл для ювелирных изделий (после золота). Однако его значение выходит далеко за рамки красоты. Оно обладает исключительно высокой тепло- и электропроводностью и чрезвычайно низким контактным сопротивлением. Именно поэтому серебро широко используется в электронике, батареях и противомикробных препаратах.
Классификация по химическим свойствам
6. Щелочные металлы

Твердый металлический натрий
Примеры: натрий, калий, рубидий, литий, цезий и франций.
Щелочь относится к основной природе гидроксидов металлов. Когда эти металлы реагируют с водой, они образуют сильные основания, которые легко нейтрализуют кислоты.
Они настолько реактивны, что обычно встречаются в природе в слиянии с другими веществами. Карналлит (хлорид калия-магния) и сильвин (хлорид калия), например, растворимы в воде и, таким образом, легко извлекаются и очищаются. Нерастворимые в воде щелочи, такие, как фторид лития, также существуют в земной коре.
Одно из самых популярных применений щелочных металлов - использование цезия и рубидия в атомных часах, наиболее точных из известных эталонов времени и частоты. Литий используется в качестве анода в литиевых батареях, композиты калия используются в качестве удобрений, а ионы рубидия используются в фиолетовых фейерверках. Чистый металлический натрий широко используется в натриевых лампах, которые очень эффективно излучают свет.
5. Щелочноземельные металлы

Изумрудный кристалл, основной минерал бериллия.
Примеры: бериллий, кальций, магний, барий, стронций и радий.
Щелочноземельные металлы в стандартных условиях мягкие и серебристо-белые. Они имеют низкую плотность, температуру кипения и температуру плавления. Хотя они не так реакционноспособны, как щелочные металлы, они очень легко образуют связи с элементами. Как правило, они вступают в реакцию с галогенами, образуя галогениды щелочноземельных металлов.
Все они встречаются в земной коре, кроме радия, который является радиоактивным элементом. Радий уже распадался в ранней истории Земли из-за относительно короткого периода полураспада (1600 лет). Современные образцы поступают из цепочки распада урана и тория.
Щелочноземельные металлы имеют широкий спектр применения. Бериллий, например, используется в полупроводниках, теплопроводниках, электрических изоляторах и в военных целях. Магний часто сплавляют с цинком или алюминием для получения материалов со специфическими свойствами. Кальций в основном используется в качестве восстановителя, а барий используется в вакуумных трубках для удаления газов.
4. Переходные металлы
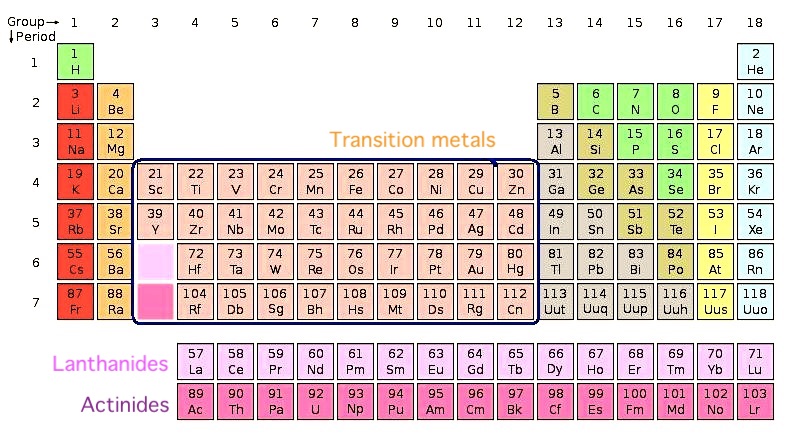
Примеры: титан, ванадий, хром, никель, серебро, вольфрам, платина, кобальт.
Большинство элементов используют электроны из своей внешней оболочки для связи с другими элементами. Переходные металлы, однако, могут использовать две крайние оболочки для соединения с другими элементами. Это химическая особенность, которая позволяет им связываться со многими различными элементами в различных формах.
Они занимают среднюю часть таблицы Менделеева, служа мостом между (или переходом) между двумя сторонами таблицы. Более конкретно, есть 38 переходных металлов в группах с 3 по 12 периодической таблицы. Все они являются пластичными, податливыми и хорошими проводниками тепла и электричества.
Многие из этих металлов, такие как медь, никель, железо и титан, используются в конструкциях и в электронике. Большинство из них образуют полезные сплавы друг с другом и с другими металлическими веществами. Некоторые из них, включая золото, серебро и платину, называются благородными металлами, потому что они крайне инертны и устойчивы к кислотам.
3. Постпереходные металлы

Висмут в виде синтетических кристаллов
Примеры: алюминий, галлий, олово, свинец, таллий, индий, висмут.
Постпереходные металлы в периодической таблице - это элементы, расположенные справа от переходных металлов и слева от металлоидов. Из-за своих свойств они также называются "бедными" или "другими" металлами.
Физически они хрупки (или мягки) и имеют более низкую температуру плавления и механическую прочность, чем переходные металлы. Их кристаллическая структура довольно сложна: они проявляют ковалентные или направленные эффекты связи.
Различные металлы этого семейства имеют различное применение. Алюминий, например, используется для изготовления оконных рам, кухонной посуды, банок, фольги, деталей автомобилей. Оловянные сплавы используются в мягких припоях, оловянных и сверхпроводящих магнитах.
Индиевые сплавы используются для изготовления плоских дисплеев и сенсорных экранов, а галлий - в топливных элементах и полупроводниках.
2. Лантаноиды

1-сантиметровый кусок чистого лантана
Примеры: лантан, церий, прометий, гадолиний, тербий, иттербий, лютеций.
Лантаноиды - это редкоземельные металлы с атомными номерами от 57 до 71. Впервые они были обнаружены в 1787 году в необычном черном минерале (гадолините), обнаруженном в Иттербю, Швеция. Позже минерал был разделен на различные элементы лантаноидов.
Лантаноиды - это металлы с высокой плотностью, плотность которых колеблется от 6,1 до 9,8 г/см³, и они, как правило, имеют очень высокие температуры кипения (1200-3500 °C) и очень высокие температуры плавления (800-1600 °C).
Сплавы лантаноидов используются в металлургии из-за их сильных восстановительных способностей. Около 15 000 тонн лантаноидов ежегодно расходуется в качестве катализаторов и при производстве стекол. Они также широко используются в лазерах и оптических усилителях.
Некоторые исследования показывают, что лантаноиды могут быть использованы в качестве противораковых средств. Лантан и церий, в частности, могут подавлять пролиферацию раковых клеток и способствовать цитотоксичности.
1. Актиниды

Металлический уран, высокообогащенный ураном-235
Примеры: актиний, уран, торий, плутоний, фермий, нобелий, лоренций
Подобно лантаноидам, актиниды образуют семейство редкоземельных элементов с аналогичными свойствами. Они представляют собой серию из 15 последовательных химических элементов в периодической системе от атомных номеров 89 до 103.
Все они радиоактивны по своей природе. Синтетически произведенный плутоний, а также природные уран и торий являются наиболее распространенными актинидами на Земле. Первым актинидом, который был открыт в 1789 году, был уран. И большая часть существующих продуктов актинидов была произведена в 20 веке.
Их свойства, такие как излучение радиоактивности, пирофорность, токсичность и ядерная критичность, делают их опасными для обращения. Сегодня значительная часть (кратковременных) актинидов производится ускорителями частиц в исследовательских целях.
Некоторые актиниды нашли применение в повседневной жизни, например, газовые баллоны (торий) и детекторы дыма (америций), большинство из них используются в качестве топлива в ядерных реакторах и для изготовления ядерного оружия. Уран-235 является наиболее важным изотопом для применения в ядерной энергетике, который широко используется в тепловых реакторах.
Читайте также:
