Наиболее распространенный элемент металл земной коры
Главным объектом геологических, в том числе минералогических, исследований является земная кора , под которой подразумевается самая верхняя оболочка земного шара, доступная непосредственному наблюдению.
Наши фактические знания о строении и химическом составе земной коры основываются почти исключительно на наблюдениях над самыми поверхностными частями нашей планеты.
Горообразующие процессы, совершавшиеся в различные геологические эпохи и приводившие к образованию высоких горных хребтов, подняли из глубины самые различные породы, не образующиеся вблизи поверхности Земли. Наиболее глубинные по происхождению горные породы из доступных прямому изучению — мантийные ксенолиты, обнаруживаемые в трубках взрыва, — являются объектом пристального внимания исследователей. Их изучение дает возможность, как показывают геологические наблюдения и подсчеты, получить более или менее реальное представление о составе и строении земного шара только до глубины 100–150 км (радиус же его превышает 6300 км).
О строении и составе глубоких недр земного шара можно судить лишь на основании косвенных данных. Как показывает сопоставление плотностей всего земного шара (5,527) и земной коры (2,7–2,8), внутренние части нашей планеты должны обладать значительно большей плотностью, чем поверхностные. Различные данные (геофизические наблюдения, данные сравнения Земли с другими космическими телами, состав метеоритов и пр.) дают основания предполагать, что это обстоятельство обусловлено не только увеличением с глубиной давления, но и изменением состава внутренних частей нашей планеты.
Согласно современным моделям, построенным на основании геофизических данных, в строении Земли выделяется несколько концентрических оболочек (геосфер, рис. 3), различающихся по физическим свойствам и составу (табл. 1).
Таблица 1. Характеристики геосфер Земли
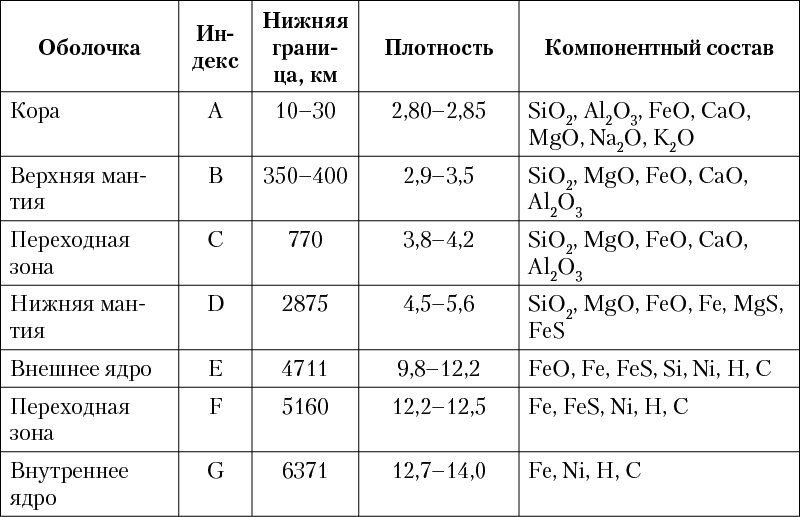
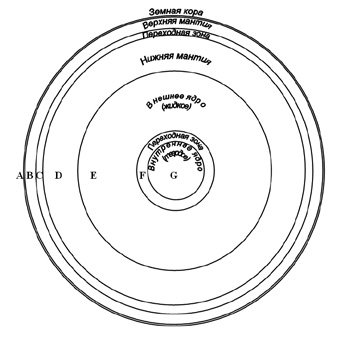
Рис. 3. Схема внутреннего строения Земли
(мощность земной коры отражена вне масштаба)
Состав земной коры
Впервые состав твердой части земной коры в весовых процентах подсчитал американский исследователь Ф. Кларк в 1889 г. Большая работа по уточнению полученных цифр была проделана В. И. Вернадским, А. Е. Ферсманом, И. и В. Ноддаками, Г. Гевеши, В. М. Гольдшмидтом и А. П. Виноградовым. Последний подсчитал средний химический состав лишь литосферы (без учета гидросферы и атмосферы).
По предложению акад. Ферсмана средние цифры содержаний отдельных элементов земной коры стали называть «числами Кларка», или просто кларками. Он же предложил выражать эти величины не только в весовых процентах, но и в атомных.
Из более чем 100 химических элементов, приведенных в периодической таблице элементов Менделеева (табл. 2), лишь немногие широко распространены в земной коре. Такие элементы в таблице располагаются преимущественно в верхней ее части, т. е. относятся к числу элементов с малыми порядковыми номерами.
Таблица 2. Периодическая система элементов Д. И. Менделеева
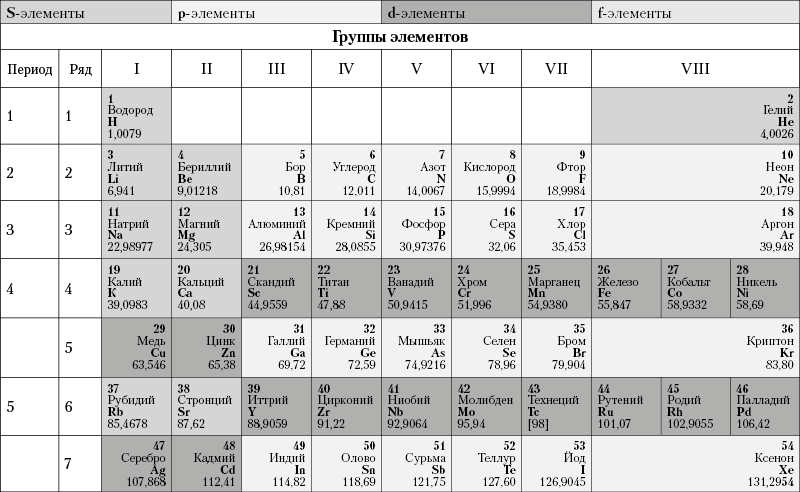
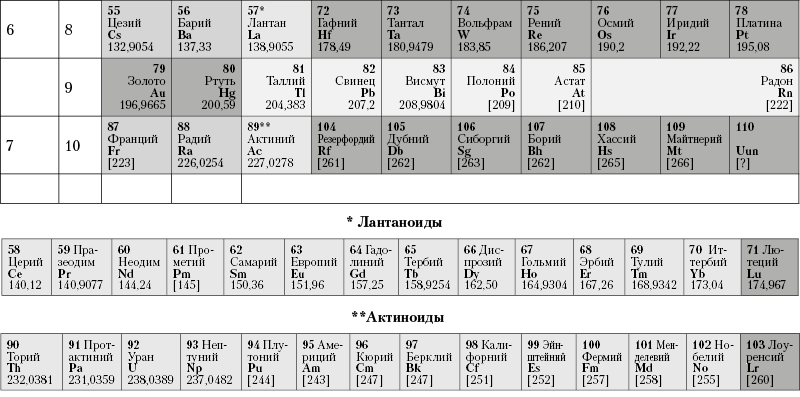
Наиболее распространенными элементами являются: О, Si, Al, Fe, Ca, Na, К, Mg, Ti, H и С. На долю всех остальных элементов, встречающихся в земной коре, приходится всего лишь несколько десятых процента (по весу). Подавляющее большинство этих элементов в земной коре присутствует почти исключительно в виде химических соединений. К числу элементов, встречающихся в самородном виде, относятся очень немногие. Те и другие возникают в результате химических реакций, которые протекают в земной коре при различных геологических процессах, приводящих к образованию самых разнообразных по составу массивов горных пород и месторождений полезных ископаемых.
Если главнейшие элементы расположить в порядке их процентного (весового) содержания в земной коре на группы по декадам 1 , то получится такая картина (табл. 3).
Таблица 3. Средний химический состав литосферы в вес. %
(по А. П. Виноградову, 1949, с уточнениями)*
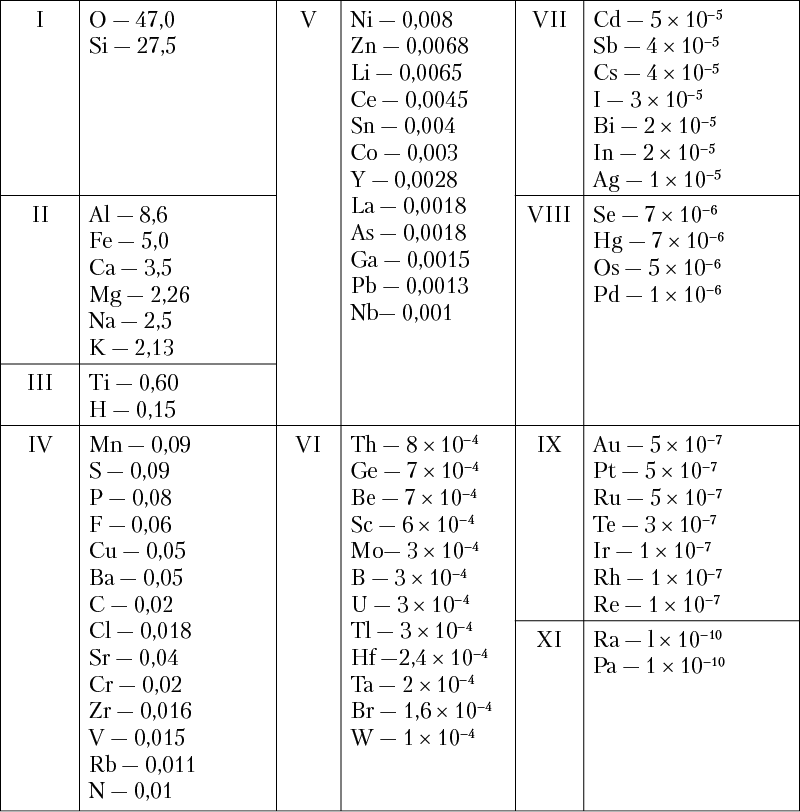
* В таблице приведены не все элементы из группы редких земель, а также благородные газы, количественные определения которых ненадежны. Данные для первых восьми элементов, а также для серы исправлены согласно последним указаниям А. П. Виноградова.
Из таблицы 3 видно, что подавляющая масса минералов земной коры должна представлять соединения элементов первых двух декад, на долю которых в весовом выражении приходится основная масса. В самом деле, в земной коре чрезвычайно широко распространены кислородные соединения кремния, алюминия, железа, а также щелочноземельных и щелочных металлов — кальция, магния, натрия и калия. К их числу относятся главным образом окислы и кислородные соли (преимущественно силикаты, алюмосиликаты, карбонаты, сульфаты и др.), входящие в состав различных горных пород, слагающих земную кору.
Кларки тяжелых металлов, играющих большую роль в промышленности, в подавляющем большинстве выражаются ничтожными величинами и попадают в последние столбцы элементов, разбитых на декады по степени распространения (табл. 4).
Таблица 4. Распространенность главных металлов в земной коре
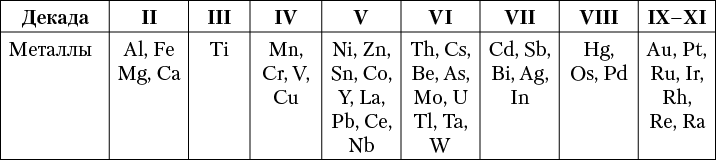
Некоторые особенности распределения тяжелых металлов в земной коре
Многие из указанных редких в земной коре элементов под влиянием совершающихся в природе геохимических процессов нередко образуют исключительно богатые скопления минерального вещества, носящие название рудных месторождений. Если бы не существовало процессов, приводящих к образованию таких месторождений, которые имело бы смысл разрабатывать с целью извлечения ценных для промышленности металлов, то можно с уверенностью сказать, что не было бы и столь мощного развития техники и культуры, какое наблюдается в настоящее время.
Тогда многие металлы, извлеченные из пород в лабораторных условиях, являлись бы исключительно дорогими. Весьма характерно, что кларки таких металлов, как ванадий, цезий, галлий и др., во много раз выше кларков ртути, висмута, серебра, золота и др. Но, несмотря на их весьма ценные свойства, они не распространены в человеческом быту, так как их месторождения с промышленными концентрациями в природе крайне редки.
Природные соединения тяжелых металлов представляют собой в основном сравнительно простые соединения. Часть этих элементов (Fe, Mn, Sn, Сr, W, Nb, Та, Th, U) преимущественно распространена в виде кислородных соединений, но зато многие другие элементы (Fe, Ni, Co, Zn, Cu, Pb, Hg, Mo, Bi, As, Sb, Ag и пр.) встречаются главным образом в виде скоплений сернистых, мышьяковистых и сурьмянистых соединений. Железо совмещает в себе свойства сидерофильных, литофильных и халькофильных элементов, обладая заметным сродством как с кислородом, так и с серой.
На диаграмме (рис. 4) по оси абсцисс расположены порядковые номера химических элементов, а по оси ординат — логарифмы их атомных кларков. Можно видеть, что с увеличением порядкового номера кривые кларков как четных, так и нечетных элементов в общем обнаруживают тенденцию к понижению. Это означает, что для большинства химических элементов имеет место обратно пропорциональная зависимость их среднего содержания в земной коре от порядкового номера, хотя встречаются и исключения (например, для Li, Be, В и др.).
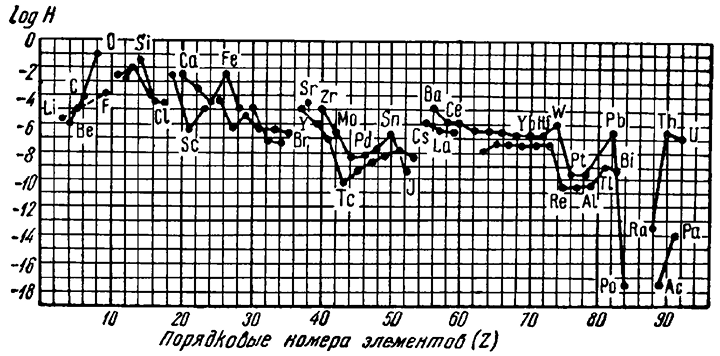
Рис. 4. Распространенность элементов в верхней части литосферы. На диаграмме даны логарифмы атомных кларков (H) как функция порядкового номера (Z), причем кислород принят за единицу
Если сравнить распространенность химических элементов в земной коре в атомных кларках с числами минералов, в которые они входят (табл. 5), то, как указал П. П. Пилипенко, между ними, за небольшим исключением, устанавливается некоторая прямая (симбатная) зависимость. Это имеет место преимущественно для элементов, обладающих малым атомным весом 2 .
Таблица 5. Взаимосвязь числа минералов
легких элементов и их атомных кларков
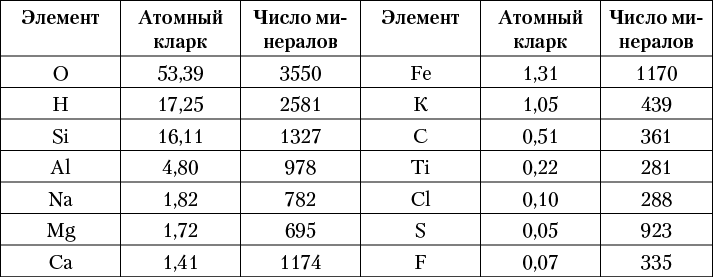
Некоторые из легких элементов играют особую роль в минералах, являясь типичными анионами или анионообразователями. Среди таких элементов прежде всего можно отметить кислород, а также водород (как компонент гидроксильного иона), серу, углерод и некоторые другие. Так как подавляющее большинство минералов являются полярными соединениями, в составе каждого из них должны присутствовать элементы, играющие роль катионов и анионов. Типичных анионов и анионообразователей среди элементов периодической системы гораздо меньше, чем катионообразующих элементов, поскольку металлы составляют около 3 / 4 всех элементов. По этой причине каждый из немногих элементов-анионообразователей будет представлен в относительно большем числе минералов по сравнению с элементами, атомы которых играют роль катионов. Этим объясняется столь значительное количество минералов — кислородных соединений, а также водосодержащих минералов и сульфидов. Для большинства распространенных элементов-металлов (главным образом легких и средних атомных весов) число минеральных видов проявляет устойчивую пропорциональность их атомным кларкам.
Для многих тяжелых металлов подобная зависимость не устанавливается. Так, теллур, атомный кларк которого в земной коре примерно в 40 раз меньше, чем кларк селена, в природных условиях образует около 150 самостоятельных минералов, в то время как для селена их известно всего около 100, и то главным образом в ассоциации с серой. Для цинка с атомным кларком в 17 раз большим по сравнению с кларком свинца мы имеем около 250 минералов, тогда как для свинца — около 450, и т. д.
Указанные различия, несомненно, вызываются химическими свойствами самих элементов, обусловленными строением их ионов и определяемыми положением этих элементов в периодической системе Менделеева. Для элементов с одинаковыми свойствами, аналогичными строением и размерами ионов, но с различными концентрациями в данном растворе или расплаве естественно ожидать, что при кристаллизации элементы с меньшей концентрацией будут входить в кристаллические структуры, образуемые господствующими элементами, как бы растворяясь в них. Если же данный элемент в окружающей среде не находит аналогичных себе по размерам и строению ионов других элементов, то в каком бы количестве он ни присутствовал в растворе при кристаллизации, он должен образовать самостоятельное соединение. Весьма показательно, что двухвалентный марганец в главной своей массе входит в состав минералов в виде изоморфной примеси к двухвалентным железу и кальцию, но зато четырехвалентный марганец всегда образует явно индивидуализированные соединения. Этим же объясняется то, что такие элементы, как рубидий, скандий, гафний, индий, рений и др., обладающие низкими атомными кларками, в природе образуют лишь несколько самостоятельных минералов, преимущественно же находятся в рассеянном состоянии, присутствуя в виде изоморфной примеси к другим элементам. В значительной мере это относится и к таким более распространенным элементам, как селен, ванадий, цезий, кадмий и др. Наоборот, элементы с очень низкими атомными кларками — теллур, золото, группа платиновых металлов, висмут и др. — сравнительно часто устанавливаются в виде самостоятельных минералов.
1 От греч. дека — десять.
2 В число минералов не включены лишь разновидности, в которые данный элемент входит в виде изоморфной примеси.
Время работы: с 10:00 до 21:00,
Выходной день: вторник
«Ретро-кафе»: в дни работы Планетария с 10:00 до 20:00.
Элементы: Железо - главный металл природы
Железо – один из самых распространённых элементов в Солнечной системе, особенно на Земле. Его среднее содержание в земной коре составляет 4,7 % по массе, уступая по этому показателю кислороду, кремнию и алюминию. Но в пересчёте на Землю в целом железо занимает едва ли не первое место, так как в мантии его содержание составляет 14%, в ядре – 86 % , а доля железного ядра составляет около 30 % от массы нашей планеты. В ядрах планет земной группы его содержание, по некоторым оценкам, составляет 90 %. Поэтому без преувеличения можно сказать, что по значимости для планет земной группы - это элемент номер один!

Железные ядра планет земной группы
В чистом виде железо встречается только в метеоритах, но почти всегда с незначительными примесями кобальта и никеля. По одной из версий слово «железо» заимствовано из праславянского языка и родственно слову «желвак», т.е. округлый камень, окатыш. В таблице Менделеева этот элемент занимает клетку №26 и обозначается символом Fe - от латинского Ferrum (железо).
Вероятно, первое железо, которое попало в руки человеку, было метеоритное, так как отдельные железные предметы были известны уже в бронзовом веке. Поэтому, определить чёткую границу перехода от бронзового века к железному - периоду, когда люди осваивали производство железа из железных руд, представляется затруднительным. По некоторым данным это происходило примерно с 1200 года до н.э. до первых столетий н.э.
Природное железо состоит из четырёх стабильных изотопов: 54 Fe , 56 Fe, 57 Fe и 58 Fe, где доля 56 Fe составляет 91 %.Также известно более 20 нестабильных изотопов железа с массовыми числами от 45 до 72. Большинство учёных считают, что железом оканчивается ряд синтеза элементов в ядрах нормальных звёзд, а все последующие элементы могут образоваться только в результате взрывов сверхновых.
Известно большое количество минералов содержащих железо, но главными минералами на железо-рудных месторождениях являются: магнетит (FeO · Fe2O3); гематит Fe2O3); гётит FeO(OH); гидрогётит FeOOH·nH2O.

Кристаллы гётита, 4 см. Урал, Россия.
В земной коре также широко распространены сульфиды железа – пирит (FeS2), карбонаты железа – сидерит (FeCO3), фосфаты железа - вивианит (Fe3(PO4)2·8H2O). По запасам железных руд Россия занимает первое место в мире.

Кристаллы магнетита, 5 см. Ковдорское месторождение, Кольский п-ов, Россияю
Понимая важнейшую роль железа в жизни планеты, академик А.Е. Ферсман ещё в 1930-х годах писал: «Железо не только основа всего мира, самый главный металл окружающей нас природы, оно основа культуры и промышленности, оно орудие войны и мирного труда. И трудно во всей таблице Менделеева найти другой такой элемент, который был бы так связан с прошлыми, настоящими и будущими судьбами человечества».
Самые распространённые элементы в земной коре

Кора — это самый внешний слой планеты. Земля состоит из ряда различных элементов, но кора составляет только 1% объема Земли в тонком внешнем слое, который охватывает другие части внутренней планеты, включая мантию, внешнее ядро и внутреннее ядро. Земная кора имеет глубину 40 км и состоит из твердых пород и минералов, которые охлаждались и затвердевали, когда Земля была молодой. В коре можно найти много разных элементов. 10 наиболее распространенных элементов в земной коре в процентах от содержания упомянуты ниже:
10 самых распространенных элементов в земной коре
- Кислород — 46,1%
- Кремний — 28,2%
- Алюминий — 8,23%
- Железо — 5,63%
- Кальций — 4,15%
- Натрий — 2,36%
- Магний — 2,33%
- Калий — 2,09%
- Титан — 0,565%
- Водород — 0,140%

1. Кислород (O)
Один из наиболее заметных и важных элементов, составляющих земную кору, — это кислород. Кислород — самый распространенный элемент в земной коре, 461 000 частей на миллион. Это означает, что он составляет примерно 46% земной коры. Во Вселенной в целом Кислород занимает третье место по распространенности. Кислород составляет 21% атмосферы Земли и 90% массы воды. Это, возможно, самый важный элемент для жизни на Земле, и действительно, он составляет примерно две трети компонентов человеческого тела. Кислород — это элемент с высокой реакционной способностью, который также легко соединяется с другими элементами. Из-за этого кислород содержится в большом количестве обычных соединений как на Земле, так и, в частности, в коре. В земной коре очень много силиката, который образован из кремния и кислорода. Кислород также соединяется с железом, образуя железную руду и различные соединения железа, которые составляют большую часть земной коры. Жидкий кислород легко воспламеняется и используется в качестве топлива, в то время как кислород и ацетилен создают пламя, достаточно горячее для сварки и плавления металла. Более того, большая часть органической жизни на Земле нуждается в кислороде для выживания. Это один из основных компонентов большинства живых существ.
2. Кремний (Si)
Как упоминалось в случае силиката, кремний также является важным элементом земной коры. Он составляет около 28% и может быть обнаружен в самых разных минералах и элементарных соединениях, обычно в сочетании с кислородом. Диоксид кремния — одно из наиболее распространенных соединений, состоящее из кремния и кислорода. Диоксид кремния является основным компонентом многих типов твердых кристаллических пород, таких как кварц, аметист, опал и горный хрусталь. Диоксид кремния — это также то, из чего состоит большая часть песка, и большая часть причины, по которой он так часто встречается в земной коре. Песок в основном состоит из минералов и горных пород на основе кремния. Кремний также используется в различных изделиях, созданных человеком, таких как большая часть электроники и микрочипов, а также стекло и кирпич.
3. Алюминий (Al)
Алюминий, третий в списке самых распространенных элементов, составляет примерно 8% земной коры и на самом деле является самым распространенным металлом в коре. Хотя это наиболее часто встречающийся металл, он всегда находится в сложной форме. Наиболее часто встречающиеся соединения — это сульфат алюминия, калия и оксид алюминия.
4. Железо (Fe)
Примерно 5% земной коры состоит из железа. Железо — очень важный элемент на Земле, и на самом деле оно составляет большую часть ядра Земли. Кроме того, из-за своего изобилия оно использовалось людьми в течение тысяч лет, что даже позволяет назвать эпоху железного века. Хотя человечество сильно развилось со времен железного века, железо по-прежнему широко используется в наше время. Из железа и углерода получается сталь — один из наиболее часто используемых металлов во всем, от небольших предметов домашнего обихода до мостов и зданий. Железо также важно для органической жизни. Это ключевая часть человеческой крови и компонент хлорофилла растений.
5. Кальций (Ca)
Кальций составляет около 4% земной коры. Хотя кальций обычно связан с ростом человека в отношении костей и развития, кальций также легко обнаруживается на Земле в различных сложных формах и часто встречается в сочетании с кислородом или водой. Карбонат кальция также является обычным соединением, и его можно найти в различных типах горных пород, таких как мрамор, мел и известняк, а также в ракушках и жемчуге.
6. Натрий (Na)
Натрий, составляющий примерно 2,3% земной коры, занимает 6-е место в списке самых распространенных элементов. Как и многие другие элементы в этом списке, он никогда не бывает свободным в природе, а находится в сложной форме. В изолированной форме он также является высокореактивным элементом. Для человека натрий чаще всего ассоциируется с каменной солью — хлоридом натрия. Поскольку натрий очень хорошо растворим в воде, он является одним из наиболее распространенных растворенных элементов, обнаруживаемых в океане, и действительно, в соленых водоемах часто образуются хлорид натрия или отложения соли, особенно там, где водоем высох. Натрий также является важным элементом для животных и людей и помогает органической жизни поддерживать адекватный баланс жидкости, который, в свою очередь, влияет на нервы и мышечные волокна.
7. Магний (Mg)
Магний является седьмым по распространенности элементом земной коры с содержанием около 2%. Металл встречается не как свободный элемент, а в сочетании с другими элементами, такими как кислород, кальций и углерод. Доломит — пример минерала, содержащего магний.
8. Калий (К)
Примерно 2% земной коры составляет калий. Это не элемент, который встречается в природе в своей одиночной форме, а входит в состав ряда соединений, свободно обнаруживаемых на Земле. Его чистая форма очень реактивна как по отношению к кислороду, так и к водороду, что означает, что он может воспламеняться в воде или на открытом воздухе. Наиболее распространенным соединением калия является хлорид калия, который используется в удобрениях и т.п., и карбонат калия, который используется для мыла и некоторых типов стекла.
9. Титан (Ti)
Титан содержится в таких минералах, как рутил, ильменит и сфен, которые содержатся в земной коре. При 0,6% состава земной коры он гораздо менее распространен, чем элементы, которые занимают места с первого по восьмое в списке. Тем не менее, это важный элемент, который известен как чрезвычайно прочный и очень легкий. Из-за этого люди по-разному используют его, от самолетов до искусственных суставов человека.
10. Водород (H)
Водород на самом деле является самым распространенным элементом в известной вселенной, но он занимает только десятое место по отношению к элементам в земной коре, поскольку чаще всего встречается в виде газа. Водород содержит множество соединений, которые легко найти на Земле как в природе, так и в антропогенных целях. Водород, конечно, является ключевым компонентом воды, H2O, но также входит в общие соединения аммиака, метана, перекиси водорода и даже сахара, которые легко используются людьми.
Самый распространенный металл в земной коре. Металлы в природе
Металлы представляют собой группу элементов, которые обладают такими уникальными свойствами, как электропроводность, высокая теплопередача, положительный коэффициент сопротивления, характерный блеск и относительная пластичность. Данный вид веществ является простым по химическим соединениям.
Классификация по группам
Металлы относятся к самым распространенным материалам, которые используются человечеством на протяжении всей его истории. Большинство из них находится в средних слоях земной коры, но есть и те, что спрятаны глубоко в горных залежах.
На данный момент металлы занимают большую часть таблицы Менделеева (94 из 118 элементов). Из официально признанных стоит отметить следующие группы:
1. Щелочные (литий, калий, натрий, франций, цезий, рубидий). При контакте с водой они образуют гидроксиды.
2. Щелочноземельные (кальций, барий, стронций, радий). Отличаются плотностью и твердостью.

3. Легкие (алюминий, свинец, цинк, галлий, кадмий, олово, ртуть). Из-за незначительной плотности часто используются в сплавах.
4. Переходные (уран, золото, титан, медь, серебро, никель, железо, кобальт, платина, палладий и пр.). Обладают изменчивой степенью окисления.
5. Полуметаллы (германий, кремний, сурьма, бор, полоний и др.). В своей структуре имеют кристаллическую ковалентную решетку.
6. Актиноиды (америций, торий, актиний, берклий, кюрий, фермий и пр.).
7. Лантаноиды (гадолиний, самарий, церий, неодим, лютеций, лантан, эрбий и др.).
Стоит отметить, что есть металлы в земной коре и такие, которые не определены в группы. К ним относят магний и бериллий.
Самородные соединения
В природе существует отдельный класс кристаллохимической кодификации. К таким элементам относят самородные металлы. Это минералы по составу между собой не связанные. Чаще всего самородные металлы в природе образуются в результате геологических процессов.

В кристаллическом состоянии в земной коре известны 45 веществ. Большинство из них в природе встречается крайне редко, отсюда и их высокая стоимость. Доля таких элементов составляет всего 0,1 %. Стоит отметить, что нахождение этих металлов также является трудоемким и недешевым процессом. Он основывается на использовании атомов с устойчивыми оболочками и электронами.
Самородные металлы называются также благородными. Для них характерны химическая инерция и устойчивость соединений. К таковым относят золото, палладий, платину, иридий, серебро, рутений и пр. Чаще всего в природе встречается медь. Железо в самородном состоянии присутствует в основном в горных залежах в виде метеоритов. Самыми редкими элементами группы являются свинец, хром, цинк, индий и кадмий.
Основные свойства
Практически все металлы в нормальных условиях отличается твердостью и стойкостью. Исключение - франций и ртуть, щелочные металлы. Температура плавления для всех элементов группы разная. Ее диапазон колеблется от -39 до +3410 градусов по Цельсию. Самым устойчивым к плавлению считается вольфрам. Его соединения теряют стойкость только при температуре выше +3400 С. Из легкорасплавляемых металлов следует выделить свинец и олово.

Также элементы делятся относительно плотности (легкие и тяжелые) и пластичности (твердые и мягкие). Все металлические соединения отлично проводят ток. Данное свойство обуславливается наличием кристаллических решеток с активными электронами. Максимальную проводимость имеют медь, серебро и алюминий, чуть меньшую – натрий. Стоит отметить и высокие термические свойства металлов. Наилучшим теплопроводником считается серебро, наихудшим – ртуть.
Металлы в окружающей среде
Чаще всего такие элементы можно встретить в виде соединений и руд. Металлы в природе образуют сульфиты, оксиды, карбонаты. Для очищения соединений сперва необходимо выделить их из состава руды. Следующим шагом будет легирование и финальная обработка.
В промышленной металлургии различаются черные и цветные руды. Первые строятся на основе железных соединений, вторые – на прочих металлах. Драгоценными металлами считаются платина, золото и серебро. Большая их часть находится в земной коре. Тем не менее, малая доля приходится и на морскую воду.
Есть благородные элементы даже в живых организмах. В человеке содержится около 3 % металлических соединений. По большей степени в организме находятся натрий и кальций, которые выступают в роли межклеточного электролита. Магний необходим для нормальной работы ЦНС и мышечной массы, железо полезно для крови, медь – для печени.
Нахождение металлических соединений
Большинство элементов располагается под верхним слоем грунта повсеместно. Самый распространенный металл в земной коре – это алюминий. Его процентное содержание варьируется в пределах 8,2 %. Найти самый распространенный металл в земной коре несложно, так как он встречается в виде руд.
Железо и кальций в природе встречают чуть реже. Их процентное содержание равно 4,1 %. Далее идут магний и натрий – по 2,3 %, калий – 2,1 %. Остальные металлы в природе занимают не более 0,6 %. Примечательно, что магний и натрий в равной степени можно добывать как в земле, так и в морской воде.

Металлические элементы в природе встречаются в виде руд или в самородном состоянии, как медь или золото. Есть вещества, которые нужно получать из оксидов и сульфидов, например, гематит, каолин, магнетит, галенит и пр.
Производство металлов
Процедура добычи элементов сводится к извлечению полезных ископаемых. Нахождение металлов в природе в виде руд является самым простым и распространенным процессом в широкой промышленности. Для поиска кристаллических залежей используется специальное геологическое оборудование, анализирующее состав веществ на конкретном участке земли. Реже нахождение металлов в природе сводится к банальному открыто-подземному методу.
После добычи наступает этап обогащения, когда из исходного минерала выделяется рудный концентрат. Для отличия элементов используют смачивание, электрический ток, химические реакции, термообработку. Чаще всего выделение металлический руды происходит в результате плавления, то есть разогрева с восстановлением.
Добыча алюминия
Данным процессом занимается цветная металлургия. По масштабам потребления и производства она является лидером среди прочих отраслей тяжелой промышленности. Самый распространенный металл в земной коре очень востребован в современном мире. По объему производства алюминий уступает только стали.

Больше всего данный элемент используется в авиационной, автомобильной и электротехнической промышленности. Примечательно, что самый распространенный металл в земной коре можно получить и «искусственным» путем. Для такой химической реакции потребуются бокситы. Из них формируется глинозем. При соединении этого вещества с угольными электродами и фтористой солью под действием электрического тока можно получить чистейшую алюминиевую руду.
Страной-лидером среди производителей данного компонента является Китай. В год там выплавляется до 18,5 млн тонн металла. Компанией-лидером в аналогичном рейтинге по добыче алюминия является российско-швейцарское объединение UC RUSAL.
Применение металлов
Все элементы группы отличаются прочностью, непроницаемостью и относительной устойчивостью к температурному воздействию. Именно поэтому металлы столь распространены в повседневной жизни. Сегодня из них делают электрические провода, резисторы, технику, предметы обихода.
Металлы являются идеальным конструкционными и инструментальными материалами. В строительстве используют чистые и комбинированные сплавы. В машиностроении и авиации главными соединениями являются сталь и более твердые связи.
Читайте также:
