Металлы и неметаллы в жизни человека
Неметаллы – это химические элементы, которые образуют в свободном состоянии простые вещества, не обладающие физическими и химическими свойствам металлов.
Это 22 элемента Переодической системы: бор B, углерод C, кремний Si, азот N, фосфор P, мышьяк As, кислород O, сера S, селен Se, теллур Te, водород H, фтор F, хлор Cl, бром Br, йод I, астат At; а так же благородные газы: гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe, радон Rn.
Физические свойства
Элементы-неметаллы образуют простые вещества, которые при обычных условиях существуют в разных агрегатных состояниях:
· газы (благородные газы: He, Ne, Ar, Kr, Xe, Rn;водород H2, кислород O2, азот N2, фтор F2, хлор Cl2.),
· жидкость (бром Br2) ,
· твердые вещества ( йод I2, углерод C, кремний Si, сера S, фосфор P и др. ) .
Атомы неметаллов образуют менее плотно упакованную структуру чем металлы, в которой между атомами существуют ковалентные связи. В кристаллической решетке неметаллов, как правило, нет свободных электронов. В связи с этим твердые вещества-неметаллы в отличие от металлов плохо проводят тепло и электричество, не обладают пластичностью.
Получение неметаллов
Способы получения неметаллов отличаются многообразием и специфичностью, общих подходов не существует. Рассмотрим основные способы получения некоторых неметаллов.
1. Получение галогенов. Самые активные галогены – фтор и хлор – получают электролизом. Фтор – электролизом расплава KHF2, хлор – электролизом расплава или раствора хлорида натрия:
Другие галогены можно также получить электролизом или вытеснением из их солей в растворе с помощью более активного галогена:
2. Получение водорода. Основной промышленный способ получения водорода – конверсия метана (каталитический процесс):
3. Получение кремния. Кремний получают восстановлением коксом из кремнезема:
SiO2 + 2C = Si + 2CO.
4. Получение фосфора. Фосфор получают восстановлением из фосфата кальция, который входит в состав апатита и фосфорита:
5. Кислород и азот получают фракционной перегонкой жидкого воздуха.
6. Сера и углерод встречаются в природе в самородном виде.
7. Селен и теллур получают из отходов производства серной кислоты, так как эти элементы встречаются в природе вместе с соединениями серы.
8. Мышьяк получают из мышьяковистого колчедана по сложной схеме превращений, включающей стадии получения оксида и восстановления из оксида углеродом.
9. Бор получают восстановлением оксида бора магнием.
Химические свойства
1. Окислительные свойства неметаллов проявляются при взаимодействии с металлами
4Al + 3C = Al4C3
2. Неметаллы играют роль окислителя при взаимодействии с водородом
H2 + F2 = 2HF
3 Любой неметалл выступает в роли окислителя в реакциях с теми металлами, которые имеют низкую ЭО
2P + 5S = P2S5
4. Окислительные свойства проявляются в реакциях с некоторыми сложными веществами
CH4 + 2O2 = CO2 + 2H2O
5. Неметаллы могут играть роль окислителя в реакциях со сложными веществами
2FeCl2 + Cl2 = 2FeCl3
6. Все неметаллы выступают в роли восстановителей при взаимодействии с кислородом
4P + 5O2 = 2P2O5
7. Многие неметаллы выступают в роли восстановителей в реакциях со сложными веществами-окислителями
S + 6HNO3 = H2SO4 + 6NO2 + 2H2O
8. Наиболее сильные восстановительные свойства имеют углерод и водород
ZnO + C = Zn + CO;
CuO + H2 = Cu + H2O
9. Существуют и такие реакции, в которых один и тот же неметалл является одновременно и окислителем, и восстановителем. Это реакции самоокисления-самовосстановления (диспропорционирования)
Cl2 + H2O =HCl + HClO
Применение неметаллов
· Водород используется в химической промышленности для синтеза аммиака, хлороводорода и метанола, применяется для гидрогенизации жиров. Используется в качестве восстановителя при производстве многих металлов, например, молибдена и вольфрама, из их соединений.
· Хлор применяют для производства соляной кислоты, винилхлорида, каучука и многих органических веществ и пластмасс, в текстильной и бумажной промышленности используют в качестве отбеливающего средства, в быту – для обеззараживания питьевой воды.
· Бром и йод используют в синтезе полимерных материалов, для приготовления лекарственных препаратов и др.
· Кислород применяется при сжигании топлива, при выплавке чугуна и стали, для сварки металлов, необходим для жизнедеятельности организмов.
· Сера используется для производства серной кислоты, изготовления спичек, пороха, для борьбы с вредителями сельского хозяйства и лечения некоторых болезней, в производстве красителей, взрывчатых веществ, люминофоров.
· Азот и фосфор применяются при производстве минеральных удобрений, азот применяется при синтезе аммиака, для создания инертной атмосферы в лампах, используется в медицине. Фосфор применяется при производстве фосфорной кислоты.
· Алмаз используется при обработке твердых изделий, в буровых работах и ювелирном деле, графит – для изготовления электродов, тиглей для выплавки металлов, в производстве карандашей, резины и др.
Металлы и неметаллы в жизни человека
На грани химии, биологии и медицины возникла новая научная область бионеорганическая химия. Бионеорганическая химия рассматривает роль металлов в возникновении и развитие различных процессов в здоровом и больном организме, создает новые эффективные препараты на основе металлорганических соединений, активно участвует в борьбе за сохранение здоровья людей и продление человеческой жизни. Особенно чутко организм реагирует на изменение концентрации микроэлементов, т.е. элементов, участвующих в организме в количестве меньше одного грамма на 70 килограмм массы человеческого тела. К таким элементам относятся медь, цинк, марганец, кобальт, железо, никель, молибден и другие.
Файлы: 1 файл
МЕТАЛЛЫ И НЕМЕТАЛЛЫ В ЖИЗНИ ЧЕЛОВЕКА.doc
МЕТАЛЛЫ И НЕМЕТАЛЛЫ В ЖИЗНИ ЧЕЛОВЕКА
На грани химии, биологии и медицины возникла новая научная область бионеорганическая химия. Бионеорганическая химия рассматривает роль металлов в возникновении и развитие различных процессов в здоровом и больном организме, создает новые эффективные препараты на основе металлорганических соединений, активно участвует в борьбе за сохранение здоровья людей и продление человеческой жизни. Особенно чутко организм реагирует на изменение концентрации микроэлементов, т.е. элементов, участвующих в организме в количестве меньше одного грамма на 70 килограмм массы человеческого тела. К таким элементам относятся медь, цинк, марганец, кобальт, железо, никель, молибден и другие.
Вода – универсальный растворитель. Она носит в себе следы всего, с чем соприкасается. Известно около 70 000 веществ, которые встречаются в воде в качестве примесей. Некоторые из этих примесей оказывают вредное влияние на человеческий организм, превышения их предельно допустимой концентрации (ПДК) нужно всячески избегать.
В старых зданиях иногда встречаются свинцовые водопроводные трубы. Некоторые американские токсикологи считают, что свинцовый водопровод Римской империи послужил причиной ее падения. Свинцовый водопровод был в Московском Кремле во времена правления Ивана Грозного. Вода, текущая из таких труб, становится опасной для жизни, поскольку свинец – токсичный металл. Он откладывается в костях скелета и влияет на центральную и периферическую нервную систему. Это особенно опасно для детей младше 6 лет, включая период внутриутробного развития. Есть данные о том, что свинец способствует развитию новообразований в почках. Помимо этого, свинец угнетает иммунитет. Использование этилированного бензина в качестве топлива приводит к загрязнению окружающей среды свинцом.
Ртуть – уникальный металл. Это единственный металл-жидкость, который может испаряться. Существуют микроорганизмы, способные включать ртуть в органические соединения. В природе ртуть бывает в самородном, жидком виде, а также входит в состав минералов. Некоторая часть ртути свободно испаряется из трещин в земной коре. Около половины всей используемой ртути приходится на батарейки, люминесцентные лампы, выключатели и измерительные приборы.
Ртуть и ее соединения нарушают белковый обмен, поражают нервную систему, печень, почки, желудочно-кишечный тракт, при вдыхании – дыхательные пути. Особенно опасны выбросы в воду с образованием метилртути – соединения более опасного, чем сама ртуть. Оно способно накапливаться в организме и вызывать болезнь Минамата. Болезнь так названа по названию озера Минамата в Японии, куда промышленная компания долгое время сливала ртуть. Болезнь была обнаружена в 1956 году. Ее симптомы – нарушение моторики, парестезия в конечностях, ослабление зрения и слуха. В тяжелых случаях – паралич.
В норме кадмий в небольших количествах присутствует в здоровом человеческом организме. Однако он токсичен, и потому его избыток легко становится губительным. Кадмий обладает способностью накапливаться, хроническое отравление приводит к анемии и болезни костей. Растворимые соединения кадмия поражают центральную нервную систему, печень и почки, нарушают фосфорно-кальциевый обмен. Кадмий изменяет на многие гормоны и ферменты, необходимые для нормальной работы организма. Источником кадмиевого загрязнения являются выбросы цветной и черной металлургии, ТЭЦ и угледобычи.
В природе цинк существует только в составе полиметаллических руд. В древней Греции был известен сплав цинка с медью – латунь. Цинк – необходимый для нормальной жизнедеятельности элемент. Однако его переизбыток вызывает поражение почек. Есть экспериментальные данные о его токсическом воздействии на кровь и сердце.
Никель участвует в регуляции обмена ДНК и является необходимым для человека микроэлементом. Недостаток его ведет к нарушению обмена веществ и снижению иммунитета. Но избыток никеля может быть вреден для здоровья. При повышении концентрации никеля в организме могут появиться аллергические реакции в виде кожной сыпи или аллергического насморка. В Германии 15% людей имеет аллергию на никель. При избытке никеля также возможна анемия, повышенная возбудимость. Поскольку никель влияет на ДНК, а также РНК, при хронической интоксикации появляется риск развития новообразований в легких, в почках, на коже. Никель могут выделять в воду электрические чайники с открытым нагревательным элементом.
Хром — это металл. Он твердый и ломкий и очень устойчив к коррозии. Он серебристо-белый, а после полировки приобретает блеск. Он плохо проводит электричество и тепло.
Ученые Национальных институтов здравоохранения США получили данные о том, что содержащийся в питьевой воде хром может вызвать рак. Были проведены лабораторные опыты над животными. Выяснилось, что, хром, который содержится в питьевой воде, может вызвать рак. Такие данные были получены в ходе лабораторных наблюдений за животными, получавшими воду с высоким содержанием хрома. У крыс появлялись злокачественные опухоли полости рта, у мышей – рак тонкой кишки. Ученые считают, что хром 6 (шестивалентный) может вызвать у людей рак легких.
Железо – важный микроэлемент, участвующий в кроветворении и внутриклеточном обмене. Железо почти всегда встречается в природной воде, как на поверхности, так и во взятой из скважины. Больше всего железа в болотных водах. В систему водоснабжения железо попадает из-за коррозии труб. Норма содержания железа в воде – не больше 0,3 мг/л. Высокое содержание железа в воде неблагоприятно для кожи. Избыток железа может изменять состав крови, вызывать аллергические реакции, железо накапливается в поджелудочной железе, почках, миокарде, иногда в щитовидной железе, мышцах и эпителии языка.
Медь – это пластичный металл с невысокой плотностью. Обладает высокой теплопроводностью.
Медь необходима для высших растений, для животных и для человека, поэтому недостаток меди нежелателен, однако в питьевой воде не должно содержаться больше меди, чем 1-1,5 мг/л. Повышение концентрации меди в питьевой воде вызывает поражение слизистых оболочек почек и печени.
Молибден входит в состав человеческого организма. Но избыток его в питьевой воде может стать причиной ослабления иммунитета, изменений функций костного мозга, тимуса и селезенки. А при наличии сопутствующего недостатка в организме кальция избыток молибдена ведет к подагре (ревматическое заболевание суставов, связанное с отложением солей, может сопровождаться опуханием и деформацией суставов).
Марганец хорошо знаком нам всем в виде марганцовки, как называют в быту перманганат калия, обладающей антисептическими свойствами. Марганец – необходимый микроэлемент, участвует в образовании костей, в кроветворении и тканевом дыхании, в жировом и углеводном обмене, поддерживает репродуктивные функции. При недостатке марганца наблюдается рвота, изменение цвета волос, замедляется сращивание костей при переломах.
Допустимое содержание марганца в водопроводной питьевой воде – 0,1 мг/л. Это больше, чем в Европе, но в пять раз меньше, чем в Америке. При повышении содержания марганца возможно развитие анемии, нарушение функционального состояния центральной нервной системы.
Название «фтор» восходит к греческому слову φθόρος («разрушение»). Фтор в своем природном виде – чрезвычайно ядовитый газ. При этом фтор – необходимый для человека микроэлемент. В организме человека фтор существует в виде соединения фторапатита и содержится в эмали зубов и костях. Если фтора в воде недостаточно (меньше 0,5 мг/л), повышается опасность кариеса.
Но избыток фтора тоже опасен. Если в воде его слишком много (более 1,0 мг/л), это приводит к флюорозу. Флюороз проявляется в виде крапинок или пятен на зубной эмали, изменяется костная ткань (остеосклероз), кости деформируются, связочный аппарат обызвествляется. Это происходит из-за того, что при избытке фтора, поступающего в организм, соли фтора начинают откладываться в костях и зубах и замещают растворимые соединения кальция нерастворимыми соединениями кальция и фтора. Особенно опасен избыток фтора для детей, у которых коренные зубы еще находятся в стадии формирования. При небольшом превышении нормы фтора поражаются только резцы, при большом – все зубы. Поражение костей происходит при сильном переизбытке фтора – свыше 6 мг/л. Хорошая же новость заключается в том, что если уменьшить поступление фтора в организм, симптомы флюороза уменьшаются.
Если ртуть – единственный жидкий металл, то бром – единственный жидкий неметалл. В простом виде это – ядовитая красно-бурая жидкость с неприятным запахом. Бром широко распространен в природе в виде соединений. В организме человека бром содержится в количестве примерно 0,2 г. Он обнаруживается в жидкостях организма: крови, слюне и моче, а также в печени и в мозге.
Препараты брома оказывают снотворное и успокаивающее действие.
Избыточное содержание микроэлемента бром в организме может привести к кожному заболеванию – бромодерме (высыпания на коже в виде бляшек или пузырей), а также нарушить работу нервной системы. Недостаток брома способствует возникновению бессонницы, к снижению уровня роста эритроцитов в крови.
Источником поступления бромидов могут быть грунтовые или подземные воды либо сточные воды предприятий химической промышленности.
Йод не нуждается в представлении. Название его на греческом языке (ιώδης) значит «фиолетовый». В нормальном виде представляет собой кристаллы черного цвета с фиолетовым металлическим отливом. В природе изредка встречается в виде минерала, но такие находки можно по пальцам пересчитать – в термальных источниках Везувия и на итальянском острове с красивым названием Вулькано. Йод находится в большом количестве в морской воде в виде иодидов (буква «и» в начале этого слова не ошибка, «йод» - это бытовое название, а «официально» в таблице Менделеева этот элемент называется именно так – «иод»).
Йод – необходимый микроэлемент, он присутствует во всех живых организмах. У животных и человека йод входит в состав вырабатываемых щитовидной железой гормонов, которые регулируют развитие организма и обмен веществ. Дефицит йода опасен, в результате могут развиться такие заболевания, как эндемический зоб, кретинизм и гипотиреоз. В организме человека содержится 12-20 мг йода, суточная потребность в йоде составляет около 0,2 мг.
Йод токсичен. Смертельная доза – 2-3 г. Избыток йода вызывает поражение почек и сердечнососудистой системы, появляется общая слабость, головная боль, рвота, понос, бурый налет на языке, боли в сердце и учащение пульса.
Ветер со стороны моря и испарения приносят в атмосферу некоторое количество йода, которое затем захватывается дождем и вместе с ним попадает в поверхностные воды. Также йод выщелачивается природными водами из магматических пород. Третий источник йода – воды нефтяных месторождений и сточные воды химической и фармацевтической промышленности.
Бор мы все знаем «в лицо» благодаря одному из его соединений – борной кислоте, которая применяется в медицине как дезинфицирующее средство и входит в состав некоторых лекарств. В свободном состоянии бор – бесцветное, серое или красное кристаллическое или аморфное вещество. Роль бора в организме человека мало изучена. Бор обнаружен в костной ткани, в мышцах и в крови. Основной источник бора – пища, с нею человек ежедневно получает 1-3 мг этого элемента. Безопасная доза для взрослого человека составляет 13 мг.
Соединения бора использовались не так давно как средства для снижения веса, однако обнаружилось, что вес снижался вследствие вызванного бором обезвоживания клеток, что вредно для организма. Борные соединения быстро всасываются, но медленно выделяются из организма. Таким образом, бор накапливается и в результате возможна борная интоксикация, которая проявляется рвотой, водянистым стулом, потерей аппетита и «борным псориазом» – кожной сыпью с упорным шелушением. Также известен борный энтерит – нарушение процессов пищеварения при длительном воздействии соединений бора.
В природные воды бор поступает из подземных вод, обогащенных бором за счет содержащих бор осадочно-метаморфических пород (борацит, бура, колеманит и др.). Также насыщены бором сточные воды некоторых производств (например, кожевенного, керамического) и бытовые сточные воды со стиральными порошками. Бор содержится в некоторых удобрениях и может попадать в воду из почв.
Лекция на тему :«Важнейшие соединения металлов и неметаллов в природе и хозяйственной деятельности человека»
В организме человека находятся 81 химический элемент из 92, встречающихся в природе. Организм человека состоит на 60% из воды, 34% приходится на органические вещества и 6% - на неорганические.
Человеческий организм - сложная химическая лаборатория. Трудно себе представить, но ежедневно наше самочувствие, настроение и даже аппетит могут зависеть от минеральных веществ. Без них бесполезными оказываются витамины, невозможны синтез и распад белков, жиров и углеводов.
Например, если вес человека составляет 70 кг, то в нем содержится (в граммах): кальция - 1700, калия - 250, натрия - 70, магния - 42, железа - 5, цинка - 3.
Очевидно, что металлы необходимы клеткам тела человека для нормальной жизнедеятельности. Как избыток, так и недостаток металлов оказывает отрицательное влияние на организм, а некоторые металлы могут оказывать на него токсичное действие.
Роль химических элементов.
Земную кору составляют сравнительно небольшое число химических элементов. Около ½ масса земной коры приходится на кислород. Более ¼ - на кремний. Всего 18 элементов; O, Si, AL , Fe , Ca , K , Mg , H , Ti , C , Cv , P , U , Mn , F , Ba , Na , K составляют 99,8% массы земной коры. Из них на 8 элементов приходится 98% - это O, Si, AL , Fe , Ca , K , Mg , Na . Тогда как в живых организмах 6 элементов – это O, S, C , P , Н, N на их долю приходится 97,4% массы организмов. Эти элементы называют органогенами.
С химической точки зрения отбор элементов при формировании организма сводится к отбору тех из них, которые способны к образованию прочных, но в то же время и лабильных связей. Эти связи должны легко подвергаться как гомолитическому (О2 --- О + О ) так и гетеролитическому (Н2О == О +2Н ) разрыву, а также циклизации (6 С --О). Именно поэтому органоген №1 в живой материи – это углерод. Атомы кислорода и водорода гораздо менее лабильны, но и они образуют устойчивую среду для соединений остальных элементов – это воду, тем самым обеспечивают протекание окислительно-восстановительных процессов. Атомы неметаллов (N,P,S) и металлов (Fe, Cu, Mg ) отличаются особой лабильностью в образовании различных химических связей. Такие как Si и AL составляющие большую часть земной коры в живых организмах играют второстепенную роль. Теперь дадим им характеристику.
Значение металлов в живых организмах?
Железо. Содержание его в организме. Он входит в состав гемоглобина, является кофактором каталозы – фермента разрушающего пероксид водорода и оберегающего клетки от его повреждающего действия. При недостатке железа нарушается азотистый, жировой и жировой обмен, развивается анемия. У растений заболевание хлороз – обесцвечивание листьев. Ежедневная потребность железа около 12мг.
Кальций потребность для взрослых 0,8 -1г, для детей 0,6 -0,9 г в сутки.
Кальций основной компонент костей. Ионы кальция передают возбуждение на мышечное волокно, вызывая ее сокращение, увеличивает силу сердечных сокращений, повышает фагоцитарную функцию лейкоцитов, активизирует защитную функцию белков, кальций влияет на проходимость сосудов – без этого элемента жиры, липиды и холестерин осели бы на стенках сосудов и закупорили бы их. Он способствует выведению из организма тяжелых металлов. Ионы кальция обеспечивают постоянство осмотического давления крови. Он способствует свертыванию крови при ранениях. В растениях он играет большую роль в работе устьиц. Обмен кальция и его поступления в кость регулируется витамином Д.
При недостатке кальция происходит вымывание его из костей, образуются камни в костях. Никотин, кофеин, алкоголь являются одним из причин недостатка кальция, т.к. способствуют его интенсивному выведению мочой. Недостаток в кальции вызывает увеличение свертываемости крови, уменьшению усвояемости цинка, клетками костной ткани, появление остеоартрита, катаракты, артериального давления.
Калий и натрий элементы биотоков. Так ли это?
Калий участвует в формировании костной ткани, участвует в поддержании нормальной проницаемости наружных мембран, для образования ряда ферментов, для поддержания сердечного ритма, участвует в работе нервной ткани. В человеческом организме до 0,25г. Суточная потребность 2-5г.
Натрий. Суточная потребность 0,1 -3,3 г. Натрий входит внутренний и внешний слой мембраны клетки для возникновения электрического мембранного биопотенциала.
При недостатке натрия возникают колики, судороги, нарушения кровообращения, слабость снижение давления, может быть обморок.
Металлы необходимые для жизнедеятельности человека?
В небольших количествах входит Mn, Co, Ni, Cn, Zn , AL , Cv , Ux потребность колеблется от 300мг до 0,2 мг в сутки. Цинк входит в состав ферментов. Содержание его в человеческом теле 2-3г. Используется для приготовления глазных капель, кожных мазей.
Марганец. Содержание его в человеческом теле 12-20мг. Недостаток его сказывается на рост длинных костей, на мышечный тонус, на образование хрящевой ткани.
Кобальт. Содержание 4-10мг. Он участвует в синтезе мышечных белков, нервных волокон, на усвоение кальция и фосфора, способствует включению иона железа в молекулу гемоглобина. Способствует углеводному обмену.
Никель. Содержание 14мг. В небольших количествах активирует пищеварительные ферменты. Много его в табачном дыме. В больших количествах он притупляет работу пищеварительных ферментов, влияет на зрение (кератины, керато-коньюктивиты). Влияет на работу кроветворительных органов.
Тяжелые металлы и почему они опасны?
Тяжелые металлы способны соединятся белком довольно прочно, нарушать тем самым работу ферментов.
Hg – энергично соединяется с группами HS – сосредотачивается в почках нарушает их работу – отеки.
Кадмий – задерживается в почках, печени, поджелудочной железе и щитовидной, нарушая тем самым их работу.
Свинец – вызывает сильнейшее отравление, поражение десен, заболевание почек, нервной системы.
Талий – поражение десен, выпадение волос, нарушается работа желудочно-кишечного тракта, нервной системы, почки.
Хром – в основном через органы дыхания ПДК – 0,0001мг/л. Соединяется с белками содержащими железо, белками печени, костного мозга, легких, вызывая рак легких и различные аллергии.
Название химического элемента
Биологическая роль в клетке
Для аэробных организмов служит окислителем в ходе клеточного дыхания, обеспечивая клетку энергией.
Участвует в свертывании крови, участвует в формировании костей и зубов, позвоночников и скелетов беспозвоночных.
Участвует в проведении нервного импульса. Поддерживает осмотическое давление в клетках
Проектная работа "Металлы и неметаллы в жизни человека"

Мало кто задумывался, что у металлов и неметаллов огромная роль в нашей жизни. Человек дышит воздухом, в котором содержатся неметаллы и соединения между ними. Он живет и применяет металлы и неметаллы в различных отраслях. Таких как медицина, машиностроение, в строительстве и хозяйстве. Так же они очень хорошо распространены в водах рек и озер, морей и океанов, составе тел животных, растений и даже в атмосфере. В организме человека содержится большое количество химических элементов. Предполагается, что недостаток или же избыток макроэлементов в организме вызывает нарушение процессов жизнедеятельности. Микроэлементы должны содержаться в определённых концентрациях, нарушение которых ведёт к патологическим изменениям.
Цель моего проекта : выяснить, какие металлы и неметаллы входят в состав человеческого организма, выяснить какова их биологическая роль.
Задачи моего проекта:
1) Выяснить значение металлов в организме человека (биологическая роль и токсичное действие).
2) Разобраться, что происходит при недостатке или избытке металлов и неметаллов.
3) Выяснить токсическое действие металлов.
4) Каким путём можно восполнить дефицит макро- и микроэлементов.
Актуальность моего проекта : Выбранная мною тема « Металлы и неметаллы в жизни человека» актуальна для всех нас: в настоящее время в нашей стране остро встали проблемы численности населения и продолжительности жизни. Здоровый образ жизни, правильное питание, уровень развития медицины, общая грамотность населения, социальные условия – вот те главные слагаемые, которые всегда, во все времена будут определяющими в здоровье и жизни человека. Что значит грамотно относиться к своему организму? Это, прежде всего, знать, что может спровоцировать те или иные заболевания. Может ли сам человек, хотя бы отчасти, быть «кузнецом своего здоровья»? Думаю, что да. Чем больше мы знаем, тем меньше не допускаем того, что может повредить нашему здоровью.
. Продуктом моего информационного проекта является памятка, с содержанием металлов и неметаллов в продуктах питания, а так же подробная презентация на эту тему.
I .1.1
Для начала, хотелось бы разобраться, что такое металлы и неметаллы и что они из себя представляют.
I .1.2
Что такое металлы?
Мета́ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых
веществ, обладающих характерными металлическими свойствами, такими, как высокие
теплопроводность и электропроводность.(серебро, медь, алюминий), характерный
В древние века было известно лишь 7 металлов ( Au , Ag , Cu , Pb , Fe , Hg ) . Это число соотносилось с количеством известных планет.
Что такое неметаллы?
Неметаллы — химические элементы с типично неметаллическими свойствами.
(водород, кислород, азот и.т.д..).
Впервые различие между металлами и неметаллами определил М.В. Ломоносов. «Металлы,- писал
он, - тела твёрдые, ковкие , блестящие». Металлы и неметаллы представлены в специальной Периодической системе химических элементов Д.И. Менделеева.

I .1.1 Роль металлов в нашей жизни
Роль металлов и в жизни человека обозначилась уже с доисторических времен. Первые металлы, с которыми познакомился человек, были медь, золото, серебро, ртуть, железо, олово, свинец. Целые эпохи стали «металлическими»: эпоха меди сменилась эпохой бронзы. На смену бронзе пришел «железный век ». В начале ХIХ века был открыт алюминий. А через полвека человек освоил его производство. В современном мире роль металлов просто огромна: металлические изделия окружают нас везде. Даже находясь в своей комнате, Вы наверняка обнаружите хотя бы одно изделие из этого материала. Еще в Средневековье алхимики утверждали, что поведение и характер человека зависят от того, какое количество металлов содержится в организме. Если в нем преобладает много свинца, то человек угрюмый и предпочитает темные тона в одежде. Если много железа, то он агрессивный и раздражается от красного цвета. А вот если в организме много меди, то человек дружелюбный и мягкий. Доля правды в этом конечно есть: в организме живых существ металлы оказывают влияние на все процессы жизнедеятельности. Например, открытие наличия железа в крови животных в XIX веке потрясло мир. Атомы железа являются составляющей частью гемоглобина, который занимается переносом кислорода, необходимого для протекания окислительно—восстановительных процессов в организме. Железо придает гемоглобину красный цвет, поэтому кровь животных и человека также красного цвета. Данный элемент в организм поступает вместе с продуктами питания – печенью, яблоками, творогами, сливами, дынями, тыквой, помидорами и абрикосами. Также для организма полезны такие ферменты как марганец, цинк и медь. Недостаточное количество металлов вызывает серьезные последствия. Недостаток кальция приводит к замедлению роста скелета и возникновению кариеса. А вот нехватка магния приводит к судорогам мышц.
Роль неметаллов в жизни человека
Неметаллы в жизни человека играют огромную роль, так как без них невозможна жизнь не только человека, но и других живых организмов. Ведь благодаря таким неметаллическим элементам, как кислород, углерод, водород и азот, образуются аминокислоты, из которых затем образуются белки, без чего не может существовать все живое на Земле. Такой необходимый микроэлемент, как сера, в организме человека выступает в роли минерала красоты, так как благодаря ней, кожа, ногти и волосы, будут оставаться здоровыми. Также, не стоит забывать, что сера принимает участие в формировании хрящевой и костных тканей, помогает улучшить работу суставов, укрепляет нашу мышечную ткань и выполняет еще много других функций, которые очень важны для здоровья человека. Анионы хлора также играют важную биологическую роль для человека, так как принимают участие в активизации некоторых ферментов. С их помощью поддерживается благоприятная среда в желудке и поддерживается осмотическое давление. Хлор, как правило, попадает в организм человека, благодаря поваренной соли при приеме пищи. Помимо важных качеств, которые неметаллы оказывают на человеческий организм, и другие живые организмы, эти вещества применяют и в других различных отраслях.
I . 1.4. Отрицательное влияние металлов и неметаллов.
Помимо всего положительного влияния , так же есть и отрицательное. Например токсичность, мера несовместимости вредного вещества с жизнью . Основным путем поступления тяжелых
металлов в организм является желудочно-кишечный тракт, который наиболее уязвим к действию техногенных экотоксикантов. Отравления соединениями тяжёлых металлов известны с древних времен. В середине четвёртого века сулема и мышьяк были наиболее распространёнными неорганическими ядами, которые использовались с криминальной целью в политической борьбе и в быту. которые использовались с криминальной целью в политической борьбе и в быту.
Отравления соединениями тяжелых металлов часто встречались в нашей стране в
1924г. Отравления соединениями меди преобладают в районах садоводства и
Отравления соединениями меди преобладают в районах садоводства и
виноделия, где для борьбы с вредителями используется медный купорос. В настоящее
время наиболее распространены отравления ртутью. Тем самым, можно сделать вывод, что тяжелые металлы и их соединения могут поступать в организм человека через лёгкие, слизистые оболочки, кожу и желудочно-кишечный тракт.
II .1. Практическая часть
II .1.2. Макро и микроэлементы
В Составе веществ, образующих клетки всех живых организмов, обнаружено более 70 элементов. Эти элементы принято делить на две группы: микроэлементы и макроэлементы.
Макроэлементы содержатся в клетках в больших количествах. В первую очередь это углерод, кислород, азот и водород. В сумме они составляют почти 98% всего содержимого клетки. Кроме названных элементов к макроэлементам относят также магний, калий, кальций, натрий, фосфор, серу и хлор. Суммарное из содержание 1,9% . Таким образом, на долю остальных химических элементов приходится около 0.1%. Это микроэлементы. К ним относят: железо, цинк, марганец, бор, медь, йод, кобальт, бром, фтор, алюминий и др.
Человек и животные получают нужные им для нормальной жизнедеятельности микроэлементы с пищей. Например, если в пище не хватает марганца, то возможна задержка роста, замедления половой зрелости, нарушение обмена веществ при формировании скелета.
Значение микроэлементов для человека впервые было выявлено при изучении такого заболевания, как эндемический зоб, которое вызывается недостатком йода в пище и воде. Прием соли, содержащей йод, приводит к выздоровлению, а добавка его к пище в малых количествах предупреждает заболевание.
II .1.3. Последствия недостатка макро и микроэлементов
Чтобы человек был здоровым, его организм должен обогащаться макро и микроэлементами. Только правильное сбалансированное питание может насытить организм человека полезными веществами, а также наладить обмен веществ .Макро и микроэлементы поступают в организм вместе с продуктами питания, с водой и воздухом. При дефиците макро и микроэлементов в организме больше всего страдают ногти и кожа. Для красоты и здоровья ногтей важно насыщать организм белком, который называют кератином. В основном организму человека недостаточно этих элементов:
Дефицит цинка приводит к заболеваниям центральной нервной системы, развитию депрессии, нервозности, сухости кожного покрова, ломкости ногтей, частым простудам. Для защиты и укрепления иммунной системы, чтобы определить, нет ли у вас дефицита цинка, можно сдать специальный анализ. По его результатам станет известно, нужно ли дополнительно пить цинк в таблетках.
Йод поддерживает гормональный баланс в организме человека, укрепляет иммунитет, помогает успешно противостоять инфекционным заболеваниям. Дефицит йода приводит к таким ситуациям как заболевания щитовидки, слабость и вялость. Ухудшается зрение, слух и память.
При недостатке меди в организме у человека нарушается обмен веществ, возникает депрессия.
Нехватка молибдена в организме приводит к ухудшению зрения, человек становится раздражительным.
Нехватка магния в организме человека приводит к бессоннице, пониженной памяти, головокружениям, головным болям, депрессии, плаксивости.
При недостатке кальция нарушается обмен веществ в организме.
При недостатке марганца ослабевает иммунитет.
Недостаток серы приводит к выпадению волос.
II .1.4. Избыток элементов в организме
Избыток элементов тоже встречается, но редко.
S - Избыток серы в организме приводит к снижению слуха и ухудшению зрения.
Cu – Избыток меди приводит к нарушению психики человека.
Mn - Острый гепатит.
Mg - Избыток марганца в организме человека приводит к замедлению пульса, сонливости, к тошноте, нарушению координации.
Ca - Из за избытка кальция может возникнуть тошнота, жажда, частая усталость, слабость и судороги.
С l – Избыток хлора в организме приводит к повышению концентрации хлора в крови.
Мо – Снижение массы тела.
Несмотря на то, что химические элементы содержатся в организме в незначительных количествах (в миллиграммах, а иногда и в микрограммах), роль их велика. Тяжелая экологическая ситуация, возрастание стрессовых ситуаций, методы обработки продуктов питания, «убивающие» биологически активные вещества, - вот далеко не полный перечень причин повсеместного роста дефицита жизненно важных элементов и избытка токсичных, наносящих непоправимый вред здоровью. У каждого металла своя дозировка. Малейшие ее колебания влияют на самочувствие людей. Таким образом каждый химический элемент вносит свою лепту в состояние нашего организма. И если этого элемента в организме в избытке или, наоборот, его не хватает, то человек начинает жаловаться на различного рода недомогания. Очень часто происходят изменения и во внешнем облике: волосы становятся тусклыми, с посеченными концами, ногти слоятся и ломаются, кожа приобретает землистый оттенок, теряет свою упругость. Здоровый организм сам способен регулировать содержание отдельных элементов. При наличии выбора (пищи и воды) животные и человек инстинктивно могут вносить лепту в это регулирование. Сознательное регулирование человеком содержания микроэлементов в почве, продуктов питания, является одной из важнейших задач.
Список источников
Л.Ю. Аликберова. «Занимательная химия», Дрофа, 1999-200с.
О.С. Габриелян – ХИМИЯ, 8 класс. Дрофа, 2015- 287с.
О.С. Габриелян – ХИМИЯ, 9 класс. Дрофа, 2015- 290с.
Габриелян О.С. «Настольная книга учителя химии». 9 класс, М.: Блик и К°, 2001
В.И. Добрынина, Е.Я. Свешникова. «Руководство к практическим занятиям по биологической химии», Медицина, 1977
Н.Е. Кузьменко, В.В.Еремин, В.А.Попков. «Начала химии», М.: Экзамен, Оникс 21 век, 2001.
М.Колтун. «Мир химии» – М.: Детская литература, 1988
А.С. Егоров, Н.М. Иванченко, «Химия внутри нас». Ростов-на-Дону: Феникс, 2004-180с.
Е.М. Ледовская «Металлы в организме человека» // Химия в школе. 2005. №3 – с 44-47.
Мультимедийное учебное пособие нового образца. «Химия». Электронная библиотека «Просвещение».
«Открытая химия». Версия 2.5 Автор курса – профессор МФТИ, Академик РАЕН
Н.Я. Логинов, А.Г. Воскресенский, И.С. Солодкин, «Аналитическая химия», Просвещение, 1979 .
В.В.Зеленцов. АНО «Центр Биотической Медицины». «Химические элементы и ваше здоровье», 2008 -51с.
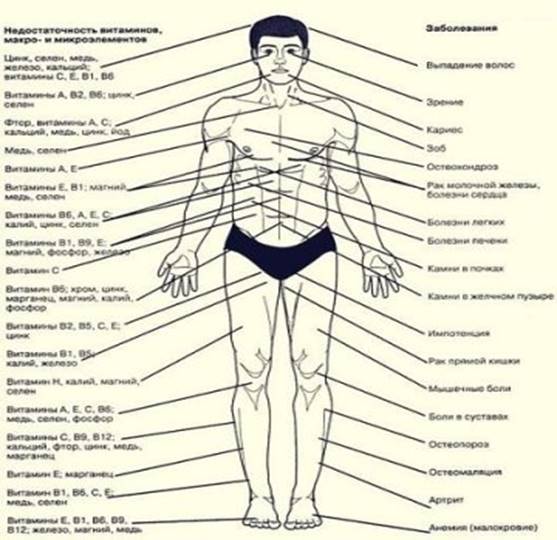
Приложение 1
Заболевания при недостатке макро и микроэлементов
Приложение 2
Биологическая роль и токсическое действие некоторых элементов в организме
Биологическая роль
Токсическое действие избытка металла
Ионы натрия поддерживают у животных и человека нормальную возбудимость мышечных клеток, участвуют в сохранении кислотно-основного баланса в организме, в регуляции сердечной деятельности (успокаивают), удерживают воду в организме.
Приводит к нарушению водного баланса, сгущению крови, вызывает дисфункцию почек, некоторые сердечно-сосудистые заболевания, а также общее нарушение обмена веществ.
Ионы калия регулируют белковый и углеводный обмен, влияют на процесс фотосинтеза и рост растений. Калий необходим для нормального функционирования всех мышц, особенно сердечной, способствует выделению избыточного натрия, избавляя организм от лишней воды и устраняя отеки.
Вызывает усиление двигательной активности, учащение сердечного ритма, нарушение углеводного, жирового и белкового обмена.
Соли магния проявляют антисептическое и сосудорасширяющее действие, понижают артериальное давление и содержание холестерина в крови, оказывают успокаивающее действие на нервную систему, играют большую роль в профилактике и лечении рака, благотворно действуют на органы пищеварения
Приводит к нарушению минерального обмена. Нарушение баланса обмена магния вызывает повышенную смертность от сердечно сосудистых заболеваний и болезней желудочно-кишечного тракта
Ионы кальция необходимы для процессов кроветворения, обмена веществ, для уменьшения проницаемости сосудов, нормального роста скелета, благотворно влияют на состояние нервной системы, оказывают противовоспалительное действие.
Если кальций попадает в организм в виде цементной
пыли, то страдают органы дыхания, у детей снижается возбудимость нервной системы.
Оказывает влияние на процессы костеобразования.
Поражаются костная ткань, печень, кровь, наблюдаются повышенная ломкость костей, выпадение волос.
Содержится в легких, печени, костях, головном мозге; действует на пищеварительные ферменты и нервную систему.
Приводит к нарушению минерального обмена.
При высоких концентрациях цинк — мутаген и онкоген. Вызывает заболевания костно-мышечной системы.
Биологический конкурент цинка.
Снижает активность пищеварительных ферментов, нарушает функцию поджелудочной железы, углеводный обмен, поражает почки и тормозит рост костей; увеличивает опасность переломов костей.
Используется в термометрах.
Поражает центральную нервную систему, сосредоточивается в почках, нарушая их деятельность; также накапливается в клетках мозга и слизистой оболочке рта.
Дефицит лития в организме человека приводит к психическим расстройствам
Вызывает общую заторможенность, нарушение дыхания и сердечного ритма, слабость, сонливость, потерю аппетита, жажду, расстройство зрения, а также дерматит лица и рук
Презентация "Неметаллы и наш организм"

НЕМЕТАЛЛЫ и НАШ ОРГАНИЗМ
Выполнила: преподаватель химии Гордеева С.В.
БУ «Нефтеюганский политехнический колледж».

В настоящее время известно более ста химических элементов, однако только небольшое число из них входит в состав живого на планете Земля. 16 элементами жизни являются : 10 металлов (Na, K, Mg, Ca, Zn, Cu, Co, Mn, Fe, Mo) и 6 неметаллов (H, O, N, C, P, S), составляющих основу биологически важных молекул и макромолекул. Элементы, находящиеся в небольших количествах в живых организмах и растениях (B, Cr, F, Cl, Br, I, Se, Si).

Кремний в организме человека
Кремний принимает участие в
процессе роста костной ткани, в
формировании хрящей и других
соединительных тканей, кроме того,
способствует поддержанию
эластичности стенок сосудов на
клеточном уровне. Кремний играет
главную роль в соединительных
компонентах ткани: эластине,
коллагене, муколисахаридах.
Снижение с возрастом уровня
кремния в аорте свидетельствует о
значимости микроэлемента в
развитии атеросклероза.

Организм усваивает только 4% кремния.
Норма кремния в день – 5 – 20 мг. Существует точка зрения, что оптимальное количество потребления кремния – 50 -100 мг.

Продукты с самым высоким содержанием кремния
неочищенное зерно,
продукция из хлебных злаков;
крупы (коричневый рис);
корнеплоды овощей
(топинамбур, картофель с
кожурой, свекла, редька,
репа, редис, лук);
водоросли;
отруби;
зелень;
ягоды;
минеральные воды.

Недостаток кремния
Недостаток кремния в организме развивается, если количество поступления микроэлемента составляет 5 мг в день и меньше.
Уровень кремния снижает избыток алюминия, употребление рафинированных пищевых продуктов. Нормализации содержания микроэлемента способствует рацион, богатый пищевыми волокнами.

Йод в организме человека
В организме человека содержится от 20 до 50 мг йода (iodine), из них не менее 60 % сосредоточено в щитовидной железе, 40% - в мышцах, яичниках, крови.
Щитовидная железа: йод является компонентом гормонов щитовидной железы и необходим для их синтеза. Они обуславливают уровень обмена веществ, оказывают влияние на преобразование пищи в энергию и на пути ее применения. Гормоны щитовидной железы значимы для роста и развития всех органов.

Йод в организме человека принимает участие в регуляции:
энергетического обмена, температуры тела;
скорости биохимических реакций;
обмена белков, жиров, водно-электролитного обмена;
процессов роста и развития организма, включая нервно-психическое развитие.

Польза йода:
обеспечивает большей энергией, способствует росту, облегчает соблюдение диеты за счет сжигания избыточного жира, активизирует умственную работу, гарантирует здоровье зубам, коже, ногтям, волосам.

Йод в продуктах питания:
морские продукты - красные и бурые водоросли (ламинария), палтус, треска, сельдь, креветки, пикша, морская соль, моллюски, сардины;
йодированная соль;
говяжья печень, яйца, молоко;
лук, щавель, белокочанная капуста, морковь (если выращены на почве, богатой йодом).

Симптомы дефицита йода в организме:
1.Увеличение выработки гормонов щитовидной железы.
2.Образование зоба.
3.Возникновение йододефицитных патологий:
• упадок сил, снижение работоспособности,
сонливость, развитие отеков конечностей,
туловища, лица;
• повышенный уровень холестерина;
• прибавление массы тела;
• понижение интеллектуального уровня:
• глухонемота;
• различные виды параличей;

Фтор в организме человека
Организм человека содержит фтор (fluorine) и фторид (соединение фтора с компонентами) в костях, зубах, кожном покрове и щитовидной железе. Содержание фтора примерно 2,6 г.

Свойства фтора
Зубы: фтор требуется для формирования эмали и твердой ткани зубов. Он оберегает зубы от кариеса и различных разрушений.
Костная система: адекватное потребление фтора способствует укреплению костей, предотвращению дегенеративных процессов.
Иные функции: фтор содействует быстрому заживлению ран и улучшению усвоения железа.

Фтор в продуктах питания
морская рыба (самая большая концентрация в соме, треске, скумбрии), морская капуста;
печень, баранина, телятина, молоко, яйца;
хлеб грубого помола, рис, овсяная крупа;
лук, шпинат, яблоки;
орехи.

Недостаток фтора в организме
Кариес зубов – заболевание, сопровождающееся процессом деминерализации и деструкции твердых тканей зубов с последующим образованием полостей.
Остеопороз - разрежение кортикального и губчатого слоев костной ткани в результате фрагментарного рассасывания костного вещества.

Хлор в организме человека.
Содержание хлора (chlorine) в организме приблизительно 115г, накопление макроэлемента происходит в коже, мышцах скелета, висцеральной ткани, концентрация во внеклеточном пространстве.

Хлор в организме человека.
Водный обмен: находясь в человеческом организме в форме солей (хлоридов), макроэлемент осуществляет функцию электролита - нормализацию водного баланса.
Кислотно-щелочной баланс: являясь одним из главных элементов водно-солевого .
Пищеварительная система: активизирует фермент амилазу, в соединении с водородом синтезирует соляную кислоту - важнейший компонент желудочного сока. Улучшает работу печени. Уровень хлора в организме обусловлен кислотностью пищеварительного сока: выше кислотность - больше расхода хлора. Воспалительные процессы (язвы, перитонит) приводят к уменьшению количества хлора в организме.

Хлор в продуктах питания
Фактически все пищевые продукты содержат хлор от 2 до 160 мг%. В особенности богаты макроэлементом мясные продукты, молочная продукция, хлеб.
пищевая соль;
оливы;

Недостаток хлора
Основными причинами недостатка хлора у человека является незначительное количество поступления с пищей и нарушения обмена хлора. Дефицит хлора встречается у детей на искусственном вскармливании.

Фосфор в организме человека
Содержание фосфора (phosphorus) в организме 500 - 750 г, примерно 90% сконцентрировано в зубах и костях.
Норма фосфора в сутки – 800 мг, максимально допустимое количество потребления - 1600 мг.
Недостаток фосфора

Функции фосфора.
Кости, зубы: в качестве компонента фосфата кальция фосфор является базовым элементом костей и зубов. И это главная функция макроэлемента.
Деление клеток: фосфор находится в составе фосфолипидов и фосфопротеинов в структуре мембран клеток, а также в составе нуклеиновых кислот, принимающих участие в процессах деления клеток, роста, хранения и применения генетической информации.
Синтез энергии: фосфор требуется для преобразования белков, углеводов и жиров в энергию. Он входит в состав молекулы аденозин трифосфата (ATP), который является аккумулятором энергии, обеспечивающим энергозависимые процессы в клетках тканей, особенно в мышечной и нервной.
Обмен веществ: фосфор принимает участие в метаболизме и продуцирование углеводов и белков.
ЦНС: фосфор вовлечен в процесс передачи нервных импульсов.

Польза фосфора
благоприятствует росту и восстановлению организма;
способствует нормализации энергетического обмена;
снижает болевые ощущения при артритах;
оказывает укрепляющее воздействие на зубы;
улучшает метаболизм;
содействует делению клеток;
координирует кислотно-щелочной баланс.

Фосфор в продуктах
молоко, молочные продукты (сыры);
мясо, субпродукты (говяжья печень), птица, яйца;
рыба, икра осетровых;
хлеб, овсяная и гречневая крупы;
орехи грецкие, семечки;
овощи, зелень (тыква, петрушка, капуста, шпинат, чеснок, морковь).

Селен в организме человека
Селен — важный микроэлемент,
являющийся частью многих ферментов и
благодаря этому играющий важную роль в
работе многих органов и систем организма.
Основная биологическая роль селена
связана с проявлением его антиоксидантных
свойств, т. к. селен является частью одного
из ключевых антиоксидантных ферментов
— глутатионпероксидазы. Дефицит селена
может привести к усилению перекисного
окисления липидов, которое в свою очередь
может привести к поражению многих
структур клетки, и как следствие — к
возникновению ряда патологических
состояний.

Свойства селена
Самое замечательное свойство
селена – борьба со старением.
Он защищает клетки от
свободных радикалов, а в
комплексе с витамином Е
раскрывает мощные
антиокислительные свойства.
Селен защищает организм от
тяжелых металлов и вредных
веществ, тем самым заслуживая
славу экологопротектора.

Норма селена
Суточная норма селена в питании - 20-70 мкг, максимально допустимое количество - 350 - 400 мкг.
В Соединенных Штатах норма селена для взрослых мужчин 70 мкг и для женщин - 55 мкг.
Селен в продуктах питания

Селен в продуктах
мясо внутренних органов, морепродукты, морские водоросли;
мышечное мясо, свиное сало;
зерно, хлебные злаки, пшеничные отруби;
молочная продукция;
оливковое масло;
овощи, фрукты, белые грибы, чеснок, бобовые, маслины, кокосы;
фисташки, кешью.
Краткое описание документа:
В настоящее время известно более ста химических элементов, однако только небольшое число из них входит в состав живого на планете Земля. 16 элементами жизни являются : 10 металлов (Na, K, Mg, Ca, Zn, Cu, Co, Mn, Fe, Mo) и 6 неметаллов (H, O, N, C, P, S), составляющих основу биологически важных молекул и макромолекул. Элементы, находящиеся в небольших количествах в живых организмах и растениях (B, Cr, F, Cl, Br, I, Se, Si). В данной презентации рассматриваются роль неметаллов для организма человека. К чему приводит избыток и недостаток неметаллов для нашего организма. В каких продуктах содержатся жизненноважные неметаллы.
Рабочие листы и материалы для учителей и воспитателей
Более 3 000 дидактических материалов для школьного и домашнего обучения
Читайте также:
