Металлы и их строение
Металлы – один из классов конструкционных материалов, характеризующийся определенным набором свойств:
К физическим свойствам металлов относят плотность, температуру плавления, цвет, блеск, непрозрачность, теплопроводность, электропроводность, тепловое расширение. По плотности металлы разделяют на легкие (до 3000 кг/м 3 ) и тяжелые (от 6000 кг/м 3 и выше); по температуре плавления — на легкоплавкие (до 973 К) и тугоплавкие (свыше 1173 К). Каждый металл или сплав обладает определенным, присущим ему цветом.
Прочность — способность металла в определенных условиях и пределах не разрушаясь воспринимать те или иные воздействия, нагрузки. Это свойство учитывается при изготовлении и проектировании изделий, выборе того или иного металла, сплава. Наибольшее напряжение, которое может выдержать металл, не разрушаясь, называют пределом прочности, или временным сопротивлением разрыву. Образцы для измерения прочности подвергают испытанию на специальной разрывной машине, которая постепенно, с возрастающей силой растягивает образец до полного разрыва.
Упругость — свойство металла восстанавливать свою форму после прекращения действия внешних сил, вызвавших деформацию. Наибольшее напряжение, после которого металл возвращается к своей первоначальной форме, называют пределом упругости. Если при дальнейшем повышении нагрузки напряжение превышает предел упругости и удлинение сохраняется после разгрузки образца, такое состояние называют остаточным удлинением. Далее наступает предел текучести, т.е. образец продолжает удлиняться без увеличения нагрузки.
Пластичность — свойство металла под действием внешних сил изменять, не разрушаясь, свою форму и размеры и сохранять остаточные (пластические) деформации после устранения этих сил . Данное свойство также определяется и измеряется на разрывной машине. Высокой пластичностью обладают золото, серебро, платина и их сплавы. Менее пластичны медь, алюминий, свинец. Это свойство металлов имеет большое значение в давильном и штамповочном производстве, волочении, прокатке.
Твердость — свойство металлов сопротивляться проникновению в них другого тела под действием внешней нагрузки, что необходимо учитывать при выборе инструментов для обработки металлов резанием. Например, важно знать твердость обрабатываемого металла, чтобы подобрать соответствующую фрезу или сверло. Испытания металлов на твердость проводят на специальных приборах — твердометрах.
Выносливость — свойство металлов сопротивляться действию повторных нагрузок . Температурные условия значительно влияют на механические свойства металлов: при нагревании их прочность понижается, а пластичность увеличивается; при охлаждений некоторые металлы становятся хрупкими, например, сталь некоторых марок, цинк и его сплавы. Нехладноломкими являются алюминий и медь.
Хрупкость — некоторые металлы обладают хрупкостью и при нормальных условиях, примером является серый чугун. В производстве изделий учитывается способность металлов поддаваться обработке, т.е. такие их технологические свойства, как ковкость, жидкотекучесть, литейная усадка, свариваемость, спекаемость, обрабатываемость резанием и некоторые другие.
Ковкость — способность металлов подвергаться ковке и другим видам обработки давлением (прокатке, прессованию, волочению, штамповке). Металлы могут коваться в холодном состоянии (золото, серебро, медь), а также в горячем (сталь).
Износостойкость – способность материала сопротивляться поверхностному разрушению под действием внешнего трения.
Коррозионная стойкость – способность материала сопротивляться действию агрессивных кислотных, щелочных сред.
Жаростойкость – это способность материала сопротивляться окислению в газовой среде при высокой температуре.
Жаропрочность – это способность материала сохранять свои свойства при высоких температурах.
Хладостойкость – способность материала сохранять пластические свойства при отрицательных температурах.
Антифрикционность – способность материала прирабатываться к другому материалу.
Жидкотекучесть — свойство расплавленного металла заполнять литейную форму. Высокой жидкотекучестью обладают цинк и его сплавы, чугун, бронза, олово, силумин (сплав алюминия с кремнием), латунь, некоторые магниевые сплавы. Низкой жидкотекучестью обладают сталь, красная медь, чистое серебро.
Литейная усадка —уменьшение объема металла при переходе из жидкого состояния в твердое. Это необходимо учитывать при изготовлении формы для отливки. Отливка получается всегда меньше модели, по которой сделана форма. Металлы с большой усадкой для литья почти не используют.
Свариваемость — способность металла прочно соединяться путем местного нагрева и расплавления свариваемых кромок изделия. Сплавы свариваются труднее, чистые металлы — легче. Легко свариваются изделия из малоуглеродистой стали. Плохо поддаются сварке чугун и высокоуглеродистые легированные стали.
Из химических свойств металлов и их сплавов наиболее важными в производстве художественных изделий являются растворение (взаимодействие с кислотами и щелочами) и окисление (антикоррозийная стойкость, т.е.стойкость к воздействию окружающей среды — газов, воды и т.д.).
Растворение (разъедание) — способность металлов растворяться в сильных кислотах и едких щелочах. Это свойство широко используется в различных областях производства художественных изделий. Растворение бывает частичное и полное. Частичное применяется для создания чистой поверхности изделия.
Окисление — способность металлов соединяться с кислородом и образовывать окислы металлов.
Данные свойства обусловлены особенностями строения металлов.
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определённым порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решётка.
Другими словами, кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело.
Элементарная ячейка – элемент объёма из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл.
Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются:
· размеры ребер элементарной ячейки. a, b, c – периоды решетки – расстояния между центрами ближайших атомов. В одном направлении выдерживаются строго определенными.
· углы между осями ().
· координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке.
· базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки.
Рис. Схема кристаллической решетки
Классификация возможных видов кристаллических решеток была проведена французским ученым О. Браве, соответственно они получили название «решетки Браве». Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа;
· примитивный – узлы решетки совпадают с вершинами элементарных ячеек;
· базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях;
· объемно-центрированный – атомы занимают вершины ячеек и ее центр;
· гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней
В металлических материалах, как правило, формируются три типа кристаллических решеток: объемноцентрированная кубическая (ОЦК), гранецентрированная кубическая (ГЦК) и гексагональная плотноупакованная (ГП). Элементарные ячейки ОЦК, ГЦК и ГП решеток показаны на рис. 9.

Рис. Типы кристаллических решеток металлов.
а) Г.Ц.К, б) О.Ц.К., в) Г.П.У.
Основными типами кристаллических реш¨ток являются:
- Объемно - центрированная кубическая (ОЦК), атомы располагаются в вершинах куба и в его центре
- Гранецентрированная кубическая (ГЦК), атомы располагаются в вершинах куба и по центру каждой из 6 граней
- Гексагональная, в основании которой лежит шестиугольник:
- простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита);
- плотноупакованная (ГПУ) – имеется 3 дополнительных атома в средней плоскости (цинк).
ОЦК решетку имеют такие металлы, как вольфрам, молибден, ниобий, низкотемпературные модификации железа, титана, щелочные металлы и ряд других металлов. Серебро, медь, алюминий, никель, высокотемпературная модификация железа и ряд других металлов имеют ГЦК решетку. ГП решетка у магния, цинка, кадмия, высокотемпературной модификации титана.
2. Физическая природа деформации металлов
Деформацией называется изменение формы и размеров тела под действием напряжений.
Напряжение – сила, действующая на единицу площади сечения детали.
Напряжения и вызываемые ими деформации могут возникать при действии на тело внешних сил растяжения, сжатия и т.д.,
Деформация металла под действием напряжений может быть упругой и пластической.
Упругой называется деформация, полностью исчезающая после снятия вызывающих ее напряжений.
При упругом деформировании изменяются расстояния между атомами металла в кристаллической решетке. Снятие нагрузки устраняет причину, вызвавшую изменение межатомного расстояния, атомы становятся на прежние места, и деформация исчезает.
Упругая деформация на диаграмме деформации характеризуется линией ОА (рис.).
Рис. Диаграмма зависимости деформации металла от действующих напряжений
Зависимость между упругой деформацией и напряжением выражается законом Гука
где: Е - модуль упругости.
Пластической или остаточной называется деформация после прекращения действия вызвавших ее напряжений.
В результате развития пластической деформации может произойти вязкое разрушение путем сдвига.
Механические свойства определяют поведение материала при деформации и разрушении от действия внешних нагрузок.
В зависимости от условий нагружения механические свойства могут определяться при:
статическом нагружении – нагрузка на образец возрастает медленно и плавно.
динамическом нагружении – нагрузка возрастает с большой скоростью, имеет ударный характер.
Прочность – способность материала сопротивляться деформациям и разрушению.
Испытания проводятся на специальных машинах, которые записывают диаграмму растяжения, выражающую зависимость удлинения образца (мм) от действующей нагрузки Р, т.е. .
Но для получения данных по механическим свойствам перестраивают: зависимость относительного удлинения от напряжения
Твердость – это сопротивление материала проникновению в его поверхность стандартного тела (индентора), не деформирующегося при испытании.
3. Методы определения твердости
О твердости судят либо по глубине проникновения индентора (метод Роквелла), либо по величине отпечатка от вдавливания (методы Бринелля, Виккерса, микротвердости).
Наибольшее распространение получили методы Бринелля, Роквелла, Виккерса. Схемы испытаний представлены на рис. 7.1.
Рис. Схемы определения твердости: а – по Бринеллю; б – по Роквеллу; в – по Виккерсу
3.1. Твердость по Бринеллю ( ГОСТ 9012)
Испытание проводят на твердомере Бринелля (рис.7.1 а)
В качестве индентора используется стальной закаленный шарик диаметром D 2,5; 5; 10 мм, в зависимости от толщины изделия.
Нагрузка Р, в зависимости от диаметра шарика и измеряемой твердости: для термически обработанной стали и чугуна – , литой бронзы и латуни – , алюминия и других очень мягких металлов – .
Продолжительность выдержки: для стали и чугуна – 10 с, для латуни и бронзы – 30 с.
Полученный отпечаток измеряется в двух направлениях при помощи лупы Бринелля.
Твердость определяется как отношение приложенной нагрузки Р к сферической поверхности отпечатка F:
Стандартными условиями являются D = 10 мм; Р = 3000 кгс; = 10 с. В этом случае твердость по Бринеллю обозначается НВ 250, в других случаях указываются условия: НВ D / P / , НВ 5/ 250 /30 – 80.
3.2. Метод Роквелла ГОСТ 9013
Основан на вдавливании в поверхность наконечника под определенной нагрузкой (рис. 7.1 б)
Индентор для мягких материалов (до НВ 230) – стальной шарик диаметром 1/16” (1,6 мм), для более твердых материалов – конус алмазный.
Нагружение осуществляется в два этапа. Сначала прикладывается предварительная нагрузка (10 ктс) для плотного соприкосновения наконечника с образцом. Затем прикладывается основная нагрузка Р1, втечение некоторого времени действует общая рабочая нагрузка Р. После снятия основной нагрузки определяют значение твердости по глубине остаточного вдавливания наконечника h под нагрузкой.
В зависимости от природы материала используют три шкалы твердости (табл. 7.1)
Шкалы для определения твердости по Роквеллу
3.3. Метод Виккерса
Твердость определяется по величине отпечатка (рис.7.1 в).
В качестве индентора используется алмазная четырехгранная пирамида.с углом при вершине 136 o .
Твердость рассчитывается как отношение приложенной нагрузки P к площади поверхности отпечатка F:
Нагрузка Р составляет 5…100 кгс. Диагональ отпечатка d измеряется при помощи микроскопа, установленного на приборе.
Преимущество данного способа в том, что можно измерять твердость любых материалов, тонкие изделия, поверхностные слои. Высокая точность и чувствительность метода.
Способ микротвердости – для определения твердости отдельных структурных составляющих и фаз сплава, очень тонких поверхностных слоев (сотые доли миллиметра).
Аналогичен способу Виккерса. Индентор – пирамида меньших размеров, нагрузки при вдавливании Р составляют 5…500 гс
3.4. Метод царапания.
Алмазным конусом, пирамидой или шариком наносится царапина, которая является мерой. При нанесении царапин на другие материалы и сравнении их с мерой судят о твердости материала.
Можно нанести царапину шириной 10 мм под действием определенной нагрузки. Наблюдают за величиной нагрузки, которая дает эту ширину.
3.5. Динамический метод (по Шору)
Шарик бросают на поверхность с заданной высоты, он отскакивает на определенную величину. Чем больше величина отскока, тем тверже материал.
Что такое металлы и их строение
Определение металлов можно дать с позиций химии, физики и техники.
В химии металлы — это химические элементы, находящиеся в левой части периодической системы элементов Д. И. Менделеева, которые обладают особым механизмом взаимодействия валентных электронов (ионов) с ядром как в самих металлах, так и при вступлении в химические реакции с другими элементами, в том числе с металлами.
Физика характеризует металлы как твердые тела, обладающие цветом, блеском, способностью к плавкости (расплавлению) и затвердеванию (кристаллизации), тепло- и электропроводностью, магнитными и другими свойствами.
В технике металлы — это конструкционные материалы, обладающие высокой обрабатываемостью (ковкостью, штампуемостью, обрабатываемостью резанием, паяемостью, свариваемостью и др.), прочностью, твердостью, ударной вязкостью и рядом других ценных свойств, благодаря которым они находят широкое применение.
Русский ученый М. В. Ломоносов (1711 — 1765), исследуя металлы и неметаллы в своем труде «Первые основания металлургии или рудных дел», дал металлам определение: «Металлом называется светлое тело, которое ковать можно. Таких тел находим только шесть: золото, серебро, медь, олово, железо и свинец». Это определение М. В. Ломоносов дал в 1773 г., когда известны были только шесть металлов.
Из металлов, добываемых из недр земли, получают большую группу конструкционных материалов, применяемых в различных отраслях промышленности. В природе одни металлы встречаются в чистом, самородном виде, другие — в виде оксидов (соединений металла с кислородом), нитридов и сульфидов, из которых состоят различные руды этих металлов.
Самыми распространенными металлами, применяемыми в качестве конструкционных материалов, являются железо, алюминий, медь и сплавы на основе этих металлов.
К металлам относятся более 80 элементов периодической системы Менделеева. Все эти металлы подразделяются на две большие группы: черные металлы и цветные металлы.
Характерными признаками черных металлов являются темно-серый цвет, блеск, высокие плотность и температура плавления, твердость, прочность, вязкость и полиморфизм (аллотропия). По физикохимическим свойствам черные металлы подразделяют на пять групп:
- железистые (железо, кобальт, никель, марганец);
- тугоплавкие (вольфрам, рений, тантал, молибден, ниобий, ванадий, хром, титан и др.);
- урановые — актиниды (уран, торий, плутоний и др.);
- редкоземельные — лантаниды (лантан, церий, иттрий, скандий и др.);
- щелочно-земельные (литий, натрий, калий, кальций и др.).
Из этих пяти групп черных металлов особенно широкое применение в промышленном производстве находят железистые и тугоплавкие металлы.
Железистые металлы, кроме марганца, называют еще ферромагнетиками. Ферромагнетики способны намагничиваться и притягивать металлы своей группы.
К тугоплавким относятся металлы, которые имеют температуру плавления выше температуры плавления железа (1 539 °С): титан — 1 667 °С, ванадий — 1 902 °С, хром — 1 903 °С, молибден — 2 615 °С, ниобий — 2 460 °С, тантал — 2 980 °С, вольфрам — 3 410 °С. Тугоплавкие металлы в основном применяются как легирующие элементы в производстве жаропрочных, жаростойких, теплостойких и специальных сплавов, в том числе твердых сплавов и высоколегированных сталей.
2. Строение металлов
Атомно-кристаллическая структура металлов. Как известно, все вещества состоят из атомов, в том числе и металлы. Каждый металл (химический элемент) может находиться в газообразном, жидком или твердом агрегатных состояниях. Каждое агрегатное состояние будет иметь свои особенности, отличные друг от друга. В газообразном металле расстояние между атомами велико, силы взаимодействия малы и атомы хаотично перемещаются в пространстве; газ стремится к расширению в сторону большего объема. При понижении температуры и давления вещество переходит в жидкое состояние. Свойства жидкого вещества резко отличаются от свойств газообразного. В жидком металле атомы сохраняют лишь так называемый ближний порядок атомов, т. е. в объеме расположено небольшое количество атомов, а не атомы всего объема. При понижении температуры жидкий металл переходит в твердое состояние, которое имеет строгую закономерность расположения атомов.
Если условно провести вертикальные и горизонтальные линии связи через центры атомов, можно увидеть, что у металлов в твердом состоянии атомы расположены в строго определенном порядке и представляют собой множество раз повторяющиеся элементарные геометрические фигуры — параллелепипеды (рис. 1). Наименьшую геометрическую фигуру называют элементарной ячейкой. Элементарные ячейки, расположенные на горизонтальных и вертикальных кристаллографических плоскостях (рис. 2), образуют пространственную кристаллическую решетку.
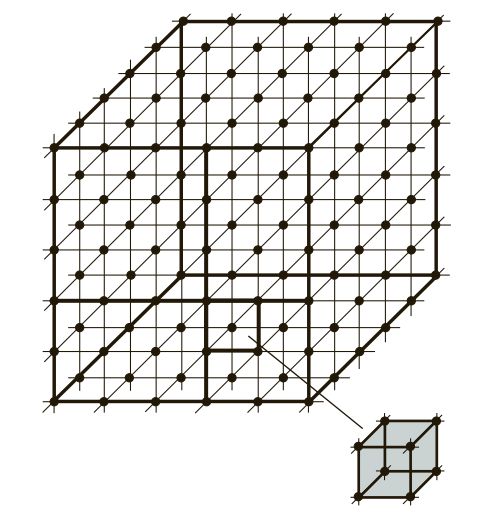
Рис. 1. Схема расположения элементарных геометрических ячеек в атомных решетках металлов и сплавов
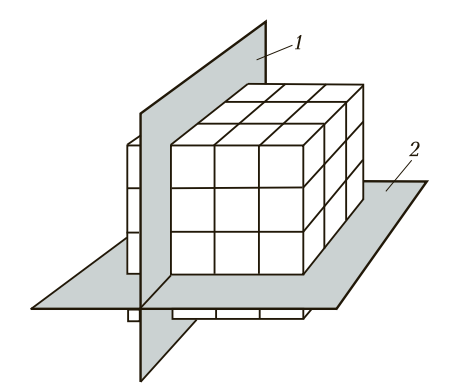
Рис. 2. Расположение кристаллографических плоскостей: 1 и 2 — соответственно горизонтальная и вертикальная кристаллографические плоскости
Элементарные кристаллические решетки характеризуют следующие основные параметры: расстояние между атомами по осям координат (по линиям связи), углы между линиями связи, координационное число — число атомов, находящихся на наиболее близком и равном расстоянии от любого атома в решетке. Форму элементарной ячейки рассматривают по кристаллографическим плоскостям в трех измерениях.
Таким образом, любой металл можно представить не как однородную цельную массу, а как массу, сложенную из множества элементарных ячеек. Блок элементарных атомных кристаллических ячеек образует атомно-кристаллическую ячейку (решетку). Если выделить эту элементарную ячейку, то в зависимости от металла получим следующие типы кристаллических ячеек (рис. 3): куб (К), объемно-центрированный куб (ОЦК), гранецентрированный куб (ГЦК), гексагональная плотноупакованная ячейка (ГПУ), гексагональная простая ячейка (Г) и др.
Простая кубическая ячейка (рис. 3, а) характерна для неметаллов, которые обладают наибольшими плотностью и удельным весом, и имеет восемь атомов, которые расположены в каждой вершине куба.
Объемно-центрированная кубическая ячейка (рис. 3, б ) состоит из восьми атомов, которые расположены по одному атому в каждой вершине куба, и одного, находящегося в центре куба на равных расстояниях от его граней. Эту форму атомной кристаллической ячейки имеют железо модификации Fe-α, ванадий, вольфрам, молибден, тантал и хром, т. е. в основном черные металлы.
Гранецентрированная кубическая ячейка (рис. 3, в) имеет 14 атомов — по одному атому в каждой вершине куба (восемь атомов) и по одному атому в центре каждой грани (шесть атомов). Гранецентрированную кубическую ячейку имеют алюминий, железо модификации Fe-γ, золото, кобальт, медь, никель, платина и серебро, в основном это цветные металлы и часть черных металлов.
Гексагональная плотноупакованная ячейка (рис. 3, г) состоит из 17 атомов. Форма геометрического тела, которую образуют эти атомы, является шестигранной призмой. При этом по шесть атомов расположены в каждой вершине верхнего и нижнего оснований, по одному атому в центре этих оснований и три атома в центре одной их трех граней (через грань). Гексагональную плотноупакованную ячейку имеют бериллий, кадмий, магний, ванадий, тантал.
Простая гексагональная ячейка (рис. 3, д) состоит из 12 атомов, которые расположены в вершинах верхнего и нижнего оснований шестигранной призмы. Такую кристаллическую ячейку имеют ртуть и цинк.
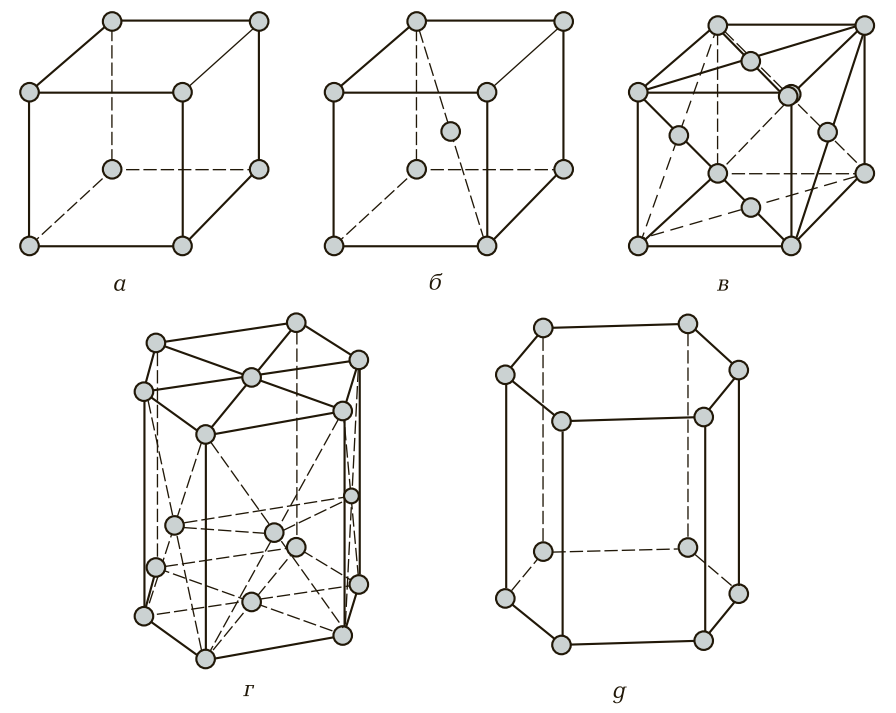
Рис. 3. Геометрические формы элементарных кристаллических ячеек: а — куб; б — объемно-центрированный куб; в — гранецентрированный куб; г — гексагональная плотноупакованная ячейка; д — гексагональная простая ячейка
Связь между атомами в кристаллической решетке и между решетками осуществляется за счет так называемой металлической связи. От прочности этой связи зависят прочность и твердость металлов. Чем выше эта связь, тем бо´льшую прочность и твердость имеют металлы. Механизм связи между атомами в решетке и между решетками имеет сложную физико-химическую природу.
В практике идеальное расположение кристаллических решеток обычно не наблюдается. Кристаллы, образуемые кристаллическими решетками, имеют искаженную геометрическую форму и различную величину.
Анизотропия металлов. Анизотропия (от гр. anisos — неравный и tropos — направление) — неодинаковость физических свойств среды (тела) в различных направлениях. Анизотропия предполагает зависимость свойств металлов от направления по плоскостям атомно-кристаллических решеток. Чем больше в плоскости атомов, тем выше свойства металлов. В горизонтальных плоскостях в любой форме атомно-кристаллических решеток больше, чем в вертикальных плоскостях. Следовательно, прочность металлов, испытанная в горизонтальном направлении, выше, чем в вертикальном. Анизотропия проявляется в процессе обработки конструкционных материалов давлением (проката, волочения, штамповки и других технологических способов получения заготовок и изделий).
На рис. 2 кристаллографические плоскости совпадают с линиями связи, проходящими через атомы металла. Форма элементарной кристаллической ячейки, расстояние между атомами и прочность металлической связи определяют физические, механические и технологические свойства металлов. Если исследуемый металл рассматривать по трем кристаллографическими плоскостям, по линиям связи между атомами, то можно заметить, что свойства по этим трем измерениям будут различны. Число атомов в этих плоскостях неодинаково. Металлическая связь между горизонтально и вертикально расположенными атомами также неодинакова. Это, в свою очередь, приводит к различной прочности металлов в продольном и поперечном направлениях. Например, предел прочности меди в продольном направлении будет в 2 раза больше, чем в поперечном.
Все металлы анизотропны, так как они состоят из кристаллов. Кристаллическое строение металлов обусловливает пластическую деформацию, т. е. изменение внешней формы и размеров под действием нагрузок без разрушения. Способность металлов и сплавов пластически деформироваться положена в основу их обработки давлением (прокатка, волочение, ковка, штамповка и прессование). При обработке давлением, например прокатке (рис. 4, а), происходит перемещение одного слоя атомных решеток по другому по кристаллографическим плоскостям (рис. 4, б).
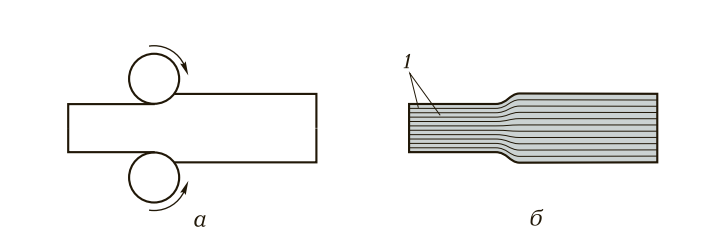
Рис. 4. Схема деформации металлов и сплавов (прокатка): а — деформация; б — скольжение металлов по кристаллографическим плоскостям в процессе деформации; 1 — кристаллографические плоскости
В процессе деформации металла при прокатке происходит не только изменение поперечных и продольных размеров заготовок, но и изменение микроструктуры металла.
Зерна под действием давления прокатных валков искажаются, приобретая продолговатую или пластинчатую форму, а затем преобразуются в волокна. Изменение микроструктуры металла в процессе деформации условно показано на рис. 5.
Процесс кристаллизации. Рассмотрим, как происходит образование кристаллов у чистых металлов. Установлено, что процесс кристаллизации металлов из жидкого состояния в твердое идет в две стадии:
- образование центров кристаллизации;
- рост кристаллов вокруг этих центров (рис. 6).
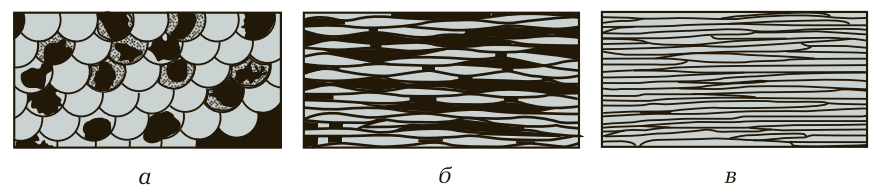
Рис. 5. Изменение микроструктуры металла в процессе деформации: а — микроструктура металла до деформации; б — микроструктура металла после первой операции деформации; в — микроструктура металла после окончательной деформации
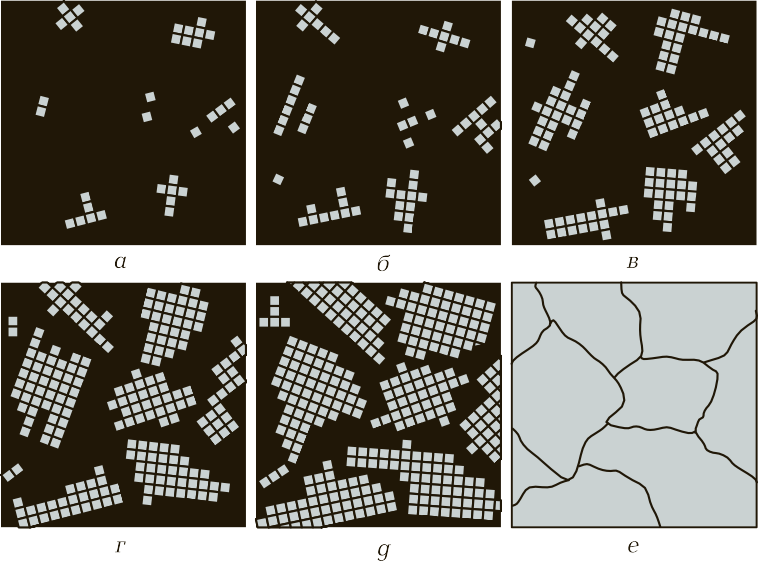
Рис. 6. Процесс кристаллизации металлов и сплавов: а — е — последовательные этапы процесса
Далее вновь появляются новые центры, и происходит рост твердой фазы вокруг первичных и вторичных центров. Процесс происходит до того момента, пока образованные таким образом кристаллы не будут соприкасаться друг с другом и не будет наличия жидкой фазы металла (см. рис. 6, г — е). Когда образование кристалла идет в жидкой фазе (в расплавленном металле), он будет иметь правильную форму, т. е. состоять из определенных геометрических фигур правильной формы. Когда кристаллы начинают соприкасаться друг с другом, а процесс затвердевания еще не закончен, тогда происходят искажения формы зерен. В практике замечено, что когда идет быстрое охлаждение, образуются мелкие зерна — мелкозернистая структура. При медленном охлаждении появление новых центров кристаллизации замедляется, но происходит рост зерна вокруг первичных центров кристаллизации. В этом случае металл будет иметь крупнозернистую структуру.
Процесс образования кристаллов в жидком состоянии и перехода металла в твердое состояние называется первичной кристаллизацией. Величина и форма зерна влияет на механические свойства металлов. Чем зерна мельче и чем правильнее их форма, тем большую твердость и прочность будет иметь металл. Чем зерна больше и чем искаженнее их форма, тем ниже твердость и прочность металла.
Аллотропия металлов. Такие металлы, как железо, кобальт, никель и др., обладают способностью изменять кристаллическую решетку при нагревании в твердом состоянии. Процесс изменения кристаллических решеток в твердом состоянии называется вторичной кристаллизацией, или аллотропией, а состояние вещества (металла) при наличии нескольких кристаллических решеток при изменении параметров (давления, температуры) — аллотропическими модификациями, или полиморфизмом. Такие металлы, как железо, молибден, вольфрам, литий в твердом состоянии при нормальной температуре имеют объемно-центрированную кубическую ячейку; алюминий, медь, серебро в твердом состоянии при нормальной температуре имеют форму гранецентрированной кубической ячейки.
На рис. 7 представлены кривые нагрева и охлаждения металла (на примере марганца). Аллотропные состояния (модификации), имеющие те или иные кубические ячейки, обозначаются греческими буквами. Первоначальное аллотропное состояние при нормальной температуре обозначается буквой α, при дальнейших повышении температуры и перекристаллизации металла — буквами β, γ, δ и т. д. При охлаждении металлов и сплавов процесс аллотропного превращения происходит в обратном порядке, как правило при тех же температурах.
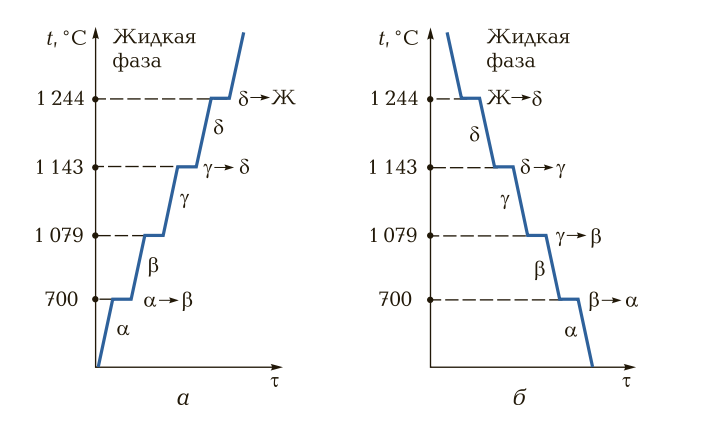
Рис. 7. Кривые нагрева (а) и охлаждения (б) марганца: t — температура; τ — время
Кристаллическое строение металлов

Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.
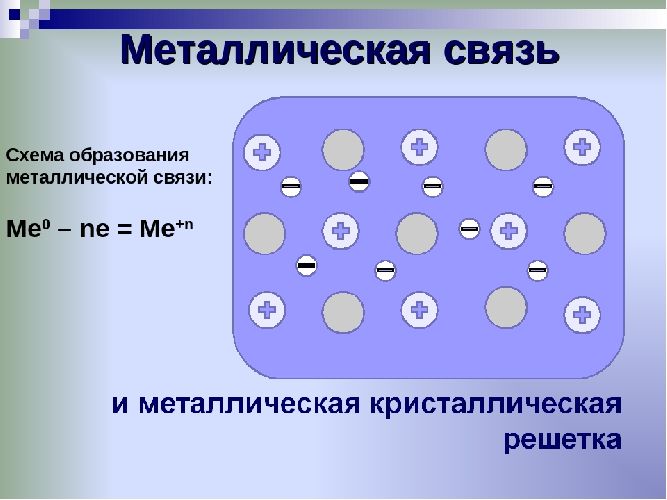
Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.
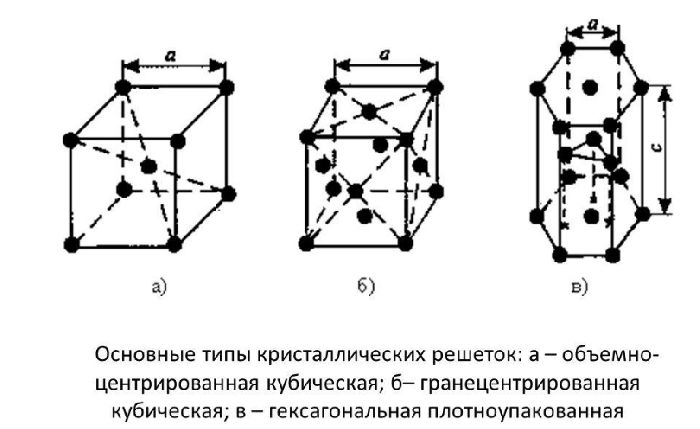
Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.
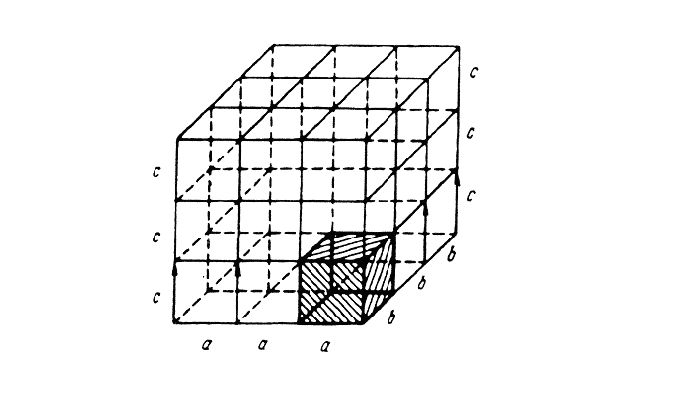
Рис. 3. Кристаллические ячейки составляют решётку.
Что мы узнали?
Узнали кратко об атомно-кристаллическом строении металлов. Металлы – твёрдые кристаллические вещества. Единицей решётки является элементарная кристаллическая ячейка. Благодаря металлическим связям ионы в узлах ячеек удерживаются на одинаковом расстоянии. Различают три типа кристаллических решёток – ОЦК, ГЦК и ГПУ, отличающихся количеством атомов и геометрической формой.
Металлы

К металлам относится большая часть элементов периодической системы – 82 химических элементов. Какими свойствами они обладают, и чем отличаются от неметаллов?
Общая характеристика
Металлами называют группу элементов, в виде простых веществ, которые обладают металлическими свойствами (пластичность, ковкость, блеск, электронная проводимость и т. д.)
Основное отличие элементов-металлов – они обладают только восстановительными свойствами, а в реакциях могут только окисляться. В соединениях они могут иметь только положительные степени окисления как в элементарных положительно заряженных ионах, так и в сложных ионах, где они образуют положительные центры.
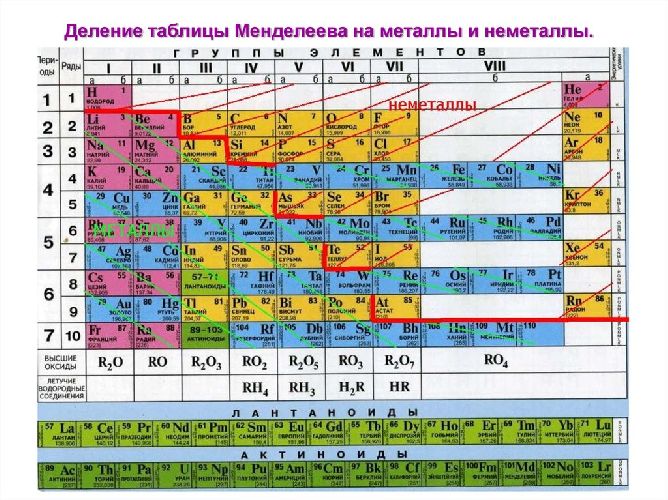
Рис. 1. Список металлов.
Как правило, на внешнем уровне элементов металлов находится небольшое число электронов (1-3), значения электроотрицательности невысокие. К металлам относятся все s-элементы (кроме водорода и гелия), d- и f-элементы, а также p-элементы под чертой бор-астат. Для типичных металлов характерен большой размер атомов, что способствует легкости отдачи валентных электронов. Образующиеся положительные ионы устойчивы, так как имеют завершенную внешнюю электронную оболочку.
Физические и химические свойства
Все металлы, кроме ртути, при нормальных условиях в виде простых веществ находятся в твердом агрегатном состоянии и образуют металлическую кристаллическую решетку.

Рис. 2. Металлы в таблице Д.И. Менделеева.
Таблица «Металлы»
В следующей таблицы представлены группы основных металлов:
| Группа металлов | Металл |
| Щелочные | литий, натрий, калий и т.д. |
| Щелочноземельные | кальций, стронций, барий и т.д. |
| Переходные | уран, титан, железо, платина и т.д. |
| постпереходные | алюминий, свинец, олово и т.д. |
| Тугоплавкие | молибден, вольфрам |
| Цветные | медь, титан, магний и т.д. |
| Благородные | золото, серебро и т.д. |
Металлы пластичны и ковки, особенно если на внешнем электронном уровне атомов по одному электрону: слои атомов перемещаются относительно друг друга без разрушения кристаллической решетки (щелочные металлы, медь, серебро, золото). В атомах непластичных хрупких металлов хрома и марганца – большое число валентных электронов.
Плотность, твердость, температура плавления металлов изменяются в широком диапазоне и зависят от атомной массы, строения атома и геометрии кристаллической решетки. Самый легкий металл – литий (плотность 0,53 г/см 3 ), самый тяжелый – осмий (плотность 22,5 г/см 3 ). Металлы с плотностью больше 5 г/см 3 относят к тяжелым, меньше 5 г/см 3 – к легким металлам.
Самая низкая температура плавления у ртути (-39 градусов по Цельсию), самый тугоплавкий металл – вольфрам (температура плавления 3410 градусов по Цельсию.) Энергия атомизации вольфрама составляет 836 кДж/моль, а температура кипения его 5930 градусов.
Металлы вступают в реакцию как с простыми, так и со сложными веществами. Как типичные восстановители металлы реагируют почти со всеми неметаллами-окислителями (кислород, сера, азот и т. д.):
Также металлы реагируют с такими сложными веществами, как оксиды и гидроксиды, разбавленные растворы кислот, с растворенными в воде щелочами.
В пределах одного и того же периода металлические свойства ослабевают, а неметаллические усиливаются; в пределах одной и той же группы (в главной подгруппе) металлические свойства усиливаются, а неметаллические ослабевают

Рис. 3. Металлы главных подгрупп.
Нахождение металлов и способы их получения
Самый распространенный на земле элемент-металл – алюминий. За ним следуют железо, кальций, натрий.
Некоторые металлы встречаются в природе в самородном состоянии (золото, ртуть, платина), но в основном они находятся в природе в виде оксидов и солей.
Получение металлов происходит с помощью металлургии (получение из руд), пирометаллургии (получение с помощью реакции восстановления при высокой температуре), гидрометаллургии (извлечение из руд в виде растворимых соединений), электрометаллургии (получение металлов электролизом расплавов и растворов их соединений).
Металлы – вещества, которые обладают высокой электро- и теплопроводностью, ковкостью, пластичностью и металлическим блеском. В данной статье по химии 9 класса рассматриваются их физические и химические свойства, формулы класса металлов, а также способы получения.
Строение металлов
Металлы -- простые вещества, обладающие в обычных условиях характерными свойствами: высокой электро - и теплопроводностью, отрицательным температурным коэффициентом электропроводности, способностью хорошо отражать электромагнитные волны (блеск и непрозрачность), высокой прочностью и пластичностью.
Свойства металлов могут значительно измениться при очень высоких давлениях. Многие металлы в зависимости от температуры и давления могут существовать в виде нескольких кристаллических модификаций.
Подобными металлическими свойствами обладают более 80 химических элементов и множество металлических сплавов. Число металлических сплавов, применяемых в технике, исчисляется тысячами и постоянно возрастает в соответствии с возникающими новыми и разнообразными требованиями, предъявляемыми многими отраслями промышленности.
Свойства металлов обусловлены их кристаллическим строением и наличием в их кристаллической решетке многочисленных не связанных с атомными ядрами подвижных электронов проводимости.
Металлические сплавы по свойствам имеют много общего с металлами, поэтому их нередко относят к металлам.
Металлы (сплавы) в промышленности разделяют на две основные группы: черные и цветные металлы.
Черные металлы -- сплав железа с углеродом, в котором могут содержаться в большем или меньшем количестве и другие химические элементы. Кобальт, никель, а также близкий к ним по свойствам марганец нередко относят к черным металлам. Черные металлы получили наибольшее распространение, что обусловлено относительно высоким содержанием железа в земной коре, его низкой стоимостью, высокими механическими и технологическими свойствами.
Цветные металлы по свойствам подразделяют на следующие группы:
легкие (Be, Mg, Al, Ti), обладающие сравнительно малой плотностью -- до 5000 кг/м 3 ;
тугоплавкие (Ti, Сг, Zr, Nb, Mo, W, V и др.) с температурой плавления выше, чем у железа (1539°С);
благородные (Ph, Pd, Ag, Os, Pt, Аи и др.), обладающие химическойинертностью:
урановые (U, Th, Pa) -- актиноиды, используемые в атомной технике;
редкоземельные металлы (РЗМ), лантаноиды (Се, Рг, Nd, Sm и др.) и сходные с ними иттрий и скандий, применяемые как присадки к различным сплавам;
щелочноземельные металлы (Li, Na, К), используемые в качестве теплоносителей в ядерных реакторах.
Классификация металлических сплавов по химическому составу, основанная на указании главного компонента сплава (железо, медь, алюминий и др.), имеет традиционный характер, и получила наибольшее распространение.
Макро-, микро- и атомную структуру металлов и сплавов изучает металлография.
Макроструктура - это строение металла, видимое невооруженным глазом или с помощью лупы в изломе или на протравленном шлифе. Микроструктура строения металла, наблюдаемое под оптическим или электронным микроскопами, позволяющими увеличить рассматриваемый участок от десяти раз до сотен тысяч раз.
Атомная структура металлов - это пространственное расположение атомов в кристаллической решетке. Этот вид структуры исследуется с помощью рентгено- графического структурного анализа.
Строение металла
Все металлы имеют кристаллическое строение. Располагаясь тем или иным способом, атомы образуют элементарную ячейку пространственной кристаллической решетки. Тип ячейки зависит от химической природы и состояния металла. Кристаллическое состояние, прежде всего, характеризуется определенным, закономерным расположением атомов в пространстве. Это обусловливает то, что в кристалле каждый атом имеет одно и то же количество ближайших атомов -- соседей, расположенных на одинаковом от него расстоянии. В процессе кристаллизации положительно заряженные ионы, располагаясь последовательно в виде элементарных кристаллических решеток, образуют кристаллы в виде зерен или дендритов. Все металлы и сплавы имеют кристаллическое строение. Образующиеся кристаллы растут, кристаллизуются из жидкого расплава сначала свободно, не мешают один другому, потом они сталкиваются и рост кристаллов продолжается только в тех направлениях, где есть свободный доступ жидкого металла. В результате первоначальная геометрически правильная форма кристаллов нарушается. После затвердевания зерна и дендриты имеют неправильную, геометрически искаженную форму.

Рисунок 1. Схема кристаллизации: а - в виде зерен; б - в виде дендритов.
Стремление атомов (ионов) металла расположиться, возможно, ближе друг к другу, плотнее, приводит к тому, что число встречающихся комбинаций взаимного расположения атомов металла в кристаллах невелико.
Существует ряд схем и способов описания вариантов взаимного расположения атомов в кристалле. Взаимное расположение атомов в одной из плоскостей показано на схеме размещения атомов (рисунок 2) .

Рисунок 2. Элементарная кристаллическая ячейка (простая кубическая).
Воображаемые линии, проведенные через центры атомов, образуют решетку, в узлах которой располагаются атомы (положительно заряженные ионы); это так называемая кристаллографическая плоскость. Многократное повторение кристаллографических плоскостей, расположенных параллельно, воспроизводит пространственную кристаллическую решетку, узлы которой являются местом расположения атомов (ионов). Расстояния между центрами соседних атомов измеряются ангстремами (1 А= 1 * 10 -8 см) или в килоисках -- kX (1kX = 1,00202 А). Взаимное расположение атомов в пространстве и величину между атомных расстояний определяют рентгеноструктурным анализом. Расположение атомов в кристалле весьма удобно изображать в виде пространственных схем, в виде так называемых элементарных кристаллических ячеек. Под элементарной кристаллической ячейкой подразумевается наименьший комплекс атомов, который при многократном повторении в пространстве позволяет воспроизвести пространственную кристаллическую решетку. Простейшим типом кристаллической ячейки является кубическая решетка. В простой кубической решетке атомы расположены (упакованы) недостаточно плотно. Стремление атомов металла занять места, наиболее близкие друг к другу, приводит к образованию решеток других типов: кубической объемноцентрированной (рисунок 3, а), кубической гранецентрированной (рисунок 3, б) и гексагональной плотноупакованной (рисунок 3, в).

Рисунок 3. Элементарные кристаллические ячейки: а - кубическая объемноцентрированная; б - кубическая гранецентрированная; в - гексагональная плотноупакованная.
металл теплопроводность электромагнитный температурный
Кружки, отображающие атомы, располагаются в центре куба и по его вершинам (куб объемноцентрированный), или в центрах граней и по вершинам куба (куб гранецентрированный), или в виде шестигранника, внутрь которого наполовину вставлен также шестигранник, три атома верхней плоскости которого находятся внутри шестигранной призмы (гексагональная решетка).
Метод изображения кристаллической решетки, приведенный на рисунке 3, является условным (как в любой другой). Может быть, более правильно изображение атомов в кристаллической решетке в виде соприкасающихся шаров (левые схемы на рисунке 3). Однако такое изображение кристаллической решетки не всегда удобно, чем принятое (правые схемы на рисунке 3).
Размеры кристаллической решетки характеризуются параметрами, или периодами решетки. Кубическую решетку определяет один параметр -- длина ребра куба а (рисунок 3, а, б). Параметры имеют величины порядка атомных размеров и измеряются в ангстремах.
Так например, параметр решетки хрома, имеющего структуру объемноцентрированного куба, равен 2,878 А, а параметр решетки алюминия, имеющего структуру гранецентрированного куба, 4,041 А.
Параметр решетки -- чрезвычайно важная характеристика. Современные методы рентгеновского исследования позволяют измерить параметр с точностью до четвертого или даже пятого знака после запятой, т. е. одной десятитысячной -- одной стотысячной доли ангстрема.
Из рассмотрения схем кристаллических решеток (рисунок 3), если считать, что атомы являются как бы упругими, касающимися друг друга шарами, вытекает, что параметр решетки а и атомный диаметр d связаны простыми геометрическими соотношениями.
Для объемноцентрированного куба
Для гранецентрированного куба
Принимая для атома форму шара, можно подсчитать, что в кубической объемноцентрированной решетке атомы занимают 68% объема, а в кубической гранецентрированной (как и в гексагональной плотноупакованной) 74%, т.е. во втором случае атомы располагаются более плотно, более компактно.
Для металлов распространена гексагональная решетка (рисунок 3, в).
Если слои атомов касаются друг друга, т. е. три атома, изображенные внутри решетки (рисунок 3, в), касаются атомов, расположенных на верхней и нижней плоскостях, то имеем так называемую гексагональную плотноупакованную решетку.
Размеры гексагональной плотноупакованной решетки характеризуются постоянным значением с/а=1,633. При иных значениях с/а получается неплотлоупакованная гексагональная решетка.
Кубическая гранецентрированная и гексагональная решетки представляют самый плотный способ укладки шаров одного диаметра.
Некоторые металлы имеют тетрагональную решетку (рисунок 4); она характеризуется тем, что ребро с не равно ребру а. Отношение этих параметров характеризует так называемую степень тетрагональности. При с/а = 1 получается кубическая решетка. В зависимости от пространственного расположения атомов тетрагональная решетка (как и кубическая) может быть простой, объемноцентрированной и гранецентрированной.

Рисунок 4. Тетрагональная решетка
Существенное значение для свойств данного металла или сплава имеет число атомов, находящихся во взаимном контакте. Это определяется числом атомов, равноотстоящих на ближайшем расстоянии от любого атома.
Число атомов, находящихся на наиболее близком и равном расстоянии от данного атома, называется координационным числом. Так, например, атом в простой кубической решетке имеет шесть ближайших равноотстоящих соседей, т. е. координационное число этой решетки равно 6.
Центральный атом в объемноцентрированной решетке имеет восемь ближайших равноотстоящих соседей, т. е. координационное число этой решетки равно 8. Координационное число для гранецентрированной решетки равно 12. В случае гексагональной плотноупакованной решетки координационное число равно 12, а в случае с/а ? 1,633 каждый атом имеет шесть атомов на одном расстоянии и шесть на другом (координационное число 6).
Для краткого обозначения кристаллической решетки с указанием в этом обозначении типа кристаллической решетки и координационного числа была принята одна из следующих систем (таблица 1).
Гексагональная плотноупакованная 1
Каждый металл обладает определенной кристаллической решеткой.
Существенной характеристикой кристаллической структуры является число атомов, приходящихся на элементарную ячейку.
В о. ц. к. решетке атомы, находящиеся в вершине, принадлежат восьми элементарным ячейкам. Следовательно, каждый атом вносит в данную элементарную ячейку только одну восьмую часть своего объема. Центральный атом полностью принадлежит данной элементарной ячейке. Следовательно, на одну элементарную ячейку приходятся 1/8 * 8+1=2 атома.
В гранецентрированном кубе на одну элементарную ячейку приходятся четыре атома (1/8 ? 8 атом от числа расположенных в вершинах куба + 1/2 ? 6=3 атома из числа центрирующих грани).
Типично металлические элементы, расположенные в левой части таблицы Д. И. Менделеева, кристаллизуются в плотной упаковке, т. е. в простые кристаллические ячейки с большим координационным числом. Типично металлическими решетками являются, как указывалось, решетки о. ц. к., г. ц. к. и г. п. у. Действительно, почти все металлы, начиная от цинка, кадмия и ртути и левее имеют в большинстве случаев простые решетки.
Для неметаллических элементов характерно малое значение координационного числа (К4 и меньше). Неметаллы обладают меньшей плотностью и меньшим удельным весом, чем металлы.
Металлы -- простые вещества, обладающие свободными, не связанными с определенными атомами электронами, которые способны перемещаться по всему объему тела. Эта особенность состояния металлического вещества определяет собой свойства металлов.
Атомы металлов легко отдают внешние (валентные) электроны, превращаясь при этом в положительно заряженные ноны. Отданные атомами свободные электроны непрерывно хаотически, т. е. беспорядочно, перемещаются по всему объему металла. Такие свободные электроны часто называют электронным газом. Положительно заряженные ионы при столкновении со свободными электронами на некоторое время могут превращаться в нейтральные атомы.
Таким образом, металлы состоят из упорядоченно расположенных в пространстве положительно заряженных ионов, перемещающихся среди них электронов и небольшого количества нейтральных атомов. Металлами являются алюминий, железо, медь, никель, хром и т.д.
Сплавы представляют собой системы, состоящие из двух или нескольких металлов или металлов и неметаллов. Сплавы обладают всеми характерными свойствами металлов. Например, сталь и чугун - сплавы железа с углеродом, кремнием, марганцем, фосфором и серой; бронза - сплав меди с оловом или другими элементами; латунь - сплав меди с цинком и другими элементами.
В промышленности широко применяют сплавы, получаемые сплавлением составляющих с последующей кристаллизацией из жидкого состояния, значительно меньше - сплавы, получаемые спеканием.
В процессе кристаллизации из расплавленного (жидкого) состояния металла или сплава положительно заряженные ионы и нейтральные атомы группируются в строго определенной последовательности, образуя кристаллические решетки - правильное упорядоченное расположение атомов в элементарной ячейке. Кристаллические решетки у металлов и сплавов могут быть различных типов: объемно-концентрированные кубические (о. ц. к.), гранецентрированные кубические (г. ц. к.), гексагональные плотноупакованные (г. п. у.). Объемно-концентрированную кубическую решетку образуют железо, медь, алюминий, свинец и др.; гексагональную плотноупакованную- цинк, магний, кобальт и др.
Для характеристики кристаллической решетки необходимо знать периоды решетки - расстояние а и с между центрами атомов или ионов, находящихся в узлах решетки. Период решетки измеряется в ангстремах (1А=10 -8 см).
В процессе кристаллизации положительно заряженные ионы, располагаясь последовательно в виде элементарных кристаллических решеток, образуют кристаллы в виде зерен или дендритов. Все металлы и сплавы имеют кристаллическое строение. Образующиеся кристаллы растут, кристаллизуются из жидкого расплава сначала свободно, не мешают один другому, потом они сталкиваются и рост кристаллов продолжается только в тех направлениях, где есть свободный доступ жидкого металла. В результате первоначальная геометрически правильная форма кристаллов нарушается. После затвердевания зерна и дендриты имеют неправильную, геометрически искаженную форму.
При нагревании поглощаемое металлами тепло расходуется на колебательные движения атомов и вследствие этого на тепловое расширение металла. При плавлении объем металлов увеличивается на 3-4%. С повышением температуры колебательные движения атомов или ионов возрастают, кристаллические зерна распадаются и сплав, проходя через твердо-жидкое состояние, превращается в расплав.
Переход в жидкое состояние не приводит к полному уничтожению кристаллической структуры. В расплаве металлов и сплавов всегда находятся мельчайшие участки, в которых сохраняется первоначальное, наследственное строение металла, близкое к кристаллическому. Кроме того, всегда присутствуют тугоплавкие частицы (остатки футеровки печи, примеси других элементов), которые могут образовывать дополнительные центры кристаллизации и вызывать начало кристаллизации. На искусственном создании центров кристаллизации в расплаве с одновременным изменением его скорости охлаждения основано управление кристаллизации сплава с целью получения заданной структуры сплава в твердом состоянии.
1. Гуляев А.П. Металловедение.- 5-е изд., перераб. и доп. - М.: Издательство "металлургия", 1977.
2. Материаловедение для слесарей-сантехников, слесарей-монтажников, машинистов строительных машин: Учебник для сред. проф.-тех. училищ /Ю.Г.Виноградов, К.С.Орлов, Л.А.Попова. - М.: Высш. школа , 2-е изд., 1989.
3. Материаловедение. Лекция 5. З.О.
4. Мойзберг Р.К. Материаловедение, 1991.
5. Ханапетов М.В. Сварка и резка металлов. - 3-е изд., перераб. и доп. - М.: Стройиздат, 1988.
Читайте также:
