Каждый период кроме первого начинается со щелочного металла
Название «щелочные металлы» произошло от их способности в реакциях с водой образовывать щелочи — основания, растворимые в воде. Слово «выщелачивать» славянского происхождения. В переводе оно означает «растворять».
Щелочными называют металлы IA группы таблицы Менделеева. Их шесть: литий, натрий, рубидий, калий, цезий, франций. По внешнему виду они представляют собой металлы серебристо-белого цвета, за исключением цезия — он золотисто-желтый. Основные физические свойства простых веществ:
- пластичность;
- мягкость;
- невысокая плотность;
- высокая химическая активность;
- легкая окисляемость;
- электропроводность;
- теплопроводность;
- легкоплавкость.
В связи со способностью быстро окисляться, т.е. вступать в реакцию с кислородом и другими веществами, в природе они встречаются в форме соединений.
Соли щелочных металлов окрашивают пламя спиртовки в различные цвета:
В отличие от этих двух представителей, литий, рубидий, цезий не встречаются в природе часто. Следовательно, они относятся к группе редких металлов. Франций — искусственно полученный элемент, отличающийся радиоактивностью.
Калий и натрий являются участниками водно-солевого, а также кислотно-щелочного баланса организма человека. Эти элементы важны для циркуляторных процессов крови, деятельности энзимов. Для жизнедеятельности растений особенно важен калий.
Щелочные металлы имеют валентность, равную единице (степень окисления +1).
Поскольку данная группа элементов в системе Менделеева следует непосредственно за инертными газами, у атомов щелочных металлов появляется новый энергетический уровень, на котором содержится один электрон. Электронная конфигурация — ns1.
Поскольку любой атом стремится приобрести конфигурацию инертного газа, атомы щелочных металлов способны легко отдать валентные электроны и проявлять восстановительные свойства. Этот факт свидетельствует о невысоких значениях энергии ионизации их атомов, а также о низких значениях электроотрицательности.
Сверху вниз по группе наблюдается увеличение радиуса атомов, снижение электроотрицательности, увеличение восстановительных свойств простых веществ.
Какие элементы относятся к щелочным металлам
Перечень щелочных металлов:
- литий — Li;
- натрий — Na;
- калий — K;
- рубидий — Rb;
- цезий — Zs;
- франций — Fr.
Они занимают IA группу в Периодической системе Д. И. Менделеева.
Электронная формула, в какую группу входят
Строение атомов щелочных металлов, которые расположены в IA группе, можно свести к таблице следующего вида:
В роли окислителей в таких взаимодействиях участвуют простые и сложные вещества. Это могут быть неметаллы, органические соединения, кислоты, соли, оксиды.
Каждый элемент взаимодействует индивидуально.
Оксид в качестве продукта образовывается только в реакциях лития:
4 L i + O 2 = 2 L i 2 O
В случае с натрием в ходе реакции образуется пероксид, а с калием, рубидием, цезием — надпероксид:
2 N a + O 2 = N a 2 O 2
- К реакциям с простыми веществами относится образование галогенидов:
2 N a + C l 2 = 2 N a C l
Рассматривая взаимодействие с H2, S, P, C, Si, необходимо знать, что для протекания данных реакций необходимо нагревание.
Литий реагирует с азотом при комнатной температуре.
- Реакции с водой протекают у щелочных металлов по-разному: литий — спокойно, всплывая на поверхность жидкости, натрий реагирует более активно с образованием пламени, калий, цезий и рубидий реагируют со взрывом. В общем виде
2 M + 2 H 2 O = 2 M O H + H 2 (М – металл)
- В два этапа протекают реакции с кислотами. Металл сначала вступает в реакцию с водой, а после, в момент образования щелочи, она реагирует с разбавленной кислотой и нейтрализуется. Такие реакции часто протекают со взрывом, поэтому на практике проводятся редко.
- В результате реакции с аммиаком образуются амиды:
2 L i + 2 N H 3 = 2 L i N H 2 + H 2
- Взаимодействие с этанолом, фенолами, в ходе которого щелочные металлы замещают атомы водорода в гидроксильной группе ОН этих соединений:
2 N a + 2 C 2 H 5 O H = 2 C 2 H 5 O N a + H 2
- Щелочные металлы могут использоваться для восстановления других металлов, к примеру, алюминия:
3 N a + A l C l 3 = A l + 3 N a C l
Физические свойства щелочных металлов объясняются металлической связью в кристаллической решетке. Для них характерен металлический блеск, отличная ковкость, пластичность, тепло- и электропроводность.
Самым твердым из всей группы является литий, а самая высокая плотность у цезия. Некоторые физические свойства щелочных металлов в сравнении представлены в следующей таблице:
Из таблицы следует, что все элементы получили свое применение благодаря низким температурам плавления (кипения). Их значения снижаются по мере увеличения порядкового номера в Периодической системе Менделеева.
Все металлы, за исключением лития, настолько мягки, что их можно разрезать ножом или на специальном оборудовании раскатать в лист фольги.
Еще одно свойство, которое имеет практическое значение в промышленности — низкая плотность. Плотность лития, натрия и калия ниже плотности воды.
Указанные физические свойства обусловлены слабой связью электронов внешних слоев с атомами щелочных металлов. Поэтому энергия ионизации атомов невысокая, и они при взаимодействии друг с другом образуют металлическую связь.
В периодической таблице в начале каждого периода стоит элемент с низкой температурой плавления (щелочной металл). По мере увеличения порядковых номеров в периоде слева направо этот показатель сначала увеличивается к середине периода (IV А группа), где расположены элементы, образующие преимущественно атомные кристаллические решетки (C, Si).
Затем в конце периода температуры плавления снова уменьшаются, поскольку в VII-VIII группах расположены элементы, простые вещества которых характеризуются молекулярными кристаллическими решетками (галогены, благородные газы).
Меры предосторожности при работе с ними
Из-за высокой химической активности работа со щелочными металлами должна осуществляться с большой осторожностью. Для их хранения выделяются отдельные емкости, которые запаивают и помещают в них слой вазелинового масла или керосина. Тогда предотвращается взаимодействие с воздухом, в частности с кислородом, и исключается горение.
На каждом предприятии, где осуществляются работы с этими химическими элементами и их соединениями, разрабатываются специальные правила безопасности и меры предосторожности, исключающие наступление аварийных ситуаций и производственных травм.
Все сотрудники перед получением допуска к работе должны пройти обязательный производственный инструктаж, который бывает предварительный (перед началом работы) и периодический (через равные промежутки времени — ежеквартально, ежегодно). Они включают качественное изучение требований нормативных документов по безопасности труда и производственному нормированию.
Сотрудники на своих рабочих местах должны находиться в защитной спецодежде, быть оснащены средствами индивидуальной защиты (для органов зрения, дыхания, кожных покровов).
Поскольку растворы щелочных металлов — щелочи, их воздействие на кожу может привести к ожогам и раздражениям. Щелочи при попадании брызг в глаза могут спровоцировать отторжение ветвей глазного нерва и вызвать полную слепоту.
Выше описана возможность бурной реакции металлов с кислородом вплоть до взрыва. Поэтому рабочие места укомплектовываются средствами пожаротушения, которые периодически проходят технические проверки своей исправности. Щелочные металлы нельзя тушить водой, так как они вступают в реакцию с ней.
Натрий и калий можно тушить аргоном и азотом. Аргон эффективнее, поскольку существенно тяжелее воздуха. Литий продолжает гореть в атмосфере азота и диоксида углерода. Для тушения горящего лития разработаны специальные порошковые составы Вексон-D3 на основе различных флюсов и графита с гидрофобизирующими добавками.
С соблюдением техники безопасности проводится и утилизация отходов после работы. Они подвергаются нейтрализации с применением специальных составов, разрешенных для применения компетентными органами.
Получение простых веществ, где применяются
Чистый натрий можно получать путем электролиза расплава хлорида натрия с графитовыми электродами, обладающими инертностью. Поскольку в таком расплаве имеются ионы Na и Cl, в ходе электролиза на катоде восстанавливаются катионы натрия до металлического натрия, а на аноде — окисляются анионы хлора до газообразного хлора.
Периодический закон

Существуют две формулировки Периодического закона химических элементов: классическая и современная.
Классическая формулировка (в изложении его первооткрывателя Д.И. Менделеева): свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная формулировка: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением Периодического закона является Периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространенными изображениями Периодической системы элементов Д. И. Менделеева являются короткая и длинная формы.
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгруппы. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Все элементы, кроме гелия, неона и аргона, образуют кислородные соединения, существует всего восемь форм кислородных соединений. В периодической системе их часто изображают общими формулами, расположенными под каждой группой в порядке возрастания степени окисления элементов: R2O, RO, R2O3, RO2, R2O5, RO3, R2O7, RO4, где символом R обозначают элемент данной группы. Формулы высших оксидов относятся ко всем элементам группы, кроме исключительных случаев, когда элементы не проявляют степени окисления, равной номеру группы (например, фтор).
Оксиды состава R2O проявляют сильные оснОвные свойства, причем их основность возрастает с увеличением порядкового номера. Оксиды состава RO (за исключением BeO) проявляют основные свойства.
Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причем их кислотность возрастает с увеличением порядкового номера.
Элементы главных подгрупп, начиная с IV группы, образуют газообразные водородные соединения. Существуют четыре формы таких соединений. Их располагают под элементами главных подгрупп и изображают общими формулами в последовательности RH4, RH3, RH2, RH.
Соединения RH4 имеют нейтральный характер; RH3 — слабоосновный; RH2 — слабокислый; RH — сильнокислый характер.
Свойства элементов в подгруппах закономерно изменяются сверху вниз:
- усиливаются металлические свойства и ослабевают неметаллические;
- возрастает атомный радиус;
- возрастает сила образованных элементом оснований и бескислородных кислот;
- электроотрицательность падает.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвертом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 29 элемента. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Физический смысл порядкового номера химического элемента: число протонов в атомном ядре и число электронов, вращающихся вокруг атомного ядра, равны порядковому номеру элемента.
Современная формулировка периодического закона Д. И. Менделеева
Химические элементы, которых на данный момент насчитывается 118, подчиняются периодическому закону, сформулированному Дмитрием Ивановичем Менделеевым во второй половине XIX века.
Периодический закон Менделеева — в чём суть
Химические элементы, существующие в нашем мире, созданные самой природой или человеком, подчиняются правилу — Периодическому закону, который является основой химической науки.
Периодический закон — закон, который заключается в сопоставлении свойств химических элементов и их атомных масс (в современной формулировке — зарядов ядер).
После открытия в 1869 году Д. И. Менделеевым Периодического закона химических элементов данная наука перестала быть исключительно описательной. Стало возможным научное предвидение.
Суть закона Менделеева заключается в том, что свойства химических элементов, расположенных в таблице, а также свойства образуемых ими соединений находятся в периодической зависимости от зарядов ядер их атомов.
Периодический закон Менделеева был выражен в форме периодической системы элементов.
Периодическая система химических элементов — упорядоченное расположение в таблице химических элементов и их естественная классификация.
Периодическая система химических элементов Д. И. Менделеева состоит из 7 периодов — они представляют собой элементы, расположенные по горизонтали в порядке возрастания атомного номера (заряда ядра), и восьми групп (столбцов).
Периоды делятся на:
Каждый, кроме первого, период начинается со щелочного металла, а заканчивается благородным газом. Слева направо в каждом периоде ослабевают металлические и усиливаются неметаллические свойства, что связано с возрастанием числа электронов на внешнем уровне каждого химического элемента и увеличением прочности их связи с атомом.
Группы делятся на подгруппы:
Сверху вниз в главных подгруппах усиливаются металлические и слабевают неметаллические свойства.
В главных подгруппах вместе с усилением металлических свойств увеличивается устойчивость соединений элементов в низких степенях окисления. В побочных подгруппах с ослабеванием металлических свойств увеличивается устойчивость соединений с высокими степенями окисления.
История открытия, какое имело значение
Первооткрывателем периодического закона является Д. И. Менделеев. Днем, когда был открыт периодический закон, считается 1 марта (17 февраля) 1869 г., когда ученый закончил работу над основным трудом, описавшим данный закон — «Опыт системы элементов, основанной на их атомном весе и химическом свойстве». Тогда с ним за звание первооткрывателя боролся Юлиус Лотар Мейер, который также создал свою систему химических элементов.
Существует легенда о том, что Дмитрий Иванович Менделеев увидел Периодическую систему химических элементов во сне. Однако сам ученый ответил так:
«Я над ней, может быть, двадцать лет думал, а вы думаете: сидел и вдруг… готово».
За основу своей классификации Д. И. Менделеев взял два свойства — химическое сходство элементов и их атомную массу. Ученый расписал на карточках основные свойства каждого элемента, после чего начал многократно переставлять их, чтобы найти закономерность.
Менделеев утверждал, что с ростом атомной массы элементов их свойства меняются, но не монотонно, как считали исследователи до него, а периодически. Свойства начинают повторяться после определенного количества элементов, однако они делают это не точь-в-точь, а с определенными изменениями.
Вторая версия Периодической системы появилась в 1870 году в статье «Естественная система элементов» в «Основах химии». Эта система больше похожа на современную: горизонтальных столбцов стало восемь, периоды остались в изначальном количестве, а каждый период был разбит на 2 ряда — для элементов основной и побочной подгрупп.
Для соблюдения периодичности химических элементов Д. И. Менделеев переписал атомные массы некоторых элементов, расставив их вопреки общим представлениям, а также оставил пустые клетки для неоткрытых элементов.
Первое определение химического закона звучало следующим образом:
Свойства элементов, а потому и свойства образуемых ими простых и сложных тел, состоят в периодической зависимости от их атомного веса.
С помощью составленной периодической системы Д. И. Менделеев смог предсказать открытие новых элементов, а также целый ряд их химических и физических свойств. Подтверждение правильности систематизации появилось уже в 70-80-х годах XIX века, когда были открыт галлий, скандий и германий, которые точно встали в установленные Менделеевым места в Периодической таблице.
Формулирование Периодического закона имело большое значение для развития химии. С открытием Периодической системы химических элементов Д. И. Менделеева мир химической науки перестал быть исключительно описательным, но получил возможность прогнозирования будущих результатов.
Попытки систематизации до него
В середине XIX века научный мир знал о существовании 63 химических элементов. Исследователи предпринимали постоянные попытки систематизирования этих элементов для возможности дальнейшего прогнозирования в химической науке. Это было необходимо для преодоления определенного кризиса — невозможности открывать новые элементы и неимения твердой научной почвы для проведения опытов.
Первым установленную попытку систематизирования химических элементов предпринял Александр Эмиль Шанкуртуа — французский химик, который в 1862 году создал свою систему химических элементов, основанную на закономерности их атомных масс.
Он разместил элементы вдоль винтовой линии — «земной спирали» — которая обращала внимание на циклическую повторяемость свойств элементов.
Данная модель не привлекла внимания общественности, но стала существенным шагом к открытию Периодической системы. Александр Эмиль Шанкуртуа первым обратил внимание на закономерности между атомными массами химических элементов, но не учитывал многих других свойств. Поэтому претензии Шанкуртуа на приоритет в открытии Периодической системы, которые появились у химика после открытия Менделеева, нельзя считать обоснованными.
Джон Александр Ньюлендс в 1866 году предложил свой вариант Периодического закона, который назвал «законом октав». Модель закона напоминала менделеевскую, но при этом в формулировке существовали настойчивые попытки Ньюлендса найти взаимосвязь между химическими элементами и музыкальной гармонией.
По мнению Джона Александра Ньюлендса следовало размещать элементы по порядку возрастания атомных масс, при этом каждый восьмой элемент, как и каждая восьмая нота, должен был стать началом новой строчки. Элементы с одинаковым атомным весом, которые были установлены в то время, располагались под одним номером.
Главной ошибкой ученого был факт того, что некоторые элементы еще не были открыты. Из-за этого система рушилась.
Наиболее близкой к менделеевской системе был вариант Юлиуса Лотара Мейера, который был опубликован в 1864 году. За основу классификации химических элементов ученый взял валентность элементов. В то время еще не было установлено, что валентность не является постоянной для отдельно взятого элемента, из-за чего система не могла быть достоверно точной.
В 1869 году Мейер изменил свою таблицу на сходную с системой Менделеева, из-за чего в западной литературе считается одним из первооткрывателей Периодического закона, либо же ученым, открывшим его независимо от Менделеева.
Современная формулировка
В начале XX века в связи с проводимыми опытами по изучению строения атома было выявлено, что заряд ядра, а не атомная масса, влияет на периодичность изменений свойств элементов. Заряд ядра также влияет на атомный номер и число электронов, распределённых по электронным оболочкам химического элемента.
Современная формулировка в связи с этим отличается от первоначальной:
Свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений, находятся в периодической зависимости от величин зарядов ядер их атомов.
В современной химии главным вопросом остается проблема верхней границы Периодической системы химических элементов Д. И. Менделеева. Последним элементом в таблице на данный момент является элемент номер 118, синтезированный в Дубне в 2002 и 2005 годах, и получивший название Оганесон в 2016 году.
Развитие периодического закона Д. И. Менделеева
В 1869 году, когда был сформулирован Периодический закон, научный мир знал только о 63 элементах. На 2021 год известно 118 элементов, продолжаются попытки получения новых.
Формулировка Периодического закона означала лишь начало развития химии и знаний о периодичности свойств химических элементов. Несмотря на то, что изначально предсказания Менделеева были встречены со скепсисом, в итоге они стали основой для целого ряда химических открытий.
В развитии периодического закона принято выделять 2 периода:
Химический этап связан с открытием элементов Периодической системы, которые предсказал Менделеев:
- 1875 — открытие галлия французским химиком Полем Эмилем Лекок де Буабодраном;
- 1879 — открытие скандия шведским химиком Ларсом Фредериком Нильсоном;
- 1886 — открытие германия немецким химиком Клеменсом Александром Винклером. Позже оказалось, что данный элемент по свойствам совпадает с менделеевским экасилицием;
- 1900-02 — преобразование Периодической системы в связи с появлением в таблице дополнительной группы элементов, включающей инертные газы.
Данное преобразование завершило химический этап развития Периодической системы.
Физический этап развития Периодического закона был начат в связи с тем, что химия не могла в полной мере объяснить причину периодичности свойств химических элементов. Физический этап развития Периодического закона привел к изменениям в естествознании, которые оказали на науку революционное влияние.
Дальнейшее изменение Периодической системы было связано с открытиями физики.
Физический этап можно условно разделить на периоды:
- 1869-97 — открытие электрона, радиоактивности и установление делимости атома;
- 1911-13 — разработка модели атома;
- 1913 — открытие изотопов и разработка их системы, также открытие закона Мозли, позволяющего определять заряд ядра и номер элемента в Периодической системе химических элементов;
- 1921-25 — разработка теории Периодической системы на основании знаний о строении оболочек атомов;
- 1926-32 — квантовая теория строения атома и Периодической системы.
В связи с открытиями физики таблица начала менять свой изначальный облик.
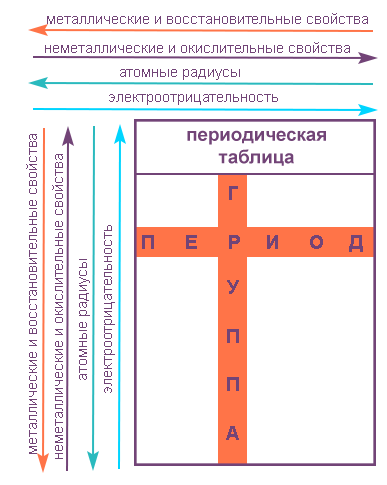
Как изменяются свойства элементов в Периодической таблице
Свойства химических элементов в Периодической таблице зависят от положения каждого элемента в ряду (периоде) и столбце (группе).
Главной характеристикой химического элемента является заряд ядра его атомов.
Периодический закон и Периодическая система химических элементов Д.И. Менделеева

Классическая, в изложении его первооткрывателя Д.И. Менделеева: свойства простых тел, а также формы и свойства соединений элементов находятся в периодической зависимости от величин атомных весов элементов.
Современная: свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от заряда ядра атомов элементов (порядкового номера).
Графическим изображением периодического закона является периодическая система элементов, которая представляет собой естественную классификацию химических элементов, основанную на закономерных изменениях свойств элементов от зарядов их атомов. Наиболее распространёнными изображениями периодической системы элементов Д.И. Менделеева являются короткая и длинная формы.
Группы и периоды Периодической системы. Физический смысл порядкового номера химического элемента
Группами называют вертикальные ряды в периодической системе. В группах элементы объединены по признаку высшей степени окисления в оксидах. Каждая группа состоит из главной и побочной подгрупп. Главные подгруппы включают в себя элементы малых периодов и одинаковые с ним по свойствам элементы больших периодов. Побочные подгруппы состоят только из элементов больших периодов. Химические свойства элементов главных и побочных подгрупп значительно различаются.
Периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров. В периодической системе имеются семь периодов: первый, второй и третий периоды называют малыми, в них содержится соответственно 2, 8 и 8 элементов; остальные периоды называют большими: в четвёртом и пятом периодах расположены по 18 элементов, в шестом — 32, а в седьмом (пока незавершенном) — 31 элемент. Каждый период, кроме первого, начинается щелочным металлом, а заканчивается благородным газом.
Закономерности изменения свойств элементов и их соединений в связи с положением в Периодической системе химических элементов Д.И. Менделеева
Напомним, что группами называют вертикальные ряды в периодической системе и химические свойства элементов главных и побочных подгрупп значительно различаются.
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства.
Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Напомним, что периодом называют горизонтальный ряд элементов, расположенных в порядке возрастания порядковых (атомных) номеров.
В пределах периода с увеличением порядкового номера элемента:
- электроотрицательность возрастает;
- металлические свойства убывают, неметаллические возрастают;
- атомный радиус падает.
Тренировочные задания
1. Среди перечисленных химический элемент с максимальным радиусом атома — это
1) неон
2) алюминий
3) калий
4) кальций
2. Среди перечисленных химический элемент с минимальным радиусом атома — это
1) алюминий
2) бор
3) калий
4) неон
3. Наиболее ярко металлические свойства выражены у элемента
1) Rb
2) Li
3) Mg
4) Ca
4. Наиболее ярко неметаллические свойства выражены у элемента
5. Наибольшее число валентных электронов у элемента
1) фтор
2) водород
3) натрий
4) сера
6. Наименьшее число валентных электронов у элемента
1) кислород
2) кремний
3) водород
4) кальций
7. Металлические свойства элементов возрастают в ряду
1) Ba, Li, Cs, Mg
2) Al, Mg, Ca, K
3) Li, Cs, Mg, Ba
4) Na, Mg, Li, Al
8. Неметаллические свойства элементов ослабевают в ряду:
1) N, S, Br, Cl
2) O, S, Se, Te
3) Se, I, S, O
4) N, P, O, F
9. Химические элементы перечислены в порядке возрастания атомного радиуса в ряду
1) углерод, бериллий, магний
2) калий, магний, алюминий
3) хлор, натрий, фтор
4) азот, фосфор, фтор
10. Химические элементы перечислены в порядке убывания атомного радиуса в ряду
1) водород, бор, алюминий
2) углерод, кремний, калий
3) натрий, хлор, фтор
4) сера, кремний, магний
11. Кислотные свойства водородных соединений усиливаются в ряду
12. Кислотные свойства водородных соединений ослабевают в ряду
13. Основные свойства соединений усиливаются в ряду
1) LiOH – KOH – RbOH
2) LiOH – KOH – Ca(OH)2
3) Ca(OH)2 – KOH – Mg(OH)2
4) LiOH – Ca(OH)2 – KOH
14. Основные свойства соединений ослабевают в ряду
15. Во втором периоде Периодической системы элементов Д.И. Менделеева с увеличением заряда ядра у химических элементов:
1) возрастает электроотрицательность
2) уменьшается заряд ядра
3) возрастает атомный радиус
4) возрастает степень окисления
16. Наиболее сильной кислотой, образованной элементом второго периода, является
1) угольная
2) азотная
3) фтороводородная
4) азотистая
17. Наиболее сильное основание образует химический элемент
1) магний
2) литий
3) алюминий
4) калий
18. Наиболее сильная бескислородная кислота соответствует элементу
1) селен
2) фтор
3) йод
4) сера
19. В ряду элементов Li → B → N → F
1) убывает атомный радиус
2) возрастают металлические свойства
3) уменьшается число протонов в атомном ядре
4) увеличивается число электронных слоёв
20. В ряду элементов Li → Na → K → Rb
1) убывает атомный радиус
2) ослабевают металлические свойства
3) уменьшается число протонов в атомном ядре
4) увеличивается число электронных слоёв
ПЕРИОДИЧЕСКАЯ ТАБЛИЦА МЕНДЕЛЕЕВА
Еще в школе, сидя на уроках химии, все мы помним таблицу на стене класса или химической лаборатории. Эта таблица содержала классификацию всех известных человечеству химических элементов, тех фундаментальных компонентов, из которых состоит Земля и вся Вселенная. Тогда мы и подумать не могли, что таблица Менделеева бесспорно является одним из величайших научных открытий, который является фундаментом нашего современного знания о химии.
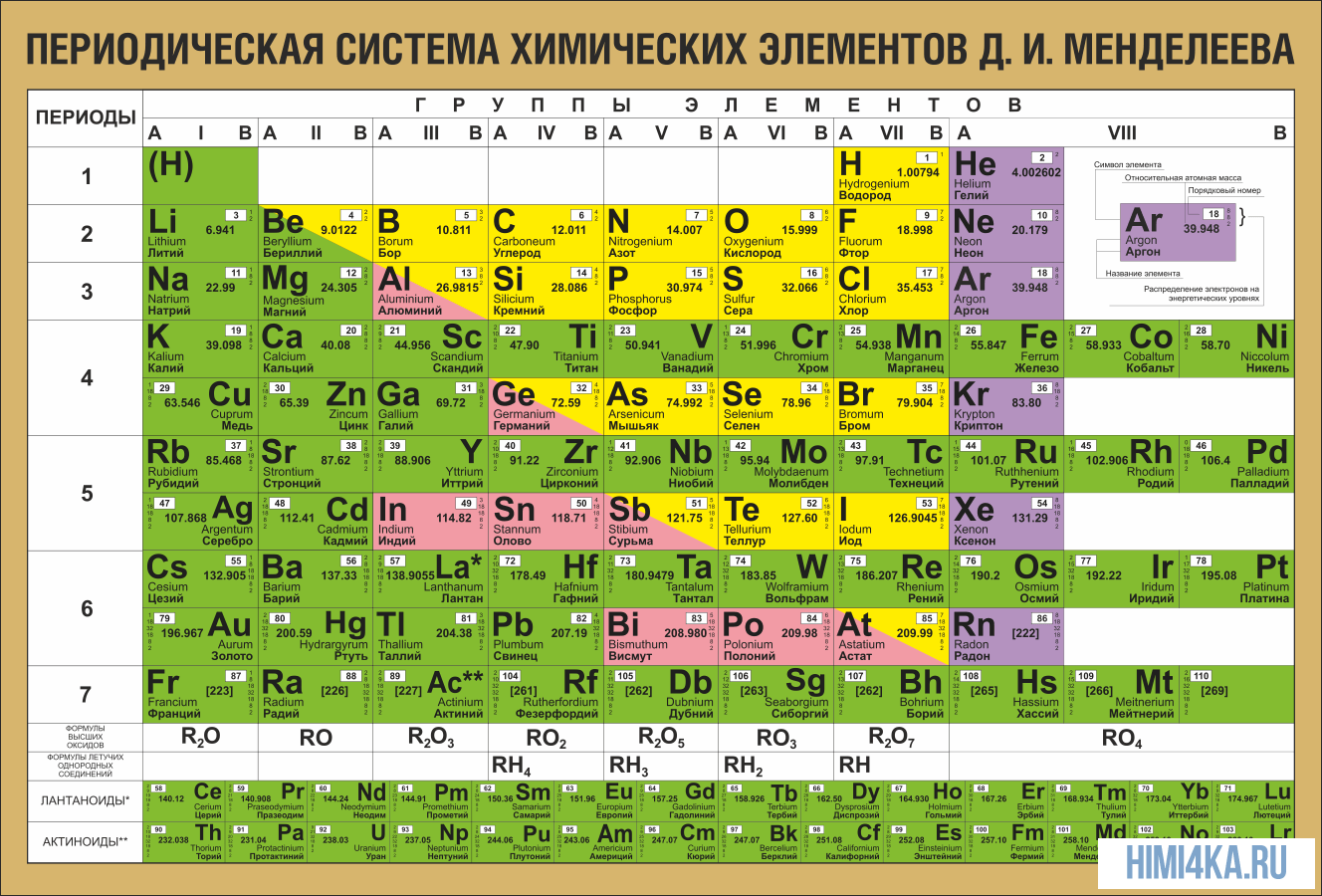
На первый взгляд, ее идея выглядит обманчиво просто: организовать химические элементы в порядке возрастания веса их атомов. Причем в большинстве случаев оказывается, что химические и физические свойства каждого элемента сходны с предыдущим ему в таблице элементом. Эта закономерность проявляется для всех элементов, кроме нескольких самых первых, просто потому что они не имеют перед собой элементов, сходных с ними по атомному весу. Именно благодаря открытию такого свойства мы можем поместить линейную последовательность элементов в таблицу, очень напоминающую настенный календарь, и таким образом объединить огромное количество видов химических элементов в четкой и связной форме. Разумеется, сегодня мы пользуемся понятием атомного числа (количества протонов) для того, чтобы упорядочить систему элементов. Это помогло решить так называемую техническую проблему «пары перестановок», однако не привело к кардинальному изменению вида периодической таблицы.
В периодической таблице Менделеева все элементы упорядочены с учетом их атомного числа, электронной конфигурации и повторяющихся химических свойств. Ряды в таблице называются периодами, а столбцы группами. В первой таблице, датируемой 1869 годом, содержалось всего 60 элементов, теперь же таблицу пришлось увеличить, чтобы поместить 118 элементов, известных нам сегодня.
Периодическая система Менделеева систематизирует не только элементы, но и самые разнообразные их свойства. Химику часто бывает достаточно иметь перед глазами Периодическую таблицу для того, чтобы правильно ответить на множество вопросов (не только экзаменационных, но и научных).
The YouTube ID of 1M7iKKVnPJE is invalid.

Группы и периоды Периодической системы

Свойства таблицы Менделеева
Оксиды состава R2O проявляют сильные основные свойства, причём их основность возрастает с увеличением порядкового номера, оксиды состава RO (за исключением BeO) проявляют основные свойства. Оксиды состава RO2, R2O5, RO3, R2O7 проявляют кислотные свойства, причём их кислотность возрастает с увеличением порядкового номера.
Элементы таблицы Менделеева
Щелочные и щелочноземельные элементы
К ним относятся элементы из первой и второй группы периодической таблицы. Щелочные металлы из первой группы — мягкие металлы, серебристого цвета, хорошо режутся ножом. Все они обладают одним-единственным электроном на внешней оболочке и прекрасно вступают в реакцию. Щелочноземельные металлы из второй группы также имеют серебристый оттенок. На внешнем уровне помещено по два электрона, и, соответственно, эти металлы менее охотно взаимодействуют с другими элементами. По сравнению со щелочными металлами, щелочноземельные металлы плавятся и кипят при более высоких температурах.
| Щелочные металлы | Щелочноземельные металлы |
| Литий Li 3 | Бериллий Be 4 |
| Натрий Na 11 | Магний Mg 12 |
| Калий K 19 | Кальций Ca 20 |
| Рубидий Rb 37 | Стронций Sr 38 |
| Цезий Cs 55 | Барий Ba 56 |
| Франций Fr 87 | Радий Ra 88 |
Лантаниды (редкоземельные элементы) и актиниды
Лантаниды — это группа элементов, изначально обнаруженных в редко встречающихся минералах; отсюда их название «редкоземельные» элементы. Впоследствии выяснилось, что данные элементы не столь редки, как думали вначале, и поэтому редкоземельным элементам было присвоено название лантаниды. Лантаниды и актиниды занимают два блока, которые расположены под основной таблицей элементов. Обе группы включают в себя металлы; все лантаниды (за исключением прометия) нерадиоактивны; актиниды, напротив, радиоактивны.
| Лантаниды | Актиниды |
| Лантан La 57 | Актиний Ac 89 |
| Церий Ce 58 | Торий Th 90 |
| Празеодимий Pr 59 | Протактиний Pa 91 |
| Неодимий Nd 60 | Уран U 92 |
| Прометий Pm 61 | Нептуний Np 93 |
| Самарий Sm 62 | Плутоний Pu 94 |
| Европий Eu 63 | Америций Am 95 |
| Гадолиний Gd 64 | Кюрий Cm 96 |
| Тербий Tb 65 | Берклий Bk 97 |
| Диспрозий Dy 66 | Калифорний Cf 98 |
| Гольмий Ho 67 | Эйнштейний Es 99 |
| Эрбий Er 68 | Фермий Fm 100 |
| Тулий Tm 69 | Менделевий Md 101 |
| Иттербий Yb 70 | Нобелий No 102 |
Галогены и благородные газы
Галогены и благородные газы объединены в группы 17 и 18 периодической таблицы. Галогены представляют собой неметаллические элементы, все они имеют семь электронов во внешней оболочке. В благородных газахвсе электроны находятся во внешней оболочке, таким образом с трудом участвуют в образовании соединений. Эти газы называют «благородными, потому что они редко вступают в реакцию с прочими элементами; т. е. ссылаются на представителей благородной касты, которые традиционно сторонились других людей в обществе.
| Галогены | Благородные газы |
| Фтор F 9 | Гелий He 2 |
| Хлор Cl 17 | Неон Ne 10 |
| Бром Br 35 | Аргон Ar 18 |
| Йод I 53 | Криптон Kr 36 |
| Астат At 85 | Ксенон Xe 54 |
| — | Радон Rn 86 |
Переходные металлы
Переходные металлы занимают группы 3—12 в периодической таблице. Большинство из них плотные, твердые, с хорошей электро- и теплопроводностью. Их валентные электроны (при помощи которых они соединяются с другими элементами) находятся в нескольких электронных оболочках.
| Переходные металлы |
| Скандий Sc 21 |
| Титан Ti 22 |
| Ванадий V 23 |
| Хром Cr 24 |
| Марганец Mn 25 |
| Железо Fe 26 |
| Кобальт Co 27 |
| Никель Ni 28 |
| Медь Cu 29 |
| Цинк Zn 30 |
| Иттрий Y 39 |
| Цирконий Zr 40 |
| Ниобий Nb 41 |
| Молибден Mo 42 |
| Технеций Tc 43 |
| Рутений Ru 44 |
| Родий Rh 45 |
| Палладий Pd 46 |
| Серебро Ag 47 |
| Кадмий Cd 48 |
| Лютеций Lu 71 |
| Гафний Hf 72 |
| Тантал Ta 73 |
| Вольфрам W 74 |
| Рений Re 75 |
| Осмий Os 76 |
| Иридий Ir 77 |
| Платина Pt 78 |
| Золото Au 79 |
| Ртуть Hg 80 |
| Лоуренсий Lr 103 |
| Резерфордий Rf 104 |
| Дубний Db 105 |
| Сиборгий Sg 106 |
| Борий Bh 107 |
| Хассий Hs 108 |
| Мейтнерий Mt 109 |
| Дармштадтий Ds 110 |
| Рентгений Rg 111 |
| Коперниций Cn 112 |
Металлоиды
Металлоиды занимают группы 13—16 периодической таблицы. Такие металлоиды, как бор, германий и кремний, являются полупроводниками и используются для изготовления компьютерных чипов и плат.
| Металлоиды |
| Бор B 5 |
| Кремний Si 14 |
| Германий Ge 32 |
| Мышьяк As 33 |
| Сурьма Sb 51 |
| Теллур Te 52 |
| Полоний Po 84 |
Постпереходными металлами
Элементы, называемые постпереходными металлами, относятся к группам 13—15 периодической таблицы. В отличие от металлов, они не имеют блеска, а имеют матовую окраску. В сравнении с переходными металлами постпереходные металлы более мягкие, имеют более низкую температуру плавления и кипения, более высокую электроотрицательность. Их валентные электроны, с помощью которых они присоединяют другие элементы, располагаются только на внешней электронной оболочке. Элементы группы постпереходных металлов имеют гораздо более высокую температуру кипения, чем металлоиды.
| Постпереходные металлы |
| Алюминий Al 13 |
| Галлий Ga 31 |
| Индий In 49 |
| Олово Sn 50 |
| Таллий Tl 81 |
| Свинец Pb 82 |
| Висмут Bi 83 |
Неметаллы
Из всех элементов, классифицируемых как неметаллы, водород относится к 1-й группе периодической таблицы, а остальные — к группам 13—18. Неметаллы не являются хорошими проводниками тепла и электричества. Обычно при комнатной температуре они пребывают в газообразном (водород или кислород) или твердом состоянии (углерод).
| Неметаллы |
| Водород H 1 |
| Углерод C 6 |
| Азот N 7 |
| Кислород O 8 |
| Фосфор P 15 |
| Сера S 16 |
| Селен Se 34 |
| Флеровий Fl 114 |
| Унунсептий Uus 117 |
А теперь закрепите полученные знания, посмотрев видео про таблицу Менделеева и не только.
Отлично, первый шаг на пути к знаниям сделан. Теперь вы более-менее ориентируетесь в таблице Менделеева и это вам очень даже пригодится, ведь Периодическая система Менделеева является фундаментом, на котором стоит эта удивительная наука.
Читайте также:
