Какой вид химической связи и тип кристаллической решетки характерны для металлов как простых веществ
В зависимости от вида частиц и от характера связи между ними различают четыре типа кристаллических решеток: ионные, молекулярные, атомные и металлические.
Ионные кристаллические решетки
Виды частиц в узлах решетки: ионы
Для веществ с ионной химической связью будет характерна ионная решетка.
Ионы-это частицы, имеющие положительный или отрицательный заряд.
Напрмер NaCl, Соли, галогениды (IA,IIA),оксиды и гидроксиды типичных металлов.
Физ. свойства: Твердые, прочные, нелетучие, хрупкие, тугоплавкие, многие растворимы в воде, расплавы проводят электрический ток
Атомные кристаллические решетки
В узлах атомной кристаллической решетки находятся отдельные атомы.
Ковалентная химическая связь.
В данных решетках молекулы отсутствуют. Весь кристалл следует рассматривать как гигантскую молекулу. Примером веществ с таким типом кристаллических решеток могут служить аллотропные модификации углерода: алмаз, графит; а также бор, кремний, красный фосфор, германий. Простые по составу.
Атомные кристаллические решетки имеют не только простые, но и сложные. Например, оксид алюминия, оксид кремния. Все эти вещества имеют очень высокие температуры плавления (у алмаза свыше 35000С) , прочны и тверды, нелетучи, практически нерастворимы в жидкостях.
Металлические кристаллические решетки
Металлическая связь. Связь в металлах между положительными ионами посредством обобществленных электронов.
общие физические свойства для металлов характерны: блеск, электропроводность, теплопроводность, пластичность.
Вещества с металлической связью имеют металлические кристаллические решетки
В узлах таких решеток находятся атомы и положительные ионы металлов, а в объеме кристалла свободно перемещаются валентные электроны. Электроны электростатически притягивают положительные ионы металлов. Этим объясняется стабильность решетки.
Молекулярные кристаллические решетки
Эти вещества являются неметаллами. Простые по составу. Химическая связь внутри молекул ковалентная неполярная. Летучие, легкоплавкие, малорастворимые в воде.
в узлах решетки нах. молекулы.
молекулярную кристаллическую решетку могут иметь не только твердые простые вещества: благородные газы, H2,O2,N2, I2, O3, белый фосфор Р4, но и сложные: твердая вода, твердые хлороводород и сероводород. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар) .
В узлах решеток находятся неполярные или полярные молекулы. Несмотря на то, что атомы внутри молекул связаны прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного взаимодействия.
ИОННЫЕ
Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов.
Связи между ионами в кристалле очень прочные и устойчивые. Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
АТОМНЫЕ
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями.
В природе встречается немного веществ с атомной кристаллической решёткой. К ним относятся бор, кремний, германий, кварц, алмаз. Вещества с АКР имеют высокие температуры плавления, обладают повышенной твёрдостью. Алмаз-самый твёрдый природный материал.
МОЛЕКУЛЯРНЫЕ
Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них ковалентные, как полярные, так и неполярные. Связи в молекулах прочные, но между молекулами связи не прочные.
Вещества с МКР имеют малую твёрдость, плавятся при низкой температуре, летучие, при обычных условиях находятся в газообразном или жидком состоянии
МЕТАЛЛИЧЕСКИЕ
Металлическими называют решётки, в узлах которых находятся атомы и ионы металла.
Для металлов характерны физические свойства: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность
молекулярная кристаллическая решетка, в узлах которой распологаются молекулы, например Cl2,I2,H2, Br2 и т. д
атомная кристаллическая решетка, в узлах которой находятся отдельные атомы, которые соединены очень прочными ковалентными связями, например алмаз
металлическая кристаллическая решетка, в узлах которой распологаются атомы и ионы металла, ну это все металлы Na, K, Mg, Ca и другие
ионная кристаллическая решетка в узлах которой находятся ионы, их образуют вещества с ионной связью. это соли, некоторые оксиды и гидроксиды металлов, самый простой пример NaCl, KI

Молекулярные кристаллические решетки
Эти вещества являются неметаллами. Простые по составу. Химическая связь внутри молекул ковалентная неполярная. Летучие, легкоплавкие, малорастворимые в воде.
в узлах решетки нах. молекулы.
молекулярную кристаллическую решетку могут иметь не только твердые простые вещества: благородные газы, H2,O2,N2, I2, O3, белый фосфор Р4, но и сложные: твердая вода, твердые хлороводород и сероводород. Большинство твердых органических соединений имеют молекулярные кристаллические решетки (нафталин, глюкоза, сахар) .
В узлах решеток находятся неполярные или полярные молекулы. Несмотря на то, что атомы внутри молекул связаны прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного взаимодействияв узлах атомных кристаллических решеток находятся отдельные атомы
Ионные кристаллические решетки
Данные типы кристаллических решеток присутствуют в соединениях с ионным типом связи. В этом случае узлы решетки содержат ионы, обладающие противоположным электрическим зарядом. Благодаря электромагнитному полю, силы межионного взаимодействия оказываются достаточно сильными, и это обуславливает физические свойства вещества. Обычными характеристиками являются тугоплавкость, плотность, твердость и возможность проводить электрический ток. Ионные типы кристаллических решеток имеются у таких веществ, как поваренная соль, нитрат калия и прочие. физические типы кристаллических решеток
Атомные кристаллические решетки
Этот тип строения вещества присущ элементам, структуру которых определяет ковалентная химическая связь. Типы кристаллических решеток подобного рода содержат в узлах отдельные атомы, связанные между собой крепкими ковалентными связями. Подобный тип связи возникает тогда, когда два одинаковых атома «делятся» электронами, тем самым образуют общую пару электронов для соседних атомов. Благодаря такому взаимодействию ковалентные связи равномерно и сильно связывают атомы в определенном порядке. Химические элементы, которые содержат атомные типы кристаллических решеток, обладают твердостью, высокой температурой плавления, плохо проводят электрический ток и химически неактивны. Классическими примерами элементов с подобным внутренним строением можно назвать алмаз, кремний, германий, бор.
ЧТО ДЕЛАТЬ В СЛУЧАЕ ОХРИПЛОСТИ ИЛИ ПОТЕРИ ГОЛОСА?
Голос человека – настоящее сокровище, которое многие не берегут. Важнейшим фактором, который влияет на голос, является состояние ЛОР-органов. Поэтому ларингит сопровождается охриплостью и даже полной потерей голоса. В случае потери голоса следует…
Читать далее.
SlickJump®
Есть противопоказания. Посоветуйтесь с врачом.
Молекулярные кристаллические решетки
Вещества, имеющие молекулярный тип кристаллической решетки, представляют собой систему устойчивых, взаимодействующих, плотноупакованных между собой молекул, которые расположены в узлах кристаллической решетки. В подобных соединениях молекулы сохраняют свое пространственное положение в газообразной, жидкой и твердой фазе. В узлах кристалла молекулы удерживаются слабыми ван-дер-ваальсовыми силами, которые в десятки раз слабее сил ионного взаимодействия. молекулярный тип кристаллической решетки
Образующие кристалл молекулы могут быть как полярными, так и неполярными. Из-за спонтанного движения электронов и колебания ядер в молекулах электрическое равновесие может смещаться – так возникает мгновенный электрический момент диполя. Соответствующим образом ориентированные диполи создают силы притяжения в решетке. Двуокись углерода и парафин являются типичными примерами элементов с молекуляной кристаллической решеткой.
Женская грудь требует особого внимания и заботы.
Не секрет, что мастопатия — это широко распространенное заболевание, от которого страдают многие женщины. Но не все знают, что его развитие может быть фоном для возникновения более серьезных.
Читать далее.
SlickJump®
Металлические кристаллические решетки
Металлическая связь гибче и пластичней ионной, хотя может показаться, что обе они базируются на одном и том же принципе. Типы кристаллических решеток металлов объясняют их типичные свойства – такие, например, как механическая прочность, тепло- и электропроводность, плавкость.
Отличительной особенностью металлической кристаллической решетки является наличие положительно заряженных ионов металла (катионов) в узлах этой решетки. Между узлами находятся электроны, которые непосредственно участвуют в создании электрического поля вокруг решетки. Количество электронов, перемещающихся внутри этой кристаллической решетки, называется электронным газом. типы кри
Металлическая химическая связь - характеристика, способы образования и свойства
Металлическая химическая связь характерна для металлов и их сплавов в кристаллическом состоянии. Образуется за счет обобществления валентных электронов. Для этого типа строения вещества не характерно образование направленных структурированных связей.
Следует отличать различные типы связи элементов кристаллов - металлическую, ионную и водородную, свойственную кристаллам льда.
Схема образования металлической связи на примерах
Механизм создания металлической связи предусматривает отрыв частично свободных электронов от атома с образованием катионов с положительным зарядом, формирующих “остов” кристаллической решетки и электронного облака. При этом металлический кристалл не приобретает положительного или отрицательного заряда.
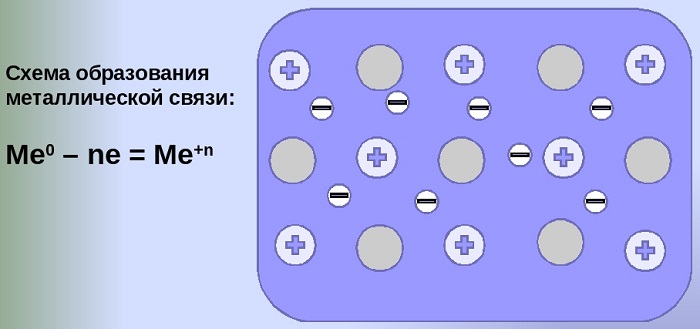
Общий случай формирования связывания металлических атомов в химии, соответствующий данному выше определению:
здесь n - число электронов, участвующих в образовании связи, как правило, от 1 до 3.
В левой части уравнения - атом металла, отдающий электроны, в правой - образовавшийся в результате ион.
Формула показывает, что в кристалле постоянно происходит присоединение и отдача электронов.
Схемы формирования связи на примере атомов различной валентности:
- K - e⁻ ⇆ K;
- Cu - 2e⁻ ⇆ Cu;
- Al - 3e⁻ ⇆ Al.
Отделяющиеся от атома электроны перемещаются на свободные валентные орбитали, которые обобществляются и позволяют всем электронам перемещаться в пределах кристалла. Отделение электронов выгодно атому с точки зрения энергетического баланса, так как позволяет сформировать электронно-стабильную оболочку.
Характерные кристаллические решетки
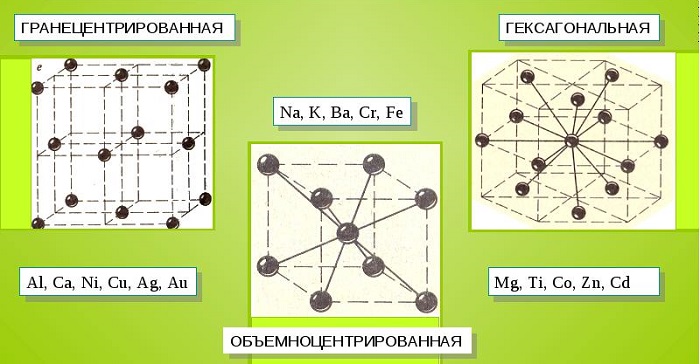
Металлические кристаллы подразделяются на 3 основных типа:
- Объемно-центрированную кубическую решетку, в которой, помимо размещения атомов в четырех вершинах куба, один из них размещается в центре объемной фигуры. Такой тип организации твердого вещества характерен для ряда металлов, включая K, Na и Li, вольфрам, хром, ниобий и др.
- Гранецентрированная кубическая решетка характеризуется расположением атомов в центре граней. Всего в ячейке задействовано 10 атомов, 4 в вершинах и 6 на гранях. Такая решетка встречается у меди, драгметаллов (серебра и золота) и металлов платиновой группы: Pd, Pt.
- Гексагональное строение решетки предполагает размещение атомов в углах и внутри 6-гранной призмы. Ячейка состоит из 15 атомов и свойственна магнию, кальцию, осмию, бериллию и ряду других металлических элементов.
Общими свойствами всех решеток являются высокая симметрия и плотная упаковка составляющих их атомов. Некоторые элементы периодической таблицы формируют уникальную структуру, например, элементарная ячейка In имеет тетрагональное строение.
Для сплавов, являющихся химическими соединениями, также характерно образование кристаллов перечисленных видов, при этом атомы каждого металла занимают определенное место в структуре.
Например, в сплаве никеля и алюминия атомы Al размещаются по углам, а атом Ni - в центре ОЦК ячейки. Свойства сплава и его структура влияют на класс прочности изделия, изготовленного из этого материала.
Физические свойства металлической связи
Физические характеристики металлических кристаллов обусловлены способностью обобществленных электронов свободно перемещаться внутри кристалла.

Характеристики, отличающие подобные вещества:
хорошая электропроводность, благодаря наличию условно свободного электронного облака;
высокая проводимость тепла;
низкая реакционная способность или инертность;
пластичность - большинство металлов можно гнуть и ковать.
Высокий уровень организации вещества обусловливает металлический блеск. Следует иметь в виду, что повышение прочности при пластической деформации и легировании приводит к образованию частично ковалентной связи.
При деформации могут возникать области повышенной прочности и низкими пластическими свойствами, похожие на вещества с ковалентной связью (например, алмаз).
Сходства и отличия металлической химической связи от ионной
Помимо рассматриваемой, металлы могут образовывать другие виды связи, включая простую ионную.
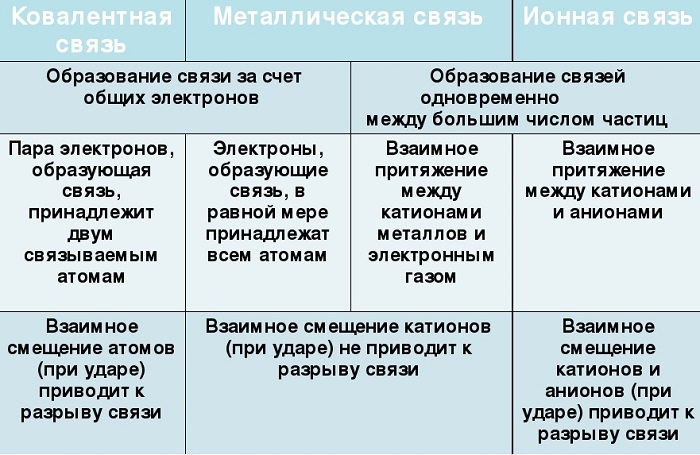
Их общие черты:
участие металлов, при этом металлическая связь формируется исключительно атомами металла, а ионная образуется между металлическим и неметаллическим элементами;
металл высвобождает электроны и становится катионом;
соединения могут существовать в кристаллической форме.
Кристаллы с ионным характером соединения отличают следующие параметры:
- В узлах размещаются как положительно, так и отрицательно заряженные ионы. Каркас металлической решетки формируют исключительно катионы.
- Узлы удерживаются за счет электростатического взаимодействия.
- При низких температурах кристаллические вещества, образованные за счет ионного взаимодействия, проявляют свойства диэлектриков (не проводят ток).
- Переход электронов с атома металла происходит на орбиты атома неметалла.
Характерный пример кристалла с ионной связью - поваренная соль, решетка которой сформирована из ионов Na⁺ и Cl⁻. Такие кристаллические вещества не обладают пластичностью и блеском.
"Какой вид химической связи и тип кристаллической решетки характерны для металлов как простых веществ?
"Какой вид химической связи и тип кристаллической решетки характерны для металлов как простых веществ?

Звязи - Металлическая химическая связь.

Какой вид химической связи и тип кристаллической решётки характерны для вещества твёрдого, тугоплавкого, растворимого в воде?
Какой вид химической связи и тип кристаллической решётки характерны для вещества твёрдого, тугоплавкого, растворимого в воде?

Определите вид химической связи и тип кристаллической решетки для следующих веществ : CIF3, Br2?
Определите вид химической связи и тип кристаллической решетки для следующих веществ : CIF3, Br2.

Простое вещество, Литий - это металл?
Простое вещество, Литий - это металл.
Он имеет (13 букв) кристаллическую решетку и (13 букв) химическую связь, образование которой можно изобразить схемой : .

Помогите пожалуйста?
Срочно надо Определите вид химической связи и тип кристаллической решетки в следующих веществах : фторид калия, вода(лед), алмаз, кислород, бромид натрия.

Составте схему образования соединения серы с водородом?
Составте схему образования соединения серы с водородом.
Определите , вид химической связи в нем, обозначьте частичные заряды на атомах.
Какой тип кристаллической решетки у этого вещества?
Опишите физические свойства, соответствующие типу кристаллической решетке.
1. какой тип кристаллической решетки и вид химической связи наиболее характерны для большинства органических веществ 2?
1. какой тип кристаллической решетки и вид химической связи наиболее характерны для большинства органических веществ 2.
Каковы особенности органических веществ (в сравнении с неорганическими)?
Щелочные металлы : состав, тип и класс веществ, тип химической связи схема ее образования, тип кристаллической решетки?
Щелочные металлы : состав, тип и класс веществ, тип химической связи схема ее образования, тип кристаллической решетки.

Вид связи и тип кристаллической решетки характерны для щелочных металлов?
Вид связи и тип кристаллической решетки характерны для щелочных металлов.
По формуле определите тип химической связи, тип кристаллической решетки, класс, к которому относится вещество, его физические и химические свойства : NaOH?
По формуле определите тип химической связи, тип кристаллической решетки, класс, к которому относится вещество, его физические и химические свойства : NaOH.

Сравните свойства простых веществ - неметаллов и металлов по плану : а) кристаллическая решетка и химическая связь ; б) физические свойства?
Сравните свойства простых веществ - неметаллов и металлов по плану : а) кристаллическая решетка и химическая связь ; б) физические свойства.
Вы открыли страницу вопроса "Какой вид химической связи и тип кристаллической решетки характерны для металлов как простых веществ?. Он относится к категории Химия. Уровень сложности вопроса – для учащихся 10 - 11 классов. Удобный и простой интерфейс сайта поможет найти максимально исчерпывающие ответы по интересующей теме. Чтобы получить наиболее развернутый ответ, можно просмотреть другие, похожие вопросы в категории Химия, воспользовавшись поисковой системой, или ознакомиться с ответами других пользователей. Для расширения границ поиска создайте новый вопрос, используя ключевые слова. Введите его в строку, нажав кнопку вверху.
Я про алюминийАлюминий – легкий, прочный и пластичный металл. Это один из самых востребованных металлов, и по темпам роста потребления он давно и с большим отрывом оставил позади сталь, никель, медь и цинк. Алюминий без преувеличений можно назвать ..
Тому що рН показує ступінь концентрації катіонів гідрогену у воді, що є дуже важливим для косметики.
1. дано N(NH3) = 4. 816 * 10 ^ 23 - - - - - - - - - - - - - - - - - - - - - - - - - - - - - V(NH3) - ? N(NH3) / N(A) = V(NH3) / Vm V(NH3) = N(NH3) * Vm / N(A) = 4. 816 * 10 ^ 23 * 22. 4 / 6. 02 * 10 ^ 23 = 15. 58 L ответ 15. 58 л 2) дано m(O2)..
Соотвественно правильным ответом будет являться : 4) KCl ; 5) AgCl ; 6) NH4Cl.
Дано W(O) = 47 % - - - - - - - - - - - - - - - - E - ? Е - это неизвестный элемент W(O) = Ar(O) * n / M(X2O3) * 100% 47% = 16 * 3 / 2x + 48 * 100% 94x + 2256 = 4800 X = 27 - это алюминий Al2O3 ответ алюминий.
Напиши нормально не понятно или сфоткай.
В SO3 32 / (32 + 3 * 16) = 0, 4 или 40 %.

Реакции есть на фотографии.

4HCl + MnO2 = MnCl2 + Cl2 + 2H2O соляная кислота отдаёт в свободном виде половину имеющегося хлора. M(Cl общ. ) = 1000 * 0, 365 * 0, 9726 = 355 г масса выделившегося хлора = 355 / 2 = 177, 5 г.
Типы химической реакции соединение, разложение замещение.
© 2000-2022. При полном или частичном использовании материалов ссылка обязательна. 16+
Сайт защищён технологией reCAPTCHA, к которой применяются Политика конфиденциальности и Условия использования от Google.
Определите вид химической связи и тип кристаллической решетки в следующих веществах : графит, хлорид кальция, хлороводород , "сухой лёд", фторид лития?
Определите вид химической связи и тип кристаллической решетки в следующих веществах : графит, хлорид кальция, хлороводород , "сухой лёд", фторид лития.
Графит это аллотропная модификация углерода (С), неметалла, значит связь здесь ковалентная неполярная(кристаллическая решётка - атомная).
KCl это соль, значит связь здесь ионная.
( тип кристаллической решётки тоже ионный).
HCl - это связь двух разным неметаллов, значит она ковалентная полярная ( тип кристаллической решётки - молекулярная).
Сухой лёд - это CO2.
Связь здесь ковалентная полярная и тип кристаллической решётки молекулярный.
LiF - это соль, значит связь здесь ионная и тип кристаллической решётки тоже ионный.
Определить тип химической связи в следующих веществах : а) фторид цезия CsF б) гидрид лития LiH в) йоид калия Kl?
Определить тип химической связи в следующих веществах : а) фторид цезия CsF б) гидрид лития LiH в) йоид калия Kl.
Какой тип кристаллической решетки характерен для этих веществ : хлорид калия, графит, сахар, кислород, алмаз?
Какой тип кристаллической решетки характерен для этих веществ : хлорид калия, графит, сахар, кислород, алмаз?
Какой тип кристаллической решетки характерен для следующих веществ : хлорид калия, графит, сахар, йод, сульфид натрия?
Какой тип кристаллической решетки характерен для следующих веществ : хлорид калия, графит, сахар, йод, сульфид натрия?
Нужен вид химической связи и тип кристаллической решётки для веществ : ацетилен, этанол, гидроксид лития?
Нужен вид химической связи и тип кристаллической решётки для веществ : ацетилен, этанол, гидроксид лития.
Определите химическую связь и тип кристаллической решетки у следующих веществ : азотная кислота , гидроксид натрия, гидроксид лития, гидроксид калия ?
Определите химическую связь и тип кристаллической решетки у следующих веществ : азотная кислота , гидроксид натрия, гидроксид лития, гидроксид калия .
На этой странице находится вопрос Определите вид химической связи и тип кристаллической решетки в следующих веществах : графит, хлорид кальция, хлороводород , "сухой лёд", фторид лития?, относящийся к категории Химия. По уровню сложности данный вопрос соответствует знаниям учащихся 5 - 9 классов. Здесь вы найдете правильный ответ, сможете обсудить и сверить свой вариант ответа с мнениями пользователями сайта. С помощью автоматического поиска на этой же странице можно найти похожие вопросы и ответы на них в категории Химия. Если ответы вызывают сомнение, сформулируйте вопрос иначе. Для этого нажмите кнопку вверху.
Ионными кристаллическими решеткаминазывают кристаллические решетки, в узлах которых находятся ионы.
Их образуют вещества с ионной связью.
Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов.
Связи между ионами в кристалле очень прочные и устойчивые.
Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи, чаще всего растворимы в воде.
Тип химической связи и кристаллической решётки у простого вещества - ковалентная неполярная химическая связь или _ _ _ _ _ _ _ _ _ _ _ _ _ и схема её образования ; - тип решётки(_ _ _ _ _ _ _, _ _ _ _?
Тип химической связи и кристаллической решётки у простого вещества - ковалентная неполярная химическая связь или _ _ _ _ _ _ _ _ _ _ _ _ _ и схема её образования ; - тип решётки
(_ _ _ _ _ _ _, _ _ _ _ _ _ _ _ _ _ _ _ или _ _ _ _ _ _ _ _ _ _ _ _ _)
Помогите вставить пропущенные слова .
Дайте характеристику медного купороса 1)вид связи 2) тип кристаллической решётки 3)химические свойства?
Дайте характеристику медного купороса 1)вид связи 2) тип кристаллической решётки 3)химические свойства.
Люди срочно надо ?
Люди срочно надо .
Определить вид химической связи и тип кристаллической решётки у веществ : CaС, H2, NaJ, PCl , Сl, CO2 ?
Определить вид химической связи и тип кристаллической решётке KCL и H2?
Определить вид химической связи и тип кристаллической решётке KCL и H2.
Приведите пример (формула) химических веществ 1) с металлической кристалической решёткой 2) с атомной кристалической решёткой 3) укажите тип кристаллической решётки у воды?
Приведите пример (формула) химических веществ 1) с металлической кристалической решёткой 2) с атомной кристалической решёткой 3) укажите тип кристаллической решётки у воды.
Определите вид химической связи, тип кристаллической решётки бромид кальция, гидрид серы, оксид серы4, алмаз Жизнь или смерть?
Определите вид химической связи, тип кристаллической решётки бромид кальция, гидрид серы, оксид серы4, алмаз Жизнь или смерть.
Читайте также:
