Какой из этих химических элементов не относится к платиновым металлам
МЕТАЛЛЫ — это вещества, обладающие высокой электропроводностью и теплопроводностью, ковкостью, пластичностью и металлическим блеском. Эти характерные свойства металла обусловлены наличием свободно перемещающихся электронов в его кристаллической решетке. Из известных в настоящее время 107 химических элементов 85 относятся к металлам.
Деление всех химических элементов периодической системы Д. И. Менделеева на металлы и неметаллы является условным. Если в периодической таблице провести диагональ через бор и астат, то в главных подгруппах, расположенных справа от диагонали, будут неметаллы, а в главных подгруппах слева от диагонали, побочных подгруппах и в восьмой группе (кроме инертных газов) — металлы. Причем элементы рядом с разделительной линией являются так называемыми металлоидами, т. е. веществами с промежуточными свойствами (металлов и неметаллов) . К ним относятся: бор В, кремний Si, германий Gе, мышьяк Аs, сурьма Sb, теллур Те, полоний Ро.
В соответствии с местом, занимаемым в периодической системе, различают переходные (элементы побочных подгрупп) и непереходные металлы (элементы главных подгрупп) . Металлы главных подгрупп характеризуются тем, что в их атомах происходит последовательное заполнение электронных s- и р-подуровней. В атомах металлов побочных подгрупп происходит достраивание d- и f-подуровней.
Неметаллы - Это химические элементы, которые образуют в свободном виде простые вещества, не обладающие физическими свойствами металлов.
Из известных химических элементов только 22 являются неметаллами. Если провести условную диагональ в переодической системе от берилия к астату, неметаллы окажутся над ней т. е. они находятся в правом верхнем углу.
Атомы неметаллов ( по сравнению с атомами металлов) содержат большее число электронов на внешнем энергетическом уровне, по этому простые вещества - неметаллы обладают, как правило, окислительно - восстановительной деятельностью (кроме фтора и кислорода, которые являются окислителями)
Неметаллы различны по своему агрегатному состоянию. Многие из них газы (кислород, азот, гелий, водород, неон, ксенон, криптон и т. д.). Твердые вещества (фосфор, фтор, йод, бор и т. д.). Бром является жидкостью.
Для неметаллов характерно явление аллотропии. многие из них существуют в виде аллотропных видоизменений, например - фосфор, углерод, кислород, сера и т. д.
Неметаллы имеют различные типы кристаллической решетки - атомную (бор, кремний, углерод в виде алмаза) и молекулярную (йод, белый фосфор, сера кристаллическая)
Физические свойства неметаллов зависят от типа решетки. Вещества с молекулярной решеткой - летучие, легкоплавкие, непрочные, с незначительной растворимостью в воде.
Кароче, там есть такая таблица металлов (такая полосочка, начинаеться Литем (кажись) а заканчиваеться чем-то тяжёлым) .
Основным признаком что эллемент - металл, являеться слабая связь электронов последнего уровня с ядром, они (металлы) могут эти электроны отдавать.
С этим связна причина их электропроводности.
проще говоря, металлы, это те элементы, которые на внешнем электронном уровне имеют 1-3 электрона, т. е. при взаимодействии с другими элементами, , они легко отдают эти электроны. Это 1, 2, 3 группа (гл. подг) перидической системы
А неметаллы, это те элементы, которые имеют почти завершенный электронный уровень, которым не хватает до завершения 1-3 электрона. Это 5,6,7 группа
Какие химические элементы являются металлами и какие являются неметаллами?
Металлы платиновой группы: обзор, список, свойства и применение
Металлы платиновой группы – это шесть благородных драгоценных химических элементов, которые расположены рядом в периодической таблице. Все они являются переходными металлами 8–10 групп 5–6 периода.
Металлы платиновой группы: список
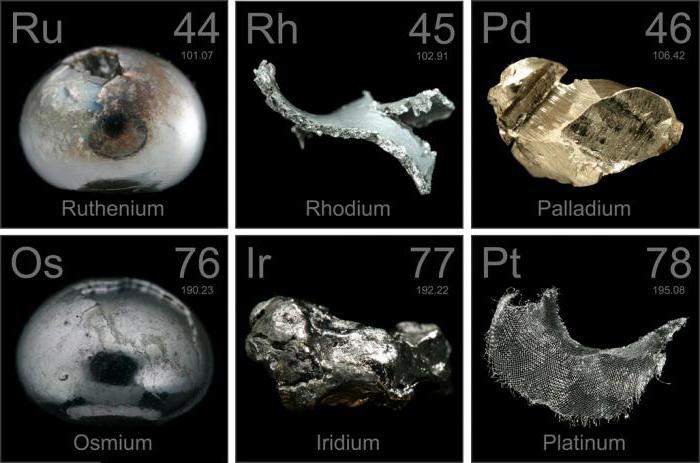
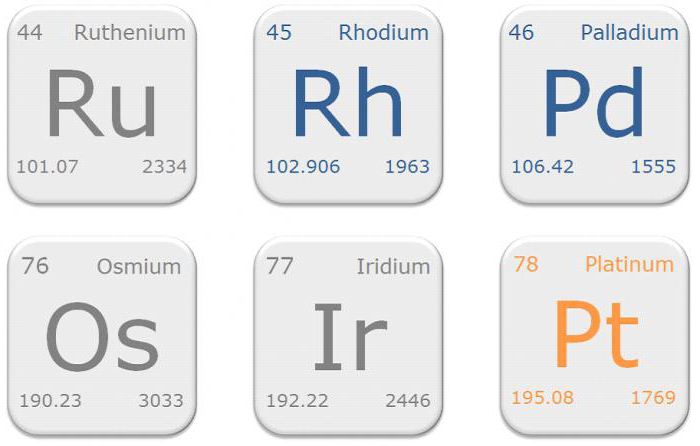
Группа состоит из следующих шести химических элементов, расположенных в порядке возрастания атомного веса:
- Ru – рутений.
- Rh – родий.
- Pd – палладий.
- Os – осмий.
- Ir – иридий.
- Pt – платина.
Металлы платиновой группы обладают серебристо-белым оттенком, за исключением осмия, цвет которого голубовато-белый. Их химическое поведение парадоксально в том, что они обладают высокой устойчивостью к воздействию большинства реагентов, но используются в качестве катализаторов, легко ускоряющих или контролирующих скорость окисления, восстановления и реакций гидрирования.
Рутений и осмий кристаллизуются в гексагональную плотноупакованную систему, а другие обладают гранецентрированной кубической структурой. Это выражается в большей твердости рутения и осмия.
История открытия
Хотя платиносодержащие золотые артефакты датированы 700 г. до н. э., присутствие этого металла является, скорее, случайностью, чем закономерностью. Иезуиты в XVI веке упоминали серые плотные камешки, связанные с аллювиальными месторождениями золота. Эти камешки нельзя было расплавить, но они образовывали сплав с золотом, при этом слитки становились ломкими, и их уже было невозможно очистить. Камешки стали называть platina del Pinto – гранулы серебристого материала из реки Пинто, впадающей реку Сан-Хуан в Колумбии.
Ковкая платина, которую можно получить только после полной очистки металла, была выделена французским физиком Шабано в 1789 году. Из нее был сделан кубок, преподнесенный папе Пию VI. Об открытии палладия в 1802 году сообщил английский химик Уильям Волластон, который назвал хим. элемент группы платиновых металлов в честь астероида. Волластон впоследствии заявлял об обнаружении еще одного вещества, присутствующего в платиновой руде. Его он назвал родием из-за розового цвета солей металла. Открытия иридия (по имени богини радуги Ириды из-за пестрой окраски его солей) и осмия (от греческого слова «запах» из-за хлорного запаха его летучего окисла) были сделаны английским химиком Смитсоном Теннантом в 1803 году. Французские ученые Ипполит-Виктор Колле-Дескоти, Антуан-Франсуа Фуркруа, и Николя-Луи Воклен выделили два металла одновременно. Рутений, последний изолированный и идентифицированный элемент, получил свое название по латинскому наименованию России от русского химика Карла Карловича Клауса в 1844 году.
В отличие от таких легко выделяемых в относительно чистом состоянии путем простого огневого рафинирования веществ, как золото, серебро, металлы платиновой группы требуют сложной водно-химической обработки. Эти методы не были доступны до конца 19 века, поэтому выявление и изоляция платиновой группы отстала от серебра и золота на тысячи лет. Кроме того, высокая температура плавления этих металлов ограничивала их применение, пока исследователи в Британии, Франции, Германии и России не разработали методы преобразования платины в форму, пригодную для обработки. Как драгоценные металлы платиновой группы начали использоваться в ювелирных изделиях с 1900 года. Хотя такое применение остается актуальным и сегодня, промышленное намного его превзошло. Палладий стал очень востребованным материалом для контактов в телефонных реле и других системах проводной коммуникации, обеспечивая длительный срок службы и высокую надежность, а платина, из-за своей устойчивости к искровой эрозии, во время Второй мировой войны стала применяться в свечах зажигания боевых самолетов.
После войны расширение методов молекулярной конверсии при переработке нефти создало огромный спрос на каталитические свойства, которыми обладают металлы платиновой группы. К 1970-м годам потребление выросло еще больше, когда стандарты автомобильных выбросов в США и других странах привело к использованию данных химических элементов в каталитической конверсии выхлопных газов.
За исключением малых россыпных месторождений платины, палладия и осмистого иридия (сплава иридия и осмия), практически нет руды, в которой бы основным компонентом был химический элемент – металл платиновой группы. Минералы, как правило, содержатся в сульфидных рудах, в частности в пентландите (Ni, Fe)9S8. Наиболее распространены лаурит RuS2, ирарсит, (Ir,Ru,Rh,Pt)AsS, осмиридиум (Ir,Os), куперит, (PtS) и браггит (Pt,Pd)S.
Крупнейшее в мире месторождение металлов платиновой группы – Бушвельдский комплекс в ЮАР. Большие запасы сырья сосредоточены в месторождениях Садбери в Канаде и Норильско-Талнахском в Сибири. В США наибольшие залежи минералов платиновой группы расположены в Стилуотере, Монтана, но здесь они значительно меньше, чем в ЮАР и России. Крупнейшими в мире производителями платины являются Южная Африка, Россия, Зимбабве и Канада.

Добыча и обогащение
Основные южноафриканские и канадские месторождения эксплуатируются шахтным способом. Практически все металлы платиновой группы извлекаются из медных или никелевых сульфидных минералов с помощью флотационной сепарации. Плавка концентрата производит смесь, которая вымывается из меди и сульфидов никеля в автоклаве. Твердый остаток выщелачивания содержит от 15 до 20% металлов платиновой группы.
Иногда до флотации используется гравитационное разделение. В результате получается концентрат, содержащий до 50% платиновых металлов, что избавляет от необходимости выплавки.
Механические свойства
Металлы платиновой группы значительно отличаются механическими свойствами. Платина и палладий довольно мягкие и очень ковкие. С этими металлами и их сплавами можно работать как в горячем, так и в холодном состоянии. Родий сначала обрабатывают горячим, а позже его можно обрабатывать холодным с довольно частым отжигом. Иридий и рутений должны быть нагреты, холодной обработке они не поддаются.
Осмий – самый твердый из группы и имеет наиболее высокую температуру плавления, но его склонность к окислению накладывает свои ограничения. Иридий наиболее коррозионностойкий из платиновых металлов, а родий ценится за сохранение своих свойств при высоких температурах.

Структурные применения
Поскольку дочиста отожженная платина очень мягкая, она восприимчива к царапинам и порче. Для увеличения твердости ее сплавляют со множеством других элементов. Платиновые драгоценности очень популярны в Японии, где ее называется «хаккин» и «белое золото». Сплавы для ювелирных изделий содержат 90% Pt и 10% Pd, который легко обрабатывать и паять. Добавление рутения повышает твердость сплава, сохраняя стойкость к окислению. Сплавы платины, палладия и меди используются в кованых изделиях, так как они тверже платино-палладиевых и менее затратны.
Тигли, используемые для производства монокристаллов в полупроводниковой промышленности, требуют коррозионной устойчивости и стабильности при высоких температурах. Для этого применения лучше всего подходят платина, платина-родий и иридий. Платинородиевые сплавы используются в производстве термопар, которые предназначены для измерения повышенных температур до 1800 °C. Палладий применяют как в чистом, так и в смешанном виде в электрических устройствах (50% потребления), в стоматологических сплавах (30%). Родий, рутений и осмий редко используются в чистом виде – они служат легирующей добавкой для других металлов платиновой группы.

Катализаторы
Около 42% всей платины, произведенной на Западе, используется в качестве катализатора. Из них 90% применяется в автомобильных выхлопных системах, где тугоплавкие гранулы или сотовые конструкции с платиновым покрытием (а также палладиевым и родиевым) содействуют преобразованию несгоревших углеводородов, окиси углерода и окислов азота в воду, углекислый газ и азот.
Сплав платины и 10% родия в виде раскаленной докрасна металлической сетки служит катализатором в реакции между аммиаком и воздухом для получения окислов азота и азотной кислоты. При подаче вместе со смесью аммиака метана можно получить синильную кислоту. При переработке нефти платина на поверхности гранул оксида алюминия в реакторе является катализатором преобразования длинноцепочечных молекул нефти в разветвленные изопарафины, которые желательны в смеси высокооктановых бензинов.

Гальваника
Все металлы платиновой группы можно наносить гальванически. Из-за твердости и блеска получаемого покрытия наиболее часто применяется родий. Хотя его стоимость выше, чем платины, меньшая плотность позволяет использовать меньшую массу материала при сопоставимой толщине.
Палладий – металл платиновой группы, который проще всего использовать для нанесения покрытий. Благодаря этому прочность материала значительно повышается. Рутений нашел применение в инструментах, предназначенных для обработки трением при низком давлении.
Химические соединения
Органические комплексы металлов платиновой группы, такие как комплексы алкилплатины, используются в качестве катализаторов в процессе полимеризации олефинов, производстве полипропилена и полиэтилена, а также при окислении этилена в ацетальдегид.
Соли платины находят все более широкое применение в химиотерапии рака. Например, они входят в состав таких лекарств, как "Карбоплатин" и "Цисплатин". Покрытые оксидом рутения электроды используются в производстве хлора и хлората натрия. Сульфат и фосфат родия применяются в родиевых гальванических ваннах.
Полный список металлов, известных науке
Посмотрите вокруг на секунду. Сколько металлических вещей вы можете увидеть? Обычно, когда мы думаем о металлах, мы вспоминаем о веществах, которые являются блестящими и прочными. Однако они также находятся в нашей пище и в наших телах. Давайте познакомимся с полным списком металлов, известных науке, узнаем их основные свойства и выясним, почему они такие особенные.

Элементы, легко теряющие электроны, которые являются блестящими (отражающими), податливыми (могут быть отлиты в другие формы) и считаются хорошими проводниками тепла и электричества, называют металлами. Они имеют решающее значение для нашего образа жизни, так как не только являются частью структур и технологий, но и важны для производства почти всех предметов. Металл есть даже в человеческом теле. Взглянув на этикетку состава мультивитаминов, вы увидите десятки перечисленных соединений.
Возможно, вы не знали, что такие элементы, как натрий, кальций, магний и цинк, необходимы для жизни, и, если они отсутствуют в наших телах, наше здоровье может быть в серьезной опасности. Например, кальций необходим для здоровых костей, магний - для метаболизма. Цинк усиливает функцию иммунной системы, а железо помогает клеткам крови переносить кислород по всему телу. Однако металлы в наших телах отличаются от металла в ложке или стальном мосте тем, что они потеряли электроны. Они называются катионами.
Металлы также обладают антибиотическими свойствами, поэтому перила и ручки в общественных местах часто изготавливаются из этих элементов. Известно, что многие инструменты делаются из серебра для предотвращения размножения бактерий. Искусственные суставы изготавливаются из титановых сплавов, которые одновременно предотвращают заражение и делают реципиентов сильнее.
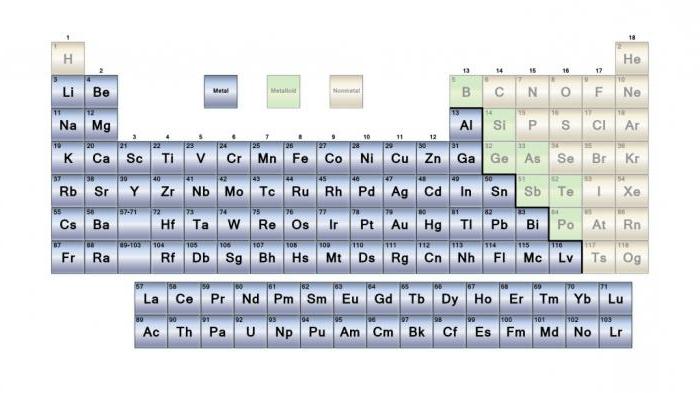
Металлы в периодической таблице
Все элементы в периодической системе Дмитрия Менделеева делятся на две большие группы: металлы и неметаллы. Первая является самой многочисленной. Большинство элементов - металлы (синий). Неметаллы в таблице изображены на желтом фоне. Есть также группа элементов, которые относят к металлоидам (красный). Все металлы сгруппированы в левой части таблицы. Обратите внимание, что водород сгруппирован с металлами в верхнем левом углу. Несмотря на это, он считается неметаллическим. Однако некоторые ученые теоретизируют, что в ядре планеты Юпитер может быть металлический водород.

Металлическое связывание
Многие из замечательных и полезных качеств элемента связаны с тем, как его атомы соединяются друг с другом. При этом возникают определенные связи. Металлическое взаимодействие атомов приводит к созданию металлических структур. Любой образец этого элемента в повседневной жизни, от автомобиля до монет в кармане, включает в себя металлическое соединение.

Во время этого процесса атомы металла разделяют свои внешние электроны равномерно друг с другом. Электроны, протекающие между положительно заряженными ионами, легко передают тепло и электроэнергию, делая эти элементы такими хорошими проводниками тепла и электричества. Медные провода используются для электроснабжения.

Реакции металлов
Реакционная способность относится к тенденции элемента реагировать с химическими веществами в его окружении. Она бывает разная. Некоторые металлы, например, калий и натрий (в колонках 1 и 2 в периодической таблице), легко реагируют со многими различными химическими веществами и редко встречаются в своей чистой, элементарной форме. Оба обычно существуют только в соединениях (связанных с одним или несколькими другими элементами) или как ионы (заряженная версия их элементарной формы).

С другой стороны, существуют и другие металлы, их еще называют ювелирными. Золото, серебро и платина являются не очень реактивными и обычно встречаются в чистом виде. Эти металлы легче теряют электроны, чем неметаллы, но не так легко, как реактивные металлы, например, натрий. Платина относительно нереакционноспособна и очень устойчива к реакциям с кислородом.
Свойства элементов
Когда вы изучали алфавит в начальной школе, вы обнаружили, что все буквы имеют свой собственный уникальный набор свойств. Например, у некоторых были прямые линии, у некоторых - кривые, а у других были линии обоих типов. То же самое можно сказать и об элементах. Каждый из них имеет уникальный набор физических и химических свойств. Физические свойства - это качества, присущие определенным веществам. Блестящий или нет, насколько он хорошо проводит тепло и электричество, при какой температуре тает, насколько большую имеет плотность.

Химические свойства включают те качества, которые наблюдаются при реагировании на воздействие кислородом, если они будут гореть (то, насколько сложно им будет удерживать их электроны во время химической реакции). Различные элементы могут иметь общие свойства. Например, железо и медь являются одновременно элементами, которые проводят электричество. Однако они не имеют одинаковых свойств. Например, когда железо подвергается воздействию влажного воздуха, оно покрывается ржавчиной, но когда медь оказывается под действием тех же условий, она приобретает специфический зеленый налет. Вот почему статуя Свободы зеленая, а не ржавая. Она сделана из меди, а не железа).

Организация элементов: металлы и неметаллы
Тот факт, что элементы имеют некоторые общие и уникальные свойства, позволяет сортировать их в красивую, аккуратную диаграмму, которая называется периодической таблицей. Она организует элементы на основе их атомного числа и свойств. Итак, в периодической таблице мы находим элементы, сгруппированные вместе, которые имеют общие свойства. Железо и медь находятся близко друг к другу, оба являются металлами. Железо обозначено символом «Fe», а медь обозначается символом «Cu».

Большинство элементов периодической таблицы - это металлы, и они, как правило, находятся в левой части таблицы. Они группируются вместе, потому что обладают определенными физическими и химическими свойствами. Например, металлы плотные, блестящие, они хорошие проводники тепла и электричества, и они легко теряют электроны в химических реакциях. Напротив, неметаллы имеют противоположные свойства. Они не плотные, не проводят тепло и электричество, и стремятся получить электроны, а не отдать их. Когда мы смотрим в периодическую таблицу, мы видим, что большинство неметаллов сгруппированы справа. Это такие элементы, как гелий, углерод, азот и кислород.

Что такое тяжелые металлы?
Список металлов достаточно многочисленный. Некоторые из них могут накапливаться в организме и не наносить ему при этом вреда, как например, природный стронций (формула Sr), который является аналогом кальция, так как продуктивно откладывается в костной ткани. Какие из них называются тяжелыми и почему? Рассмотрим четыре примера: свинец, медь, ртуть и мышьяк.
Где находятся эти элементы и как они влияют на окружающую среду и здоровье человека? Тяжелые металлы представляют собой металлические, встречающиеся в природе соединения, которые имеют очень высокую плотность по сравнению с другими металлами - по меньшей мере, они в пять раз больше плотности воды. Они токсичны для людей. Даже небольшие дозы могут привести к серьезным последствиям.

- Свинец. Это тяжелый металл, являющийся токсичным для людей, особенно для детей. Отравление этим веществом может привести к проблемам неврологического характера. Несмотря на то что когда-то он был весьма привлекательным из-за его гибкости, высокой плотности и способности поглощать вредное излучение, свинец был выведен из употребления по многим направлениям. Этот мягкий серебристый металл, который встречается на Земле, является опасным для людей и накапливается в организме в течение долгого времени. Самое страшное, что от него нельзя избавиться. Он сидит там, накапливается и постепенно отравляет тело. Свинец токсичен для нервной системы и может вызвать серьезное повреждение головного мозга у детей. Он широко использовался в 1800-х годах для создания макияжа и вплоть до 1978 года использовался в качестве одного из ингридиентов в краске для волос. Сегодня свинец используется в основном в больших батареях, в качестве экранов для рентгеновских лучей или изоляции для радиоактивного материала.
- Медь. Это красновато-коричневый тяжелый металл, у которого есть множество применений. Медь по-прежнему является одним из лучших проводников электричества и тепла, и многие электрические провода сделаны из этого металла и покрыты пластиком. Монеты, в основном мелочь, также делают из этого элемента периодической системы. Острые отравления медью встречаются редко, но, как и свинец, она может накапливаться в тканях, что в конечном итоге приводит к токсичности. Люди, которые подвергаются воздействию большим количеством меди или медной пыли, также находятся в зоне риска.
- Ртуть. Этот металл токсичен в любой форме и может даже поглощаться кожей. Его уникальность состоит в том, что он является жидким при комнатной температуре, его иногда называют «быстрым серебром». Его можно увидеть в термометре, потому что в качестве жидкости он поглощает тепло, изменяя объем даже с малейшей разницей в температуре. Это позволяет ртути подниматься или падать в стеклянной трубке. Поскольку это вещество является мощным нейротоксином, многие компании переходят на спиртовые термометры, окрашенные в красный цвет.
- Мышьяк. Со времен Римской империи вплоть до викторианской эпохи мышьяк считался «королем ядов», а также «ядом царей». История пронизана бесчисленными примерами как королевских лиц, так и простых людей, совершающих убийства для личной выгоды, используя соединения мышьяка, у которых не было ни запаха, ни цвета, ни вкуса. Несмотря на все отрицательные влияния, этот металлоид также имеет свои области применения, даже в медицине. Например, триоксид мышьяка является очень эффективным препаратом, используемым для лечения людей с острым промиелоцитарным лейкозом.

Что такое драгоценный металл?
Драгоценный металл представляет собой металл, который может быть редким или трудно добываемым, а также экономически очень ценным. Каков список металлов, являющихся драгоценными? Всего их три:
- Платина. Несмотря на свою тугоплавкость, она используется в ювелирных изделиях, электронике, автомобилях, в химических процессах и даже в медицине.
- Золото. Этот драгоценный металл используется для изготовления ювелирных изделий и золотых монет. Однако он имеет много других применений. Он используется в медицине, производстве и лабораторном оборудовании.
- Серебро. Этот благородный металл серебристо-белого цвета является очень ковким. в чистом виде является достаточно тяжелым, оно легче свинца, но тяжелее меди.

Металлы: виды и свойства
Большинство элементов можно рассматривать как металлы. Они сгруппированы в середине в левой стороне таблицы. Металлы бывают щелочные, щелочноземельные, переходные, лантаноиды и актиниды.

- твердое вещество при комнатной температуре (за исключением ртути);
- обычно блестящее;
- с высокой температурой плавления;
- хороший проводник тепла и электричества;
- с низкой способностью к ионизации;
- с низкой электроотрицательностью;
- податливый (способный принимать заданную форму);
- пластичный (можно вытянуть в проволоку);
- с высокой плотностью;
- вещество, которое теряет электроны в реакциях.

Список металлов, известных науке
- литий;
- бериллий;
- натрий;
- магний;
- алюминий;
- калий;
- кальций;
- скандий;
- титан;
- ванадий;
- хром;
- марганец;
- железо;
- кобальт;
- никель;
- медь;
- цинк;
- галлий;
- рубидий;
- стронций;
- иттрий;
- цирконий;
- ниобий;
- молибден;
- технеций;
- рутений;
- родий;
- палладий;
- серебро;
- кадмий;
- индий;
- коперниций;
- цезий;
- барий;
- олово;
- железо;
- висмут;
- свинец;
- ртуть;
- вольфрам;
- золото;
- платина;
- осмий;
- гафний;
- германий;
- иридий;
- ниобий;
- рений;
- сурьма;
- таллий;
- тантал;
- франций;
- ливерморий.

Всего известно около 105 химических элементов, большая часть из которых - металлы. Последние являются очень распространенным элементом в природе, который встречается как в чистом виде, так и в составе всевозможных соединений.

Металлы залегают в недрах земли, их можно найти в различных водоемах, в составе тел животных и человека, в растениях и даже в атмосфере. В периодической системе они располагаются начиная с лития (металл с формулой Li) и заканчивая ливерморием (Lv). Таблица она продолжает пополняться новыми элементами, и в основном это металлы.
Все о платиновых металлах

Практически каждый человек знает о существовании драгоценных металлов. К их числу относят серебро, золото и платину. При этом далеко не каждому известно о существовании платиновой группы. Ее представителей также относят к числу благородных.


Особенности
Платиновые металлы – это группа из 6 элементов, которые расположены рядом друг с другом в периодической химической таблице. Каждый их элементов группы по праву считается благородным. Это связано со следующими химическими и физическими свойствами.
- Специалисты отмечают низкую концентрацию платиновых металлов. Количество месторождений невелико. Данная характеристика также относится к химическим элементам, которые традиционно считаются редкими и дорогостоящими.
- Представители вышеуказанной группы обладают свойствами следующих металлов: родий, осмий, палладий, рутений.
- В процессе изучения платиноидов было отменно сходство в атомном строении с элементами, указными выше.


Ученые, работающие в области химии, поделили все платиновые металлы на две группы, называемые триадами.
Разделение производится по весу.
- Группа №1. Это самые легкие представители. К ним относится палладий, рутений и родий.
- Группа №2. Оставшиеся 6 металлов – иридий, осмий и сама платина. Это уже тяжелые металлы.


Металлы и их свойства
У металлов вышеуказанной группы имеются свои обозначения. Список такой.
- Рутений – Ru.
- Родий – Rh.
- Палладий – Pd.
- Осмий – Os.
- Иридий – Ir.
- Платина – Pt.


Заметка: все обозначения расположены в определенном порядке, согласно атомному весу.
От наименьшего значения к большему. Все платиновые металлы обладают схожими характеристиками.
- Первое сходство заключается во внешнем виде. Практически все элементы, кроме осмия, имеют светлый оттенок (сочетание белого и серебристого цветов). Осмий отличается легким голубоватым тоном.
- Металлы имеют высокую устойчивость по отношению к множеству реагентов. При этом платиноиды являются эффективными катализаторами.
- С их помощью контролируют различные химические процессы, управляют скоростью окисления, а также следят за другими реакциями. Такое поведение металлов считается удивительным и парадоксальным.

Свойства
На поверхности не образуется окисление. Таким образом, наглядно демонстрируется инертность. По мнению специалистов, она особенно заметна у платины. При изучении представителей платиновой группы нельзя было обойти стороной температуру плавления. Самое низкое значение у палладия и составляет 1554 градуса. Самое высокое значение у осмия. Его температура насчитывает 3 тысячи 27 градусов по Цельсию.
Следующее одинаковое свойства – тугоплавкость. Данная характеристика говорит о замечательной износостойкости. Несмотря на внешнее сходство, физические качества отличаются. В зависимости от этих показателей, при обработке используются специальные методики. Рутений и осмий – очень хрупкие металлы и требуют особо бережного отношения.
Высокая пластичность – показатель палладия и платины.


Где добываются?
Месторождения платиновых металлов обычно рассеяны на территории Канады и Южной Африки. В этих регионах получение полезного ископаемого происходит стандартным шахтным способом. Как показывает практика, большинство платиноидов добывается путем извлечения элементов из никелевых сульфидных минералов или же медных руд. В работе используют флотационную сепарацию. В процессе обработки металла выполняется плавка полученного концентрата, в результате этого получается специальная смесь. Объем платиновых металлов – от 15 до 20% от сухого остатка.
В некоторых случаях процесс добычи и обработки может отличаться. Иногда на заводах используется гравитационное разделение. В этом случае количество необходимых химических элементов возрастает до 50%. Такой вариант обработки исключает выплавку. Несмотря на то что богатые залежи МПГ встречаются редко, некоторые месторождения также находятся на территории Канады, Китая, Австралии и Финляндии.
Существуют и другие источники, однако, доля их добычи насчитывает всего 0,3% от общей массы, добываемой на планете.

Где используются?
Платиноиды нашли свое применение в различных сферах. Универсальные свойства металлов данной группы активно используются на сегодняшний день. Чистая платина само по себе очень мягкая и податливая. В таком состоянии она очень восприимчива и различным повреждениям и дефектам. Чтобы повысить твердость и износостойкость драгоценного металла, используются различные элементы. Платину сплавляют с другими химическими элементами.
Ювелирные украшения из платины высоко ценятся и стоят дороже золота. Особую популярность они обрели в Японии. Жители Страны восходящего солнца называют такие изделия «хаккин». Основной ювелирного сплава является платина и составляет 90% от общей массы. Оставшиеся 10% – это палладий. С ним легко работать, включая пайку и другую обработку.


Также для увеличения твердости, драгоценный белый металл соединяют с рутением. Добавление этого элемента увеличивает стойкость к процессу окисления. МПГ нашли свое применение в изготовлении кованых изделий. В этом случае используется сплав, состоящий из меди, платины и палладия. Такой вариант более доступный по цене, по сравнению с составом из двух элементов: платины и палладия.
Специальные сплавы, которые делаются с использованием платиноидов, широко используются при изготовлении термопар. Это специальное устройство с широким спектром применения. Его основное предназначение заключается в изменении высоких температур (максимальное значение – до 1800 градусов по Цельсию выше нуля). Некоторые представители применяются в чистом виде. Как правило, они выступают в качестве добавок к остальным металлам из платиновой группы. Палладий нашел свое применение в сфере производства электрического оборудования, а также в современных стоматологических сплавах.

Катализаторы
Более 40% всей полученной платины, которая изготавливается за границей, используется как катализатор. Это удивительное и полезное свойство было обозначено еще в первой части статьи. Практически весь металл (примерно 90%) нашел свое применение в сфере производства выхлопных систем для автомобилей. Драгоценный материал, а также родий и палладий, выступает в качестве защитного покрытия для сотовых конструкций и других элементов. Слой металла защищает от процессов окисления, сохраняя оборудование целым и невредимым. Вступая в химическую реакцию, агрессивные компоненты преобразовываются в безопасные соединения и вещества.
Химические элементы могут выполнять задачу эффективного катализатора не только в качестве покрытия, но и в виде раскаленной сетки из металла. В этом случае происходит реакция между воздухом и ядовитым веществом – аммиаком. В результате получается азотная кислота и оксид азота. Для получения других веществ добавляют различные компоненты.
Еще одна сфера, которая не обходится без использования МПГ – добыча нефти. Это глобальная отрасль, которая указывает на ценность платиноидов и их важность в промышленности.


Другие варианты использования металлов такие.
- На территории России из палладия изготавливаются инвестиционные монеты. Делать это начали после того, как во времена СССР была выпущена монета из чистого палладия. Номинал – 25 рублей.
- Высоковольтное оборудование также не обходится без использования МПГ. При изготовлении электроники данного типа нужны износостойкие и надежные контакты, которые будут устойчивы к негативному воздействию со стороны. Несмотря на развитие новых технологий, в настоящее время нет действующей альтернативы платиноидам.
- В процессе изготовления инструментов и устройств для работы в сложных условиях также активно используются такие металлы. Чтобы трудиться в агрессивной среде, оборудование должно быть прочным, износостойким и долговечным. Именно эти характеристики оно получает от платиновых металлов.
- Чтобы значительно повысить стойкость титана к коррозии, к нему добавляют немного палладия. Также данный элемент платиновой группы часто подмешивают к стали.
- В области медицины активные соединения также активно используются. Данная практика применялась ранее и сохраняет актуальность на сегодняшний день.
- Не стоит забывать о платиновой фольге. Этот материал используется, чтобы защищать устройство химических реакторов.
- Сплав из серебра и палладия активно применяется в слаботочной электронике.


О том, как ещё используется этот драгоценный металл, смотрите в следующем видео.
Читайте также:
