Химические соединения в металлических сплавах
Рассмотрим ряд основополагающих определений и понятий.
Сплав – вещество, полученное сплавлением двух и более элементов (компонентов). Сплав, приготовленный преимущественно из металлических элементов и обладающий металлическими свойствами, называются металлическим сплавом.
По количеству компонентов сплавы соответственно называются двойными, тройными и многокомпонентными.
Структурные составляющие – обособленные части сплава, имеющие одинаковое строение с присущими им характерными особенностями.
Система – совокупность тел (твердых, жидких) в определенном объеме при определенных внешних условиях, взятых для исследования.
Компонент – простейшая часть (вещество) из образующих систему. В металлических сплавах компонентами являются элементы (металлы и неметаллы) и химические соединения (не диссоциирующие при нагревании)
Фаза – однородная часть системы, имеющая физическую границу раздела (поверхность), при переходе через которую химические состав или структура изменяются скачком.
2.1. Строение сплавов
Чистые металлы находят довольно ограниченное применение. Основными конструкционными материалами являются металлические сплавы. В основном сплавы получают путём кристаллизации жидкого расплава нескольких металлов, но могут быть и другие пути – спеканием, диффузией, осаждением и другие.
Почти все металлы в жидком состоянии растворяются друг в друге в любых соотношениях и образуют однородный жидкий раствор с равномерным распределением атомов одного металла среди атомов другого металла.
При образовании сплавов в процессе их затвердевания возможно различное взаимодействие компонентов. По характеру взаимодействия компонентов все сплавы подразделяются на три основных типа: механические смеси, твердые растворы и химические соединения.
Механическая смесь двух компонентов образуется, если они не способны к взаимодействию или взаимному растворению.
Каждый компонент при этом кристаллизуется в свою кристаллическую решетку. Структура механических смесей неоднородная, состоящая из отдельных зерен компонента А и компонента В. Свойства механических смесей зависят от количественного соотношения компонентов.
Если механическая смесь образуется при первичной кристаллизации, она называется эвтектической, если в результате вторичной – эвтектоидной.
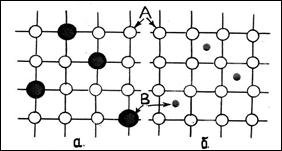
Твердые растворы образуются, когда один компонент растворяется в другом. Тогда в твердом состоянии атомы одного компонента входят в кристаллическую решетку другого. Если атомы кристаллической решетки одного компонента А частичного замещаются атомами другого В, образуются твердые растворы замещения, рис. 2.1а. Твердые растворы замещения образуются элементами, атомные радиусы которых отличаются не более чем на 8 – 15%, но и в этом случае кристаллическая решетка растворителя искажается, не утрачивая своего строения.
Если атомы растворимого компонента В внедряются в пустоты решетки растворителя А, то образуются твердые растворы внедрения (рис. 2.1б). Следовательно, атомы растворимого элемента должны быть соизмеримы с пустотами кристаллической решетки растворителя. Концентрация твердых растворов внедрения не может быть высокой – не более 1…2%.

Рис. 2.1. Схемы твердых растворов замещения (а) внедрения (б)
Твердый раствор имеет однородную структуру и одну кристаллическую решетку. Обозначают твердые растворы буквами греческого алфавита α, β, γ, δ и т.д.
Химическое соединение образуется, если компоненты сплава А и В вступают в химическое взаимодействие. Химическое соединение имеет свою кристаллическую решетку, которая отличается от кристаллических решеток компонентов. При этом сохраняется кратное соотношение компонентов, что позволяет выразить состав химического соединения формулой А n В m .
Свойства химического соединения резко отличаются от свойств образующих его компонентов при этом они, как правило, обладают большой твердостью и хрупкостью (карбиды, нитриды и др.). Химическое соединение имеет однородную структуру, состоящую из одинаковых по составу и свойствам зерен, и может играть роль компонента в сплавах.
2.2. Диаграммы состояния двойных сплавов
Диаграмма состояния – графическое изображение состояния сплава изучаемой системы в зависимости от концентрации в нем компонентов и температуры. Диаграмма состояния показывает равновесные, устойчивые состояния сплава, т.е. такие, которые при данных условиях обладают минимальной свободной энергией.
Построение диаграмм состояния осуществляют различными экспериментальными методами. Наиболее часто используется метод термического анализа. Он заключается в том, что составляют несколько сплавов с различной концентрацией компонентов, расплавляют их и медленно охлаждают, фиксируя время охлаждения и температуру.
По полученным данным строят серию кривых охлаждения в координатах: время (τ, сек) – температура (t,°С), на которых наблюдают точки перегибов и температурные остановки – критические точки фазовых переходов (рис. 2.2).
Рис. 2.2. Кривая охлаждения сплава
В отличие от чистых металлов сплавы кристаллизуются не при постоянной температуре, а в интервале температур, поэтому на кривых охлаждения сплавов есть две критические точки. В верхней критической точке, называемой точкой ликвидус (tл), начинается кристаллизация. В нижней критической точке - солидус (tс) кристаллизация завершается.
Диаграмму строят в координатах температура – концентрация. Линии диаграммы разграничивают области одинаковых фазовых состояний. Для построения диаграммы состояния используют большое количество кривых охлаждения для сплавов различных концентраций. При построении диаграммы критические точки переносятся с кривых охлаждения на диаграмму (оси температура – концентрация) и соединяются линией. В получившихся на диаграмме областях записывают фазы или структурные составляющие. Линия начала кристаллизации сплавов на диаграмме называется линией ликвидус, а линия окончания кристаллизации – солидус.
Вид диаграммы зависит от того, как взаимодействуют между собой компоненты.
Диаграмма состояния сплавов,
образующих механические смеси чистых компонентов (1 тип)
Рассмотрим кривые охлаждения нескольких сплавов системы А – В, имеющих различный состав (рис. 2.3). Кристаллизация чистого компонента А (100%) начинается в т.1 и заканчивается в т.1*, протекая при постоянной температуре. Выше этой температуры компонент А находится в жидком состоянии, ниже – в твердом. Аналогично происходит кристаллизация чистого компонента В.
Кривая охлаждения сплава (60% А + 40%В) аналогична кривым охлаждения чистых компонентов. На ней имеется также только одна температурная остановка 2-2*, т.е. кристаллизация происходит при постоянной температуре. Особенность кристаллизации этого сплава заключается в том, что происходит одновременная кристаллизация обоих компонентов – появляются и растут кристаллы, образуя мелкокристаллическую механическую смесь обоих компонентов (А+В).
Механическая смесь двух или более разнородных кристаллов, одновременно кристаллизующихся из жидкости, называется эвтектикой (от эвтэо (греч.) – легкоплавкий). Сплав, отвечающий составу эвтектики, называют эвтектическим сплавом. Он имеет постоянную и минимальную температуру плавления (кристаллизации) для сплавов данной системы и постоянный химический состав.

Рис. 2.3. Диаграмма состояния сплавов, образующих механические смеси
чистых компонентов, состав сплавов: 1 – 100%А, 2 – 80%А+20%В,
3 – 60%А+40%В, 4 – 20%А+80%В, 5 – 100%В
Кристаллизация сплава (80%А + 20%В) происходит иначе. На кривой имеются две кристаллические точки: точка перегиба 1 и температурная остановка 2-2*. Выше т.1 сплав находится в жидком состоянии, в т.1 появляются первые зародыши кристаллов компонента А – начало кристаллизации. Выделение и рост зерен А продолжается до т.2. При этой температуре жидкий сплав, вследствие удаления из расплава компонента А в виде твердых кристаллов, приобретет эвтектический состав (60%А + 40%В) и при постоянной температуре, равной эвтектической, произойдет одновременная кристаллизация обоих компонентов (А+В), т.е. произойдет эвтектическое превращение.
Сказанное в равной степени относится и к сплаву (20%А + 80%В), отличие состоит лишь в том, что на участке 1–2 происходит образование и рост зерен компонента В. Для этих сплавов характерной особенностью является то, что кристаллизация на участке 1–2 происходит в интервале температур.
Полученные критические точки перенесем на диаграмму, где координатами будут концентрация и температура. Если затем соединить линией все точки начала кристаллизации (линия АСВ) и точки окончания кристаллизации линия (ДСF), то получим диаграмму состояния системы А – В. Линия АСВ – геометрическое место точек ликвидус, называется линией ликвидус. Линия ДСF – линией солидус. Выше линии ликвидус находится жидкость (расплав), ниже линии солидус – сплавы находятся в твердом состоянии. Сплав, отвечающий составу эвтектики (точка С), как уже указывалось, называется эвтектическим. Сплавы, находящиеся левее точки С, называют доэвтектическими. Их структура – избыточные кристаллы А и эвтектика (А+В). Сплавы, расположенные правее точки С, – заэвтектические, их структура кристаллы – В и эвтектика (А+В). Из этого следует что А, В и эвтектика (А+В) являются структурными составляющими сплавов.
Диаграмма состояния сплавов с неограниченной растворимостью
компонентов в твердом состоянии (2 тип)
Для таких сплавов возможно образование двух фаз: жидкого сплава Ж и твердого раствора α. На диаграмме две линии, верхняя – ликвидус и нижняя – солидус (рис. 2.4).

Рис. 2.4. Диаграмма состояния сплавов с неограниченной растворимостью
Диаграмма состояния сплавов с ограниченной растворимостью
в твердом состоянии (3 тип)
В таких сплавах могут существовать три фазы: жидкий раствор (Ж), твердый раствор компонента В в компоненте А – (α) и твердый раствор компонента А в компоненте В – (β). Эта диаграмма содержит в себе элементы двух предыдущих (рис. 2.5).

Рис. 2.5. Диаграмма состояния сплавов с ограниченной растворимостью
компонентов в твердом состоянии
Линия АСВ – линия ликвидус, линия АЕСFВ – линия солидус. Линия ЕСF – линия эвтектики. Таким образом, здесь также образуется эвтектика, доэвтектические и заэвтектические сплавы. Линия РЕ – линия ограниченной растворимости компонента В в компоненте А, по этой линии происходит выделение вторичных кристаллов β II (вследствие уменьшения растворимости компонента В в компоненте А с понижением температуры). Процесс выделения вторичных кристаллов называется вторичной кристаллизацией.
Диаграмма состояния сплавов, образующих устойчивые химические соединения (4 тип)

Рис. 2.6. Диаграмма 4 типа
Такая диаграмма характеризуется наличием вертикальной линии, соответствующей соотношению компонентов в химическом соединении АnВ m (рис. 2.6). Эта линия делит диаграмму на две части, которые можно рассматривать как самостоятельные диаграммы сплавов, образуемых устойчивым химическим соединением и одним из компонентов. На рисунке представлена диаграмма для случая, когда каждый из компонентов образует с химическим соединением механическую смесь.
2.3. Пластическая деформация, наклеп и рекристаллизация
Пластическая деформация – это необратимая деформация, т.е. ее влияние на форму, структуру и свойства тела сохраняются после снятия нагрузки. При пластической деформации зерна деформируются, вытягиваются в направлении деформации, образуется волокнистая структура, увеличивается число дислокаций. При этом прочность и твердость металла повышается, а пластичность и вязкость снижаются. Явление упрочнения металла при пластической деформации называется наклепом, или нагартовкой.
Волокнистое строение и наклеп можно устранить при нагреве металла. Частичное снятие наклепа происходит уже при небольшом нагреве. Снимается искажение кристаллической решетки. Этот процесс называется возвратом (рис. 2.7). Но волокнистая структура при этом сохраняется.
При нагреве до более высоких температур в металле происходит образование новых равноосных зерен. Такой процесс называют рекристаллизацией. Наклеп при этом снимается полностью. Различают рекристаллизацию первичную и собирательную.
Рекристаллизация первичная (участок 1–2 на рис. 2.7) заключается в образовании зародышей и росте новых равновесных зерен с неискаженной кристаллической решеткой.
Собирательная рекристаллизация – вторая стадия процесса, заключающаяся в росте образовавшихся новых зерен. Рост зерен обусловлен стремлением системы к более равновесному состоянию за счет уменьшения внутренней поверхности зерен. Особенность собирательной рекристаллизации – вторичная рекристаллизация – рост отдельных зерен за счет других. Основными факторами, определяющими величину зерен, являются температура, продолжительность выдержки при нагреве и степень деформации.

Рис. 2.7. Схема изменения структуры и свойств наклепанного металла
при возврате (отдыхе) и рекристаллизации
Температура, при которой идет процесс рекристаллизации, называется температурой рекристаллизации. Абсолютная температура рекристаллизации
где а – коэффициент, зависящий от структуры и состава металла. Для особо чистых металлов а = 0,2, для металлов технической чистоты а = 0,3 – 0,4, для сплавов а = 0,5 – 0,6.
На практике наклеп устраняют рекристаллизационным отжигом.
Если деформирование происходит при температуре выше температуры рекристаллизации, то наклепа не происходит. Такая деформация называется горячей. Деформация, которая происходит при температуре ниже температуры рекристаллизации, называется холодной.
Тема 1.3. Строение металлических сплавов
В конце предыдущей темы отмечалось, что создание сплавов – наиболее общий путь повышения прочности металлических материалов. Этот метод (сплавления) позволяет получить также более широкий диапазон особых полезных свойств (например, жаропрочность, коррозионную стойкость, тепло – и износостойкость и др.).
Сплавы– это материалы, полученные сплавлением или спеканием (порошковая металлургия) двух или более компонентов.
Компоненты – вещества, образующие сплав; ими могут быть химические элементы или устойчивые химические соединения.
Структура и свойства сплава определяются в первую очередь природой (типом) фаз, образующихся при сплавлении компонентов.
Фаза– однородная по химическому составу, типу решетки и свойствам часть сплава, отделенная от других частей границей раздела.
В зависимости от характера физико–химического взаимодействия компонентов в металлических сплавах возможны триосновныхтипа твердых(кристаллических)фаз:
1) химические элементы,
2)химические соединения,
3)твердые растворы.
Основной (матричной) фазой большинства промышленных сплавов являются твердые растворы, поэтому рассмотрим их более подробно.
Твердые растворы – это фазы, в которых атомы одного компонента В размещены (растворены) в кристаллической решетке другого компонента А – «растворителя». По мере увеличения числа атомов В в решетке А химический состав и свойства твердого раствора плавно изменяются (в частности, температура плавления), т.е. это фазы переменного состава (в отличие от химических элементов и химических соединений).
Сплав, представляющий собой твердый раствор, является однофазным веществом с решеткой, присущей основному компоненту (растворителю). Атомы второго компонента (растворенного) размещены в решетке растворителя, как правило, случайным, неупорядоченным образом.
 |
По способу размещения атомов растворенного вещества (В) в решетке А различают два основных типа твердых растворов – растворы замещения и внедрения (рис. 1.3.1)
Рис. 1.3.1. Твердые растворы замещения (а) и внедрения (б)
Видно, что при образовании твердых растворов замещения атомы В располагаются в вакансиях решетки компонента А (см. рис. 1.2.5). При этом количество атомов В в решетке А может изменяться в широких пределах (при определенных условиях возможна даже неограниченная взаимная растворимость компонентов в твердом состоянии).
В случае твердых растворов внедрения атомы В располагаются в междоузлиях решетки А. Понятно, что это возможно, если размеры атомов В сравнимы с размерами межатомных пустот решетки А. Поэтому растворы внедрения образуют с металлами элементы, имеющие наименьший атомный радиус (H, B, C, N). Такие растворы всегда имеют ограниченную растворимость.
Очевидно, что растворенные атомы (В) являются точечными дефектами, вызывающими искажение решетки А (см. рис. 1.2.6), поэтому образование сплавов – твердых растворов должно приводить к повышению прочности исходных компонентов (см. параграфы 1.2.2 и 1.2.3).
Химические соединения обычно имеют фиксированный состав, отвечающий формуле АnВm , где n и m – простые числа, причем тип решетки соединения Аn Вm отличается от решетки исходных компонентов.
В железоуглеродистых сплавах (сталях и чугунах), которые обсуждаются в последующих темах, наиболее важны соединения металлов (например, железа) с углеродом – карбиды.
Независимо от природы химические соединения в металлических сплавах, как правило, обладают высокой твердостью и хрупкостью(т.е. малопластичны); твердые растворы, напротив, имеют хорошую пластичность (и вязкость), но невысокую прочность и твердость.
Поэтому оптимальному сочетанию свойств конструкционных металлических сплавов (высоким значения прочности и ударной вязкости) соответствует структура, в которой дисперсные (» 10 нм) частицы твердых химических соединений равномерно и достаточно плотно (на расстояниях » 20…40 нм) распределены в пластичной матричной фазе – твердом растворе.
Исходя из этого можно сказать, что свойства сплавов зависят в первую очередь от природы и относительных количеств присутствующих фаз, но также и от формы, размеров, взаимного расположения кристаллов этих фаз, т.е. от конкретной структуры сплава. Например, если частицы химических соединений расположены в виде сетки в твердом растворе, эксплуатационная надежность такого материала будет понижена из-за возможности облегченного разрушения по хрупким оболочкам (химических соединений), разобщающим зерна твердого раствора.
Итак,свойства сплавов(данного химического состава)определяются их структурой. Чтобы прогнозировать свойства какого-либо сплава, нужно знать его структуру.
Структуру сплавов различного химического состава можно установить путем анализа соответствующих диаграмм фазового равновесия или диаграмм состояния.[4]
Под состоянием понимают наличие тех или иных фаз в сплаве данного химического состава при данной температуре. То есть диаграммы состояния строятся в координатах «температура–химический состав сплавов системы А–В».
Линии диаграмм состояния – это линии фазовых превращений («критические линии»), при пересечении которых фазовый состав (структура) сплавов обязательно изменяется.
Умение анализировать диаграммы состояния является важной частью освоения курса материаловедения. К сожалению, из-за ограниченности объема «Опорного конспекта» нет возможности посвятить этому вопросу отдельную тему, но рекомендуется самостоятельно проработать соответствующую тему (см. [1…4, 8]). Это облегчит усвоение материала последующих тем, посвященных структуре и свойствам конкретных промышленных сплавов.
Внимание!
Тема 1.3 – небольшая по объему и достаточно простая для восприятия, однако она содержит ряд новых понятий, для усвоения которых требуются определенные усилия, поэтому…
Вопросы для самопроверки к теме 1.3
1. Дайте определение понятий «сплав», «компонент», «фаза». Может ли двухкомпонентный сплав быть однофазным?
2. Какое слово является ключевым в определении понятия «фаза»?
3. Перечислите основные типы кристаллических фаз в металлических сплавах?
4. Что такое твердый раствор? Какие типы твердых растворов существуют?
5. В чем принципиальное отличие химических соединений от твердых растворов? Как отличаются механические свойства этих фаз?
6. Как Вы представляете себе оптимальную структуру конструкционных сплавов? Нарисуйте ее.
7. В каких координатах строятся диаграммы состояния?
8. Каков основной смысл линий диаграмм состояния?
9. Какова роль диаграмм состояния в курсе материаловедения?
Напоминаем, что с темой «Диаграммы состояния двойных сплавов» крайне желательно ознакомиться в учебной литературе [1-4, 8], поскольку изучение структуры и свойств конкретных промышленных сплавов во многом базируется на анализе соответствующих диаграмм состояния (см., например, темы 2.1 и 2.2).
Промежуточные тесты к теме 1.3
I. Какая из перечисленных характеристик не входит в определение понятия «фаза»?
4. Граница раздела.
5. Химический состав.
II. Какое из перечисленных утверждений неверно? В результате сплавления компонентов А и В сплав может быть:
4) твердым раствором;
5) химическим соединением.
III. Какой термин в следующем перечне является лишним?
1. Химический элемент.
3. Химическое соединение.
5. Твердый раствор.
IV. Какое из перечисленных утверждений неверно?
По сравнению с твердыми растворами химические соединения в металлических сплавах:
1) более твердые;
2) имеют постоянный химический состав;
3) менее пластичны;
4) имеют определенную температуру плавления;
5) имеют бóльшую ударную вязкость.
V. Какой из перечисленных факторов является определяющим в формировании механических свойств сплавов?
3.1. Общие сведения о металлах, сплавах металлов и их свойствах
♦ Металлами являются вещества, характеризующиеся в обычных условиях высокими электро- и теплопроводностью, ковкостью, «металлическим» блеском, непрозрачностью и другими свойствами, обусловленными наличием в их кристаллической решетке большого количества не связанных с атомными ядрами подвижных электронов проводимости.
В технике металлы принято делить на черные (железо и сплавы на его основе) и цветные (все остальные).
Свойства металлов объясняются особенностями их строения:
─ расположением и характером движения электронов в атомах;
─ расположением атомов, ионов и молекул в пространстве;
─ размерами, формой и характером кристаллических образований.
Особенности атомного строения определяют характер взаимодействия металлов, способность их давать различного рода соединения, в которые входят несколько металлов, металлы с неметаллами и т.д.
При разных температурах некоторые химические элементы имеют два и более устойчивых типа кристаллических решеток. Существование одного металла в различных кристаллических формах (модификациях) при разных температурах называется полиморфизмом, или аллотропией, а переход из одного строения в другое — полиморфным (аллотропическим) превращением. Аллотропические формы, получающиеся в результате полиморфного превращения, обычно обозначают начальными буквами греческого алфавита.
К таким полиморфным металлам относятся, например, кобальт (Со), олово (Sn), марганец (Mn), железо (Fe). В свою очередь, изменение строения кристаллической решетки вызывает изменение свойств — механических, химических и магнитных, электропроводности, теплопроводности, теплоемкости и др.
К металлам, которые имеют только один тип кристаллической решетки и называются изоморфными, относятся алюминий (Аl), медь (Cu), никель (Ni), хром (Сr), ванадий (W) и др.
Наиболее полную информацию о строении и свойствах металлов получают при использовании комплекса методов исследований:
─ структурных (основаны на макроскопическом, микроскопическом анализах строения металла или сплава и др.);
─ физических (основаны на измерении различных физических свойств: тепловых, магнитных и др.).
Так, например, метод элементного микроанализа изменения поверхности стоматологических сплавов в условиях ротовой полости применяется многими исследователями (Hani Н. et al., 1989).
♦ Металлические сплавы - это макроскопически однородные системы, состоящие из двух или более металлов с характерными металлическими свойствами. В широком смысле сплавами называются любые однородные системы, получаемые сплавлением металлов, неметаллов, оксидов, органических веществ.
Структура и свойства чистых металлов (см. табл. 21) существенно отличаются от структуры и свойств сплавов (см. табл. 22), состоящих из двух и более металлов.
По количеству элементов (компонентов сплава) различают двух-, трех- или многокомпонентные сплавы (см. табл. 19, 28, 31, 35, 38—40).
Образование новых однородных веществ при взаимном проникновении атомов называют фазами сплава.
В расплавленном виде все компоненты обычно находятся в атомарном состоянии, образуя неограниченный жидкий однородный раствор, в любой точке которого химический состав статистически одинаков. При затвердевании расплава атомы компонентов укладываются в порядке кристаллической решетки, образуя твердое кристаллическое вещество — сплав.
Существуют три типа взаимоотношений компонентов сплава:
- образование механической смеси, когда каждый элемент кристаллизуется самостоятельно, при этом свойства сплава будут усредненными свойствами элементов, которые его образуют;
- образование твердого раствора, когда атомы компонентов образуют кристаллическую решетку одного из элементов, являющегося растворителем, при этом тип решетки основного металла сохраняется;
- образование химических соединений, когда при кристаллизации разнородные атомы могут соединяться в определенной пропорции с образованием нового типа решетки, отличающейся от решеток металлов сплава. Образование химического соединения — сложный процесс, при котором создается новое вещество с новыми качествами, а решетка при этом имеет более сложное строение. Соединение теряет основное свойство металла — способность к пластической деформации, становится хрупким.
Соответственно этому, свойства сплавов будут зависеть от того, какие фазы в них образуются: твердые растворы, химические соединения или смеси чистых металлов. Если атомные объемы двух металлов и их температуры плавления резко отличаются, то в жидком состоянии такие элементы обладают, как правило, ограниченной растворимостью.
В то же время неограниченную растворимость, или способность образовывать твердые растворы в любых пропорциях, имеют только металлы с кристаллической решеткой одного типа. Металлы, расположенные недалеко друг от Друга в таблице Менделеева (Сu29 и Ni28; Fe26 и Ni28; Fe26 и Cr24; Fe26 и Co27; Co27 и Ni28) или расположенные в одной группе (As33 и Sb51; Au79 и Ag47; Au79 и Cu29; Bi83 и Sb51), имеют неограниченную растворимость.
Таким образом, взаимодействие элементов в сплавах и характер образующейся структуры определяются положением элементов в таблице Менделеева типом кристаллической решетки, размерами атомов, т.е. физической природой элементов.
Зависимость свойств от состава сплавов:
─ в сплавах, имеющих структуру механических смесей, свойства изменяются в основном прямолинейно. Некоторые свойства механических смесей, в первую очередь твердость и прочность, зависят от размеров частиц (от степени дисперсности) и значительно повышаются при измельчении;
─ в сплавах-твердых растворах — свойства изменяются по криволинейной зависимости;
─ при образовании химических соединений свойства изменяются скачкообразно.
Многие физические и механические свойства сплавов четко зависят от структуры, однако некоторые технологические свойства, такие как литейные (способность обеспечить хорошее качество отливки) или свариваемость, зависят не столько от структуры, сколько от того, в каких температурных условиях проходило затвердевание сплавов.
Так, например, стоматологические сплавы золота, отлитые в форму и быстро охлажденные в воде, будут иметь вид твердого раствора, отличающегося характерной мягкостью, ковкостью и меньшей прочностью, чем сплавы с упорядоченным расположением атомов (Копейкин В.Н., 1995). Однако если ту же отливку охлаждать медленно до комнатной температуры, то твердый раствор, превалирующий при температуре более 424°С, полностью переходит в фазу AuCu путем перераспределения атомов в пространственной кристаллической решетке в более упорядоченную структуру. Это приводит к повышению прочности и твердости при потере ковкости сплава. Сплавы с высоким содержанием золота (выше 88%) не образуют упорядоченной фазы.
Поэтому о зависимости механических и физических свойств однофазных сплавов (α и β) говорят следующие положения, известные из курса металловедения:
─ твердость, прочность и электросопротивление твердых растворов выше, чем у чистых металлов;
─ электропроводность и температурный коэффициент электросопротивления у твердых растворов ниже, чем у чистых металлов;
─ электрохимический потенциал при этом изменяется по плавной кривой.
Помимо свойств металлической матрицы, имеющей определенную кристаллическую решетку и тем самым определяющую основные параметры механических свойств, на последние может оказывать влияние дополнительное легирование такими элементами, как молибден, вольфрам, ниобий, углерод, азот и др. Присутствие их в сплавах даже в небольших количествах значительно повышает прочность, износостойкость, жаропрочность и другие свойства, необходимые при эксплуатации конструкций.
Добавка небольших количеств (0,005%) иридия и рутения превращает грубую зернистую структуру сплавов золота в мелкозернистую, что дает возможность улучшить на 30% прочность на растяжение и предел прочности при удлинении, не влияя при этом на твердость и предел текучести. Особенно эффективно увеличивается прочность при легировании кобальтохромовых сплавов 6% молибденом и дополнительно 1—2% ниобия в присутствии 0,3% углерода. В металлических сплавах образуются различные химические соединения между двумя или несколькими металлами (их называют интерметаллидами) так и между металлом и неметаллом (карбиды, оксиды и т.д.).
Наличие неметаллических включений в структуре сплава ведет к образованию усталости, трещин, внутренних пор и полостей, коррозионному растрескиванию отливок, что приводит в конечном счете к разрушению. Неметаллические включения играют существенную роль в процессе вязкого и усталостного разрушения.
Основу неметаллических включений в сплаве Виталлиум составляют марганец и кремний. В кобальтохромовом сплаве (КХС) содержатся включения нитридов титана и силикаты. Приведенные в таблице 27 данные свидетельствуют, что у образца, испытавшего циклическую нагрузку, произошли изменения почти по всем параметрам: значительно уменьшены пределы упругости и текучести прочности, напряжения, разрушения, относительного удлинения и сужения. Это свидетельствует о тенденции к усталости металла.
В результате циклических напряжений металл «устает», прочность его снижается (см. табл. 27) и наступает разрушение образца (протеза). Такое явление называют усталостью, а сопротивление усталости — выносливостью. Разрушение от усталости происходит всегда внезапно вследствие накопления металлом необратимых изменений, которые приводят к возникновению микроскопических трещин — трещин усталости, возникающих в поверхностных зонах образца. При этом чем больше на поверхности царапин, выбоин и других дефектов, вызывающих концентрацию напряжения, тем быстрее образуются трещины усталости.
В связи с усталостью металла появляются микротрещины на границе неметаллических включений, зерен металла, которые в процессе циклической нагрузки увеличиваются, образуя магистральную трещину, приводящую к разрушению металла.
♦ Основной характеристикой, определяемой при испытании на усталость материала, является предел выносливости - наибольшее напряжение, которое может выдержать материал без разрушения при произвольно большом числе перемен (циклов) нагрузки. Максимальное напряжение, не вызывающее разрушения, соответствует пределу выносливости.
Кроме механических испытаний, металлические материалы подвергаются технологическим испытаниям (изгиб, перегиб и др.) с целью определения их пригодности к различным технологическим операциям в процессе использования. Приложение к образцу нагрузки при механическом испытании приводит к деформации (см. с. 11).
Материаловедение по ортопедической стоматологии
Читайте также:
