Графит имеет металлическую кристаллическую решетку
Кристаллической решеткой называют пространственное расположение атомов или ионов в кристалле. Точки кристаллической решетки, в которых расположены атомы или ионы, называют узлами кристаллической решетки.
Кристаллические решетки подразделяют на молекулярные, атомные, ионные и металлические.
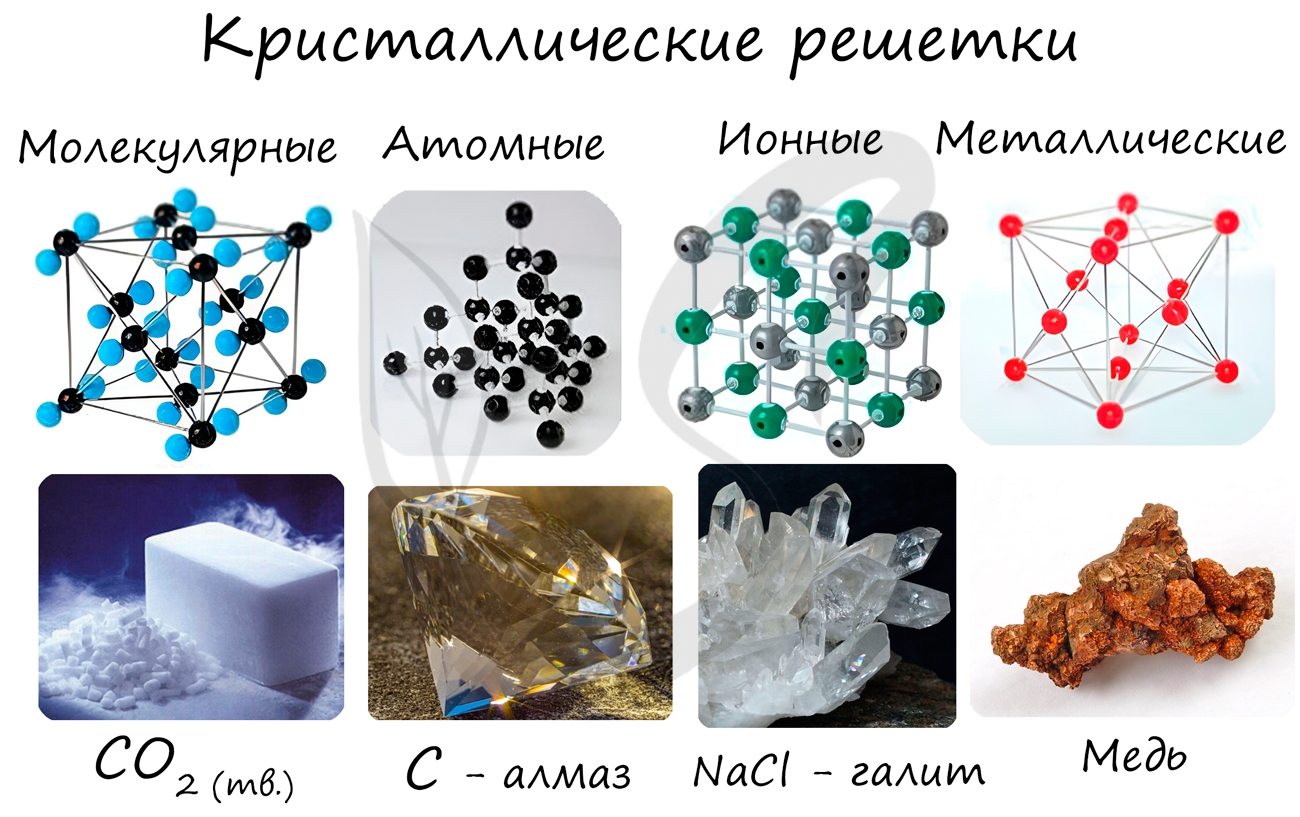
Очень важно не перепутать вид химической связи и кристаллической решетки. Помните, что кристаллические решетки отражают пространственное расположение атомов.
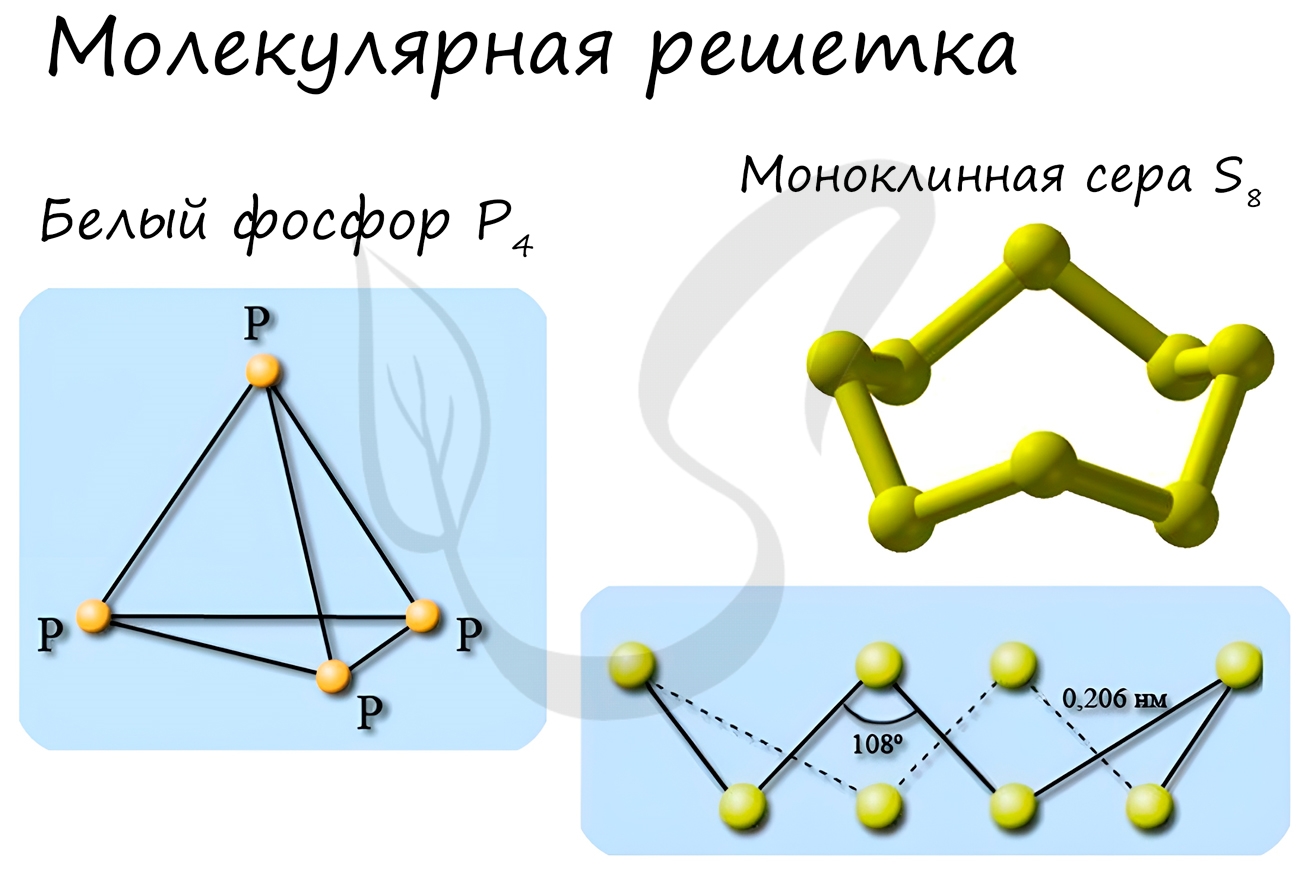
Молекулярная кристаллическая решетка
В узлах молекулярной решетки расположены молекулы. При обычных условиях молекулярную решетку имеют большинство газов и жидкостей. Связи чаще всего ковалентные полярные или неполярные.
Классическим примером вещества с молекулярной решеткой является вода, так что ассоциируйте свойства этих веществ с водой. Вещества с молекулярной решеткой непрочные, имеют небольшую твердость, летучие, легкоплавкие, способны к возгонке, для них характерны небольшие температуры кипения.
Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2. Особо хочется отметить белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы подробно изучили в статье, посвященной классификации веществ.
Ионная кристаллическая решетка
В узлах ионной решетки находятся атомы, связанные ионной связью. Этот тип решетки характерен для веществ, обладающих ионной связь: соли, оксиды и гидроксиды металлов.
Ассоциируйте этот ряд веществ с поваренной солью - NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.

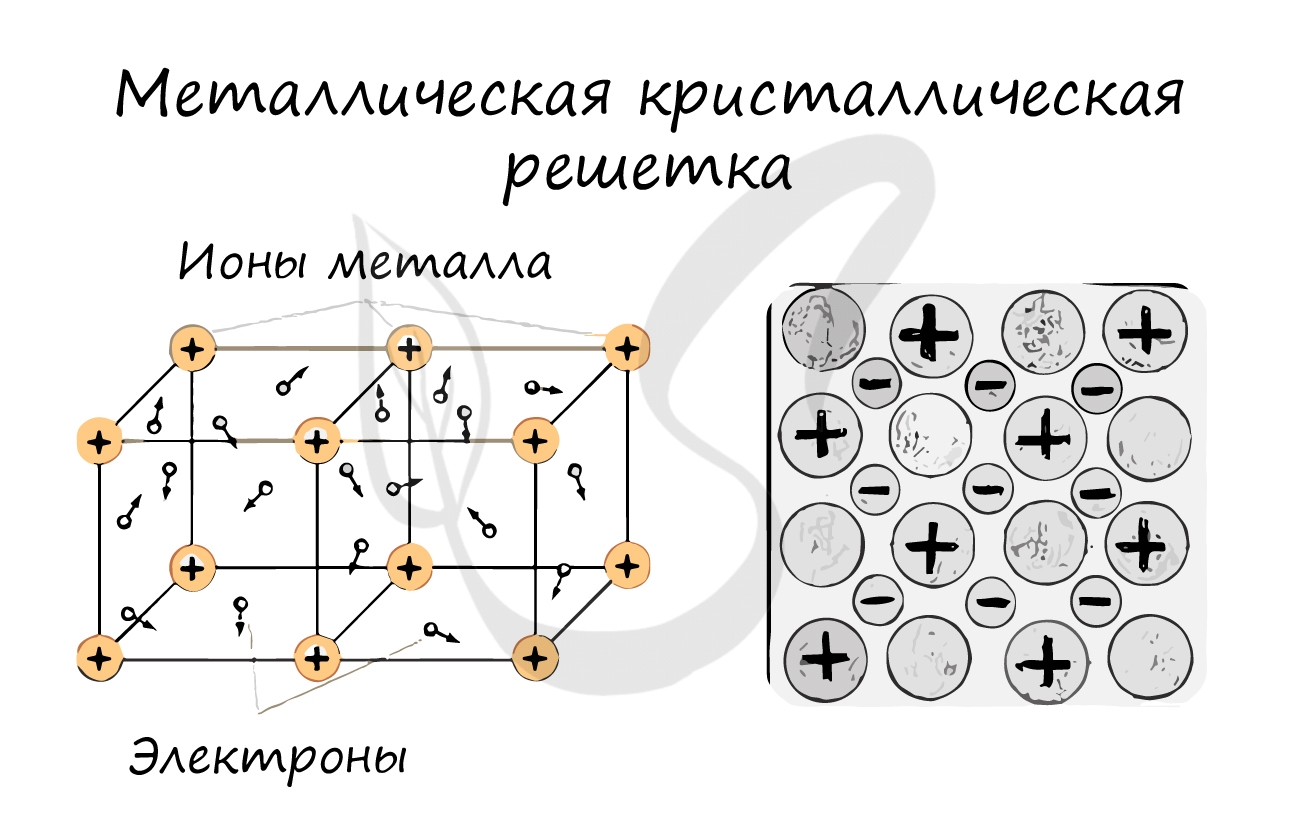
Металлическая кристаллическая решетка
В узлах металлической решетки находятся атомы металла. Этот тип решетки характерен для веществ, образованных металлической связью.
Ассоциируйте свойства этих веществ с медью. Они обладают характерным металлическим блеском, ковкие и пластичные, хорошо проводят электрический ток и тепло, имеют высокие температуры плавления и кипения.
Примеры: Cu, Fe, Zn, Al, Cr, Mn.
Атомная кристаллическая решетка
В узлах атомной решетки находятся атомы, связанные ковалентной полярной или неполярной связью.
Ассоциируйте эти вещества с песком. Они очень твердые, очень тугоплавкие (высокая температура плавления), нелетучие, прочные, нерастворимы в воде.
Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), красный и черный фосфор (P).

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Таблица типов кристаллических решёток: йода, алмаза, графита, натрия

Графит — минерал из класса самородных элементов, одна из аллотропных модификаций углерода. Минерал широко распространен в природе. Обычно встречается в виде единичных чешуек, пластинок и кластеров, различающихся по размеру и содержанию графита. Есть месторождения кристаллического графита, связанные с магматическими породами или кристаллическими сланцами, а также скрытокристаллический графит, образовавшийся во время метаморфизма углей.
- Структура
- Имущество
- Морфология
- Источник
- Заявка
- Классификация
- Физические свойства
- Оптические свойства
- Кристаллографические свойства
Агат — цена и лечебно-магические свойства
Физические свойства и структура алмаза
СТРУКТУРА

Полиморфная (аллотропная) гексагональная кристаллическая модификация чистого углерода, наиболее устойчивая в условиях земной коры. Слои кристаллической решетки могут быть расположены по-разному, образуя множество политипов, с симметрией от гексагональной системы (гексагонально-дипирамидальная симметрия) до тригональной (wc ди-тригонально-скаленоэдрической). Кристаллическая решетка графита стратифицированного типа. В слоях атомы C находятся в узлах гексагональных ячеек слоя. Каждый атом C окружен тремя соседями на расстоянии 1,42Α
Существует две модификации графита: α-графит (гексагональный P63 / mmc) и β-графит (ромбоэдрический R (-3) m). Отличаются они упаковкой слоев. В α-графите половина атомов каждого слоя находится выше и ниже центров шестиугольника (набор… ABABAB…), а в β-графите каждый четвертый слой повторяет первый. Ромбоэдрический графит удобно изобразить в гексагональных осях, чтобы показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как это метастабильная фаза. Однако в природных графитах содержание ромбоэдрической фазы может достигать 30%. При температуре 2500-3300 К ромбоэдрический графит полностью переходит в гексагональный.
Химия — удивительная наука. Столько невероятного можно обнаружить в, казалось бы, обычных вещах.
Всё материальное, что окружают нас повсюду, существует в нескольких агрегатных состояниях: газы, жидкости и твёрдые тела. Учёные выделили ещё и 4-е — плазму. При определённой температуре какое-либо вещество может переходить из одного состояние в другое. Например, вода: при нагревании свыше 100, из жидкой формы, превращается в пар. При температуре ниже 0 переходит в следующее агрегатную структуру — лёд.
Весь материальный мир имеет в своём составе массу одинаковых частиц, которые между собой связаны. Эти мельчайшие элементы строго выстраиваются в пространстве и образуют так называемый пространственный каркас.
Это интересно: анионы и катионы в химии, таблица растворимости.
СВОЙСТВА

Коэффициент теплопроводности графита от 278,4 до 2435 Вт / (м * К) зависит от марки графита, от направления относительно базисных плоскостей и от температуры.
Электропроводность монокристаллов графита анизотропна, в направлении, параллельном базисной плоскости, близка к металлической, в перпендикулярной — в сотни раз ниже. Минимальное значение проводимости наблюдается в диапазоне 300-1300 К, а положение минимума смещено в низкотемпературную область для идеальных кристаллических структур. Рекристаллизованный графит имеет самую высокую электропроводность.
Коэффициент теплового расширения графита до 700 К отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение уменьшается с повышением температуры. Выше 700 К коэффициент теплового расширения становится положительным. В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положительный, практически не зависит от температуры и более чем в 20 раз превышает абсолютное среднее значение для базальных плоскостей.
Монокристаллы графита диамагнитны, магнитная восприимчивость незначительна в базисной плоскости и высока в ортогональных базисных плоскостях. Коэффициент Холла изменяется с положительного на отрицательный при 2400 К.
Графит атомная кристаллическая решетка какая
В приведённой ниже таблице перечислены характерные свойства веществ с атомной и ионной кристаллическими решётками.
Характерные свойства веществ
— твёрдые при обычных условиях;
— в расплавах и растворах проводят электрический ток
| С атомной кристаллической решёткой | С ионной кристаллической решёткой |
Используя данную информацию, определите, какую кристаллическую решётку имеет:
1) хлорид кальция
Запишите ответ в отведённом месте:
1) Хлорид кальция имеет
Хлорид кальция — вещество с ионной химической связью, тугоплавкое (Т пл = 772 °C), проводит электрический ток — имеет ионную кристаллическую решётку.
Графит — вещество с ковалентной неполярной химической связью, нелетучее, твёрдое — имеет атомную кристаллическую решётку.
Ответ: Хлорид кальция — ионная кристаллическая решётка, графит — атомная кристаллическая решётка.
МОРФОЛОГИЯ

Хорошо сформированные кристаллы встречаются редко. Кристаллы пластинчатые, чешуйчатые, изогнутые, обычно несовершенной пластинчатой формы. Чаще всего это листья без кристаллографических очертаний и их агрегаты. Образует сплошные радиально-радиальные агрегаты скрытокристаллические, листовые или округлые, реже — сферулитовые агрегаты концентрически-зонального строения. В крупнокристаллических осадках часто наблюдается треугольная штриховка на плоскостях (0001).
Металлический тип
В своём строении напоминает молекулярную, но имеет всё же более прочные связи. Отличие данного типа в том, что на её узлах находятся положительно заряженные катионы. Электроны, которые находятся в межузловом пространстве, участвуют в образовании электрического поля. Они ещё носят название электрического газа.
Простые металлы и сплавы, характеризуются металлическим типом решётки. Для них характерно наличие металлического блеска, пластичность, тепло- и электропроводность. Они могут плавиться при различных температурах.
ПРОИСХОЖДЕНИЕ

Он образуется при высоких температурах в вулканических и магматических породах, пегматитах и скарнах. Он встречается в кварцевых жилах с вольфрамитом и другими минералами в среднетемпературных гидротермальных полиметаллических месторождениях. Распространен в метаморфических породах — кристаллических сланцах, гнейсах, мраморах. Крупные месторождения образуются в результате пиролиза угля под воздействием ловушек на угольных месторождениях (Тунгусский бассейн). Акцессорный минерал метеоритов. Попутные минералы: кварц, пирит, гранаты, шпинель.
Определение
Кристаллическая решётка — особая структура твёрдого вещества, при которой частицы стоят в геометрически строгом порядке в пространстве. В ней можно обнаружить узлы — места, где расположены элементы: атомы, ионы и молекулы и межузловое пространство.
Твёрдые вещества, в зависимости от диапазона высоких и низких температур, являются кристаллическими или аморфными — они характеризуются отсутствием определённой температуры плавления. При воздействии повышенных температур они размягчаются и постепенно переходят в жидкую форму. К такого рода веществам относятся: смола, пластилин.
В связи с этим можно поделить на несколько видов:
Но при различных температурах одно вещество может иметь различные формы и проявлять многообразные свойства. Это явление называется аллотропной модификацией.
Это интересно: металлы и неметаллы в периодической таблице Менделеева.
ПРИМЕНЕНИЕ

Для изготовления плавильных тиглей, футеровочных плит — применение основано на высокой термостойкости графита (в отсутствие кислорода), его химической стойкости к ряду расплавленных металлов. Он используется в электродах, в нагревательных элементах, благодаря своей высокой электропроводности и химической стойкости практически ко всем агрессивным водным растворам (намного выше, чем у драгоценных металлов). Для производства химически активных металлов электролизом расплавов, твердых смазок, комбинированных жидких и пастообразных смазок, пластиковых наполнителей.
это замедлитель нейтронов в ядерных реакторах, компонент композиции для изготовления стержней с черным графитом (в смеси с каолином). Он используется для получения синтетических алмазов в качестве эталона длины нанометрового диапазона для калибровки сканеров микроскопа с туннельным эффектом и атомно-силового микроскопа, для изготовления контактных щеток и токосъемников для различных электрических машин электромобили и мостовые краны с тележкой, мощные реостаты и другие устройства, где требуется надежный мобильный электрический контакт для изготовления тепловой защиты носовой части боеголовок баллистических ракет и возвращаемых космических кораблей.
| Молекулярная масса | 12,01 г / моль |
| Происхождение названия | от древнегреческого. — пиши, пиши |
| Статус IMA | действителен, впервые описан до 1959 г. (до IMA) |
Описание графита:
Графит широко распространен в природе как минерал. Он встречается обычно в виде отдельных чешуек, пластинок и скоплений, разных по величине и содержанию.
Природный графит по своему химическому составу не отличается чистотой. В большом количестве (до 10-25%) в нем присутствует зола, состоящая из разных составляющих (Fe2O3, SiO2, Аl2O3, MgO, Р2О5, CuO, СаО и др.), газы (до 2%) и битумы, иногда вода.
Также графит получается искусственным путем различными способами. Например, нагреванием смеси кокса и пека до 2 800 °C.
ФИЗИЧЕСКИЕ СВОЙСТВА
| Минеральный цвет | железо черное превращается в стальную серую |
| Цвет линии | черный становится стальным серым |
| Прозрачность | непрозрачный |
| Светить | полуметаллический |
| Декольте | очень хорошо на |
| Твердость (шкала Мооса) | 1-2 |
| Расставаться | как слюда |
| Власть | гибкий |
| Плотность (измеренная) | 2,09 — 2,23 г / см3 |
| Радиоактивность (GRApi) | 0 |
Типы и марки графита:
В соответствии с ГОСТ 17022-81 «Графит. Типы, марки и общие технические требования» выделяют следующие минералогические типы графита:
Этим же ГОСТом предусмотрены следующие марки графита: ГСМ-1, ГСМ-2, ГАК-1, ГАК-2, ГАК-3, ГК-1, ГК-2, ГК-3, ГС-1, ГС-2, ГС-3, ГС-4, П, ЭУЗ-М, ЭУЗ-II, ЭУЗ-III, ЭУТ-I, ЭУТ-II, ЭУТ-III, ГТ-1, ГТ-2, ГТ-3, ГЭ-1, ГЭ-2, ГЭ-3, ГЭ-4, ГЛ-1, ГЛ-2, ГЛ-3, ЭУН, ГЛС-1, ГЛС-2, ГЛС-3, ГЛС-4.
Им соответствуют следующие виды использования (потребления) графита:
– графит специальный малозольный,
– графит кристаллический электроугольный,
– графит кристаллический литейный,
– графит скрытокристаллический электроугольный,
– графит скрытокристаллический литейный.
Лечебное влияние
Первыми оценили графит гомеопаты. Они установили, что минерал подходит для лечения кожных патологий (экземы, псориаз, лишай, другие).
Сегодня список расширен:
- Нарушение обмена веществ.
- Сбой в работе щитовидной железы.
- Заболевания дыхательных путей (ринит, бронхиальная астма).
- Проблемы ЖКТ (гастрит, язва желудка, 12-перстной кишки, колиты).
- Женские недуги (аменорея, хроническое воспаление яичников, мастопатия).
- Конъюнктивит, катаракта, ячмень.
Минерал «курирует» также эмоциональное здоровье. Его прописывают при утренней головной боли, неврастении, апатии, депрессии.
Кристаллическая решетка и структура графита
Графит (от др.-греч. γράφω — пишу) – это природный материал, относящийся к классу самородных элементов, аллотропная модификация углерода. Он имеет слоистую структуру. Каждый слой кристаллической решетки графита может по-разному располагаться по отношению друг к другу, образуя политипы.

Графит находит свое применение в производственной и промышленной деятельности. Графитовые изделия отличаются повышенными эксплуатационными характеристиками. Графит устойчив к химическим и природным воздействиям, он достаточно прочный, хорошо проводит электрический ток, отличается низкой твердостью, относительной мягкостью, после воздействия высоких температур затвердевает.
Плотность составляет 2.23 г/см 3 . Графит имеет металлический блеск и темно-серый цвет. Теплопроводность этого минерала достаточно большая, поэтому его используют для изготовления комплектующих деталей электрооборудования.
Различают месторождения кристаллического графита, связанного с магматическими горными породами или кристаллическими сланцами, и скрытокристаллического графита, образовавшегося при метаморфизме углей.
Структура графита

Гексагональная кристаллическая полиморфная (аллотропная) модификация чистого углерода, наиболее устойчивая в условиях земной коры.
Слои кристаллической решетки могут по-разному располагаться относительно друг друга, образуя целый ряд политипов, с симметрией от гексагональной сингонии (дигексагонально-дипирамидальный вид симметрии), до тригональной (дитригонально-скаленоэдрический в.с.). Кристаллическая решетка графита — слоистого типа.
В слоях атомы С расположены в узлах гексагональных ячеек слоя. Каждый атом С окружен тремя соседними с расстоянием 1,42Α
Различают две модификации графита: α-графит (гексагональный P63/mmc) и β-графит (ромбоэдрический R(-3)m). Различаются упаковкой слоёв. У α-графита половина атомов каждого слоя располагается над и под центрами шестиугольника (укладка …АВАВАВА…), а у β-графита каждый четвёртый слой повторяет первый. Ромбоэдрический графит удобно представлять в гексагональных осях, чтобы показать его слоистую структуру.
β-графит в чистом виде не наблюдается, так как является метастабильной фазой. Однако, в природных графитах содержание ромбоэдрической фазы может достигать 30 %. При температуре 2500-3300 К ромбоэдрический графит полностью переходит в гексагональный.

Хорошо проводит электрический ток. В отличие от алмаза обладает низкой твёрдостью (1 по шкале Мооса). Относительно мягкий. После воздействия высоких температур становится немного твёрже, и становится очень хрупким. Плотность 2,08—2,23 г/см³.
Цвет тёмно-серый, блеск металлический. Неплавкий, устойчив при нагревании в отсутствие воздуха. Жирный (скользкий) на ощупь. Природный графит содержит 10—12 % примесей глин и окислов железа. При трении расслаивается на отдельные чешуйки (это свойство используется в карандашах).
Теплопроводность графита от 278,4 до 2435 Вт/(м*К), зависит от марки графита, от направления относительно базисных плоскостей и от температуры.
Электрическая проводимость монокристаллов графита анизотропна, в направлении, параллельном базисной плоскости, близка к металлической, в перпендикулярном — в сотни раз меньше.
Минимальное значение проводимости наблюдается в интервале 300—1300 К, причём положение минимума смещается в область низких температур для совершенных кристаллических структур. Наивысшую электрическую проводимость имеет рекристаллизованный графит.
Коэффициент теплового расширения графита до 700 К отрицателен в направлении базисных плоскостей (графит сжимается при нагревании), его абсолютное значение с повышением температуры уменьшается. Выше 700 К коэффициент теплового расширения становится положительным.
В направлении, перпендикулярном базисным плоскостям, коэффициент теплового расширения положителен, практически не зависит от температуры и более чем в 20 раз выше среднего абсолютного значения для базисных плоскостей.
Монокристаллы графита диамагнитны, магнитная восприимчивость незначительна в базисной плоскости и велика в ортогональных базисным плоскостях. Коэффициента Холла меняется с положительного на отрицательный при 2400 К.

Хорошо образованные кристаллы редки. Кристаллы пластинчатые, чешуйчатые, кривогранные, обычно имеют пластинчатую несовершенную форму. Чаще бывает представлен листочками без кристаллографических очертаний и их агрегатами.
Образует сплошные скрытокристаллические, листоватые или округлые радиально-лучистые агрегаты, реже — сферолитовые агрегаты концентрически-зонального строения. У крупнокристаллических выделений часто наблюдается треугольная штриховка на плоскостях (0001).

Образуется при высокой температуре в вулканических и магматических горных породах, в пегматитах и скарнах. Встречается в кварцевых жилах с вольфрамитом и др. минералами в среднетемпературных гидротермальных полиметаллических месторождениях.
Широко распространён в метаморфических породах — кристаллических сланцах, гнейсах, мраморах. Крупные залежи образуются в результате пиролиза каменного угля под воздействием траппов на каменноугольные отложения (Тунгусский бассейн). Акцессорный минерал метеоритов. Сопутствующие минералы: кварц, пирит, гранаты, шпинель.

Для изготовления плавильных тиглей, футеровочных плит — применение основано на высокой температурной стойкости графита (в отсутствие кислорода), на его химической стойкости к целому ряду расплавленных металлов.
Применяется в электродах, нагревательных элементах — благодаря высокой электропроводности и химической стойкости к практически любым агрессивным водным растворам (намного выше, чем у благородных металлов).
Для получения химически активных металлов методом электролиза расплавленных соединений, твёрдых смазочных материалов, в комбинированных жидких и пастообразных смазках, наполнитель пластмасс.
Является замедлителем нейтронов в ядерных реакторах, компонентом состава для изготовления стержней для чёрных графитовых карандашей (в смеси с каолином).
Используется для получения синтетических алмазов, в качестве эталона длины нанометрового диапазона для калибровки сканеров сканирующего туннельного микроскопа и атомно-силового микроскопа, для изготовления контактных щёток и токосъёмников для разнообразных электрических машин, электротранспорта и мостовых подъёмных кранов с троллейным питанием, мощных реостатов.
А также прочих устройств, где требуется надёжный подвижный электрический контакт, для изготовления тепловой защиты носовой части боеголовок баллистических ракет и возвращаемых космических аппаратов.
Ионные кристаллические решетки. Свойства веществ с ионным типом кристаллической решетки.
Как мы знаем, все материальные вещества могут пребывать в трех базовых состояниях: жидком, твердом, и газообразном. Правда есть еще состояние плазмы, которое ученые считают ни много ни мало четвертым состоянием вещества, но наша статья не о плазме. Твердое состояние вещества потому твердое, так как имеет особую кристаллическую структуру, частицы которой находятся в определенном и четко заданном порядке, создавая, таким образом, кристаллическую решетку. Строение кристаллической решетки состоит из повторяющихся одинаковых элементарных ячеек: атомов, молекул, ионов, других элементарных частиц, связанных между собой различными узлами.

Хорошо образованные кристаллы редки. Кристаллы пластинчатые, чешуйчатые, кривогранные, обычно имеют пластинчатую несовершенную форму. Чаще бывает представлен листочками без кристаллографических очертаний и их агрегатами. Образует сплошные скрытокристаллические, листоватые или округлые радиально-лучистые агрегаты, реже — сферолитовые агрегаты концентрически-зонального строения. У крупнокристаллических выделений часто наблюдается треугольная штриховка на плоскостях (0001).
Кристаллографические свойства
| Точечная группа | 6 mm — дигексагонально-пирамидальный |
| Пространственная группа | P63mc |
| Сингония | гексагональная |
| Параметры ячейки | a = 2.461Å, c = 6.708Å |
| Двойникование | по |
Виды решеток
В зависимости от частиц кристаллической решетки существует четырнадцать типов оной, приведем наиболее популярные из них:
Металлическаякристаллическая решетка.
Далее более подробно опишем все типы кристаллической решетки.



Катионы, их образование из атомов в результате процесса окисления. Анионы, их образование из атомов в результате процесса восстановления. Ионная связь, как связь между катионами и анионами за счет электростатического притяжения.
Химическая связь — это взаимодействие атомов, обусловливающее устойчивость химической частицы или кристалла как целого.
Химическая связь образуется за счет электростатического взаимодействия между заряженными частицами: катионами и анионами, ядрами и электронами. При сближении атомов начинают действовать силы притяжения между ядром одного атома и электронами другого, а также силы отталкивания между ядрами и между электронами. На некотором расстоянии эти силы уравновешивают друг друга, и образуется устойчивая химическая частица.
При образовании химической связи может произойти существенное перераспределение электронной плотности атомов в соединении по сравнению со свободными атомами. В предельном случае это приводит к образованию заряженных частиц — ионов (от греческого «ион» — идущий).
Если атом теряет один или несколько электронов, то он превращается в положительный ион — катион (в переводе с греческого — «идущий вниз). Так образуются катионы водорода Н+, лития Li+, бария Ва2+. Приобретая электроны, атомы превращаются в отрицательные ионы — анионы (от греческого «анион» — идущий вверх). Примерами анионов являются фторид ион F−, сульфид-ион S2−.
Катионы и анионы способны притягиваться друг к другу. При этом возникает химическая связь, и образуются химические соединения. Такой тип химической связи называется ионной связью:
Ионная связь, как правило, возникает между атомами типичных металлов и типичных неметаллов. Характерным свойством атомов металлов является то, что они легко отдают свои валентные электроны, тогда как атомы неметаллов способны легко их присоединять.
Рассмотрим возникновение ионной связи, например, между атомами натрия и атомами хлора в хлориде натрия NaCl.
Отрыв электрона от атома натрия приводит к образованию положительно заряженного иона – катиона натрия Na+.
Присоединение электрона к атому хлора приводит к образованию отрицательно заряженного иона – аниона хлора Cl-.
Между образовавшимися ионами Na+ и Cl-, имеющими противоположный заряд, возникает электростатическое притяжение, в результате которого образуется соединение – хлорид натрия с ионным типом химической связи.
Ионная связь
– это химическая связь, которая осуществляется за счет электростатического взаимодействия противоположно заряженных ионов.
Таким образом, процесс образования ионной связи сводится к переходу электронов от атомов натрия к атомам хлора с образованием противоположно заряженных ионов, имеющих завершенные электронные конфигурации внешних слоев.
1. Атомы металлов, отдавая внешние электроны, превращаются в положительные ионы:
где n — число электронов внешнего слоя атома, соответствующее номеру группы химического элемента.
2. Атомы неметаллов, принимая электроны, недостающие до завершения внешнего электронного слоя
, превращаются в отрицательные ионы:
3. Между разноимённо заряженными ионами возникает связь, которая называется

2 . Классификация ионов: по составу, знаку заряда, наличию гидратной оболочки.
Классификация ионов:
1. По знаку заряда: катионы (положительные, K+, Ca2+, H+) и анионы (отрицательные, S2-, Cl-, I-). 2. По составу: сложные ( , ) и простые (Na+, F-)
Ионные кристаллические решетки. Свойства веществ с ионным типом кристаллической решетки.
| Ионными называют кристаллические решетки, в узлах которых находятся ионы. Их образуют вещества с ионной связью. Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов. Рассмотрим строение кристалла поваренной соли, в узлах которого находятся ионы хлора и натрия. |

Ионными называют кристаллические решетки
, в узлах которых находятся ионы. Их образуют вещества с ионной связью, которой могут быть связаны как простые ионы Na+, Cl—, так и сложные SO42- , OH—. Следовательно, ионными кристаллическими решетками обладают соли, некоторые оксиды и гидроксиды металлов. Например, кристалл хлорида натрия построен из чередующихся положительных ионов Na+ и отрицательных Cl—, образующих решетку в форме куба. Связи между ионами в таком кристалле очень устойчивы. Поэтому вещества с ионной решеткой отличаются сравнительно высокой твердостью и прочностью, они тугоплавки и нелетучи.
Кристаллическая решетка — а) и аморфная решетка — б).
Связи между ионами в кристалле очень прочные и устойчивые.Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
Вещества с ионной кристаллической решеткой обладают следующими свойствами:
1. Относительно высокой твердостью и прочностю;
Примеры: соли – хлорид натрия, карбонат калия, основания – гидрооксид кальция, гидрооксид натрия.
Атомная решетка
Вещества с атомной кристаллической решеткой, как правило, имеют в своих узлах, состоящих собственно из атомов сильные ковалентные связи. Ковалентная связь происходит, когда два одинаковых атома делятся друг с другом по-братски электронами, образуя, таким образом, общую пару электронов для соседних атомов. Из-за этого ковалентные связи сильно и равномерно связывают атомы в строгом порядке – пожалуй, это самая характерная черта строения атомной кристаллической решетки. Химические элементы с подобными связями могут похвастаться своей твердостью, высокой температурой плавления. Атомную кристаллическую решетку имеют такие химические элементы как алмаз, кремний, германий, бор.
Ковалентные кристаллы
В узлах таких кристаллических решеток содержатся отдельные атомы или молекулы, соединенные между собой ковалентными связями.
Ковалентная связь представляет собой химическую связь, которая включает разделение пар электронов между атомами. Это разделение приводит к стабильному балансу сил притяжения и отталкивания между этими атомами. Ковалентные твердые вещества представляют собой класс соединений с расширенными решетками, в которых каждый атом или молекула ковалентно связаны с ближайшими соседями. Это означает, что весь кристалл, по сути, является одной гигантской молекулой. Чрезвычайно сильные связывающие силы, которые соединяют все смежные атомы, объясняют экстремальную твердость этих твердых тел. Они не могут быть разрушены или истерты без разрушения большого количества ковалентных химических связей. Точно так же ковалентное твердое вещество не может «расплавиться» в обычном смысле, так как весь кристалл является одной гигантской молекулой. При нагревании до очень высоких температур эти твердые вещества обычно разлагаются на их элементы.
Другим свойством ковалентных твердых тел является плохая электропроводность, поскольку делокализованных электронов в таких веществах нет. В случае расплавления, в отличие от ионных соединений, такие вещества также неспособны проводить электричество, так как их макромолекулы состоят из незаряженных атомов, а не ионов.
Теперь, зная вид химической связи в веществе, можно охарактеризовать не только ее количественный и качественный состав, но и физические свойства.
Металлическая решетка
Тип связи металлической кристаллической решетки гибче и пластичнее ионной, хотя внешне они весьма похожи. Отличительной особенностью ее является наличие положительно заряженных катионов (ионов метала) в узлах решетки. Между узлами живут электроны, участвующие в создании электрического поля, эти электроны еще называются электрическим газом. Наличие такой структуры металлической кристаллической решетки объясняет ее свойства: механическую прочность, тепло и электропроводность, плавкость.
Различные вещества
- Алмаз. Минерал обладает высокой ценностью и после огранки используется в ювелирных украшениях. Так в чём же заключается секрет популярности этого камня? Атомы углерода составляют основу всей решётки. Между атомами минерала существует прочная ковалентная связь. Для кристаллической решётки алмаза характерно плотное содержание атомов в виде куба. Другими словами, узлами считаются атомы углерода, а своеобразными гранями куба являются прочные ковалентные связи. Такой минерал считается самым прочным на планете, и неизвестно, сколько таких своеобразных кубов включает в себя цельный алмаз.
- Графит. Углерод также может быть и в другой кристаллической модификации. Атомная решётка данного элемента включает в себя только атомы углерода, ей присуща слоистая структура. В графите каждый атом связан тремя атомами углерода. Из-за этого он обладает металлическим блеском, высокой теплопроводностью.
- Кристаллическая решётка йода имеет молекулярный тип. Атомы молекул соединяются ковалентными связями, но молекулы химического элемента имеют слабые силы притяжения. Это характеризует йод тем, что он имеет малую твёрдость, низкую температуру плавления.
- Натрий. Представитель металлической кристаллической решётки. Между катионами, расположенными в узлах решётки, двигаются электроны. Они, присоединяясь к катионам, нейтрализуют их заряд, в свою очередь, нейтральные атомы отпускают часть электронов, преобразуясь в катионы. Такой тип кристаллической решётки наделяет металл пластичностью, электро- и теплопроводностью.
- Сухой лёд. Или оксид углерода в затвердевшем виде. Имеет молекулярную кристаллическую решётку в форме куба. Молекулы удерживаются между собой слабыми связями. иффузия читайте в нашей статье.
Это интересно: как определить валентность по таблице Менделеева?
Видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.

Автор: Павел Чайка, главный редактор журнала Познавайка
При написании статьи старался сделать ее максимально интересной, полезной и качественной. Буду благодарен за любую обратную связь и конструктивную критику в виде комментариев к статье. Также Ваше пожелание/вопрос/предложение можете написать на мою почту [email protected] или в Фейсбук, с уважением автор.
Эта статья доступна на английском – Crystal Lattice in Chemistry.
Графит в природе
В природе содержится в гранитах, пирите. Он образуется в магматических и вулканических горных породах, скарнах и пегматитах при высоких температурах, встречается в кварцевых жилах с различными материалами, широко распространен в мраморе, кристаллических сланцах, гнейсах. В результате пиролиза под воздействием на каменноугольные отложения траппов образуются крупные залежи природного минерала.
Показатели:
- Содержание минералов 2.0%
- Содержание углерода > 98.0%
- Содержание серы 550 ppm
- Температурный диапазон -200…3000°C
- Выщелачиваемый хлорид 50 ppm
- Сжимаемость 40%
- Регенерация 15%
- pH диапазон 0-14
- Проседание под нагрузкой
Стоимость материала
Реализацией графита и его смесей занимаются специальные организации, добывающие и получающие материал. Стоимость его находится на вполне приемлемом уровне и зависит от содержания углерода и габаритов кристалликов. У каждого сорта есть своя цена — чем больше в материале углерода, тем, соответственно, он дороже и имеет лучшие технические характеристики.
Продается графит как оптом, так и в розницу. Примечательно, что при оптовой покупке можно получить очень неплохую скидку.
Стоимость материала также зависит и от региона продажи. Средняя же цена составляет примерно 45−50 рублей за 1 кг. Графитовые изделия имеют большую стоимость.
Месторождения
Самые большие залежи графита расположены в Китае, Украине, Мексике, Канаде и Южной Корее. Месторождения минерала экономически выгодны для страны, на территории которой он расположен. В процессе разработки залежей обеспечение промышленности нужным сырьём. Камнем образованы скопления серого цвета. Графитовая руда добывается открытым способом, а кусковой минерал подземным методом.
Одним из высокотемпературных жильных залежей минералов стоит выделить месторождение на Цейлоне, которое обладает большим промышленным значением. Здесь графитовые жилы расположены среди гнейсов. Такие же месторождения есть в Квебеке, штате Монтана и Англии.
Где и как добывается
Залежи графита промышленных объемов есть на всех континентах:
- Обе Америки – США, Канада, Бразилия;
- Европа – ФРГ, Гренландия, Италия;
- Австралия.
Сырье каждого графитового рудника можно отличить по структуре, цвету, другим признакам.
Россия располагает тремя крупнейшими месторождениями:
- Бурятия – качественное плотнокристаллическое сырье.
- Краснодарский край (два) – плотно-, мелкокристаллический, чешуйчатый, графитовые сланцы.
Графиты формируются каменноугольным пиролизом либо под влиянием экстремально высоких температур и давления. Например, излияниями магмы на отложения каменного угля.
Его добывают наземным или подземным способами. Графитовые кристаллы находят в сланцах, мраморах, других органических породах.
Ежегодный мировой объем добычи графита – 600 тыс. тонн.
Запасы
Мировые запасы графита (1978, тысяч т) в капиталистических и развивающихся странах: чешуйчатого — Южная Америка, 136; Европа, 3500; Африка, 5442; Азия, 900; плотнокристаллического — Азия, 2900; скрытокристаллического — Северная Америка (без США), 3084; Европа, 5623; Азия, 6168. О добыче графита см. в ст. графитовая промышленность.
Получение алмаза из графита
Формула графита — C — позволила ученым произвести множество опытов, вследствие чего были найдены аллотропные вещества графита.
Преподаватели рассказывают и школьникам, и студентам о том, как ученые пытались создать алмазы из графита. Эта история очень интересная и увлекательная, а еще она позволяет запомнить о существовании таких аллотропных веществ, как графит и алмаз, и об их различиях.
Некоторое время назад ученые пытались создать алмазы из графита. Они считали, что если формула алмаза и графита одинакова, то они смогут создать алмаз, ведь камень очень дорогой и редкий. Теперь мы знаем, что минерал алмаз появляется в природе при высоком давлении и мгновенном охлаждении. Поэтому ученые решили взорвать ѓрафит, тем самым создав нужные условия для образования алмаза. И на самом деле случилось чудо, после взрыва на графите образовались очень маленькие кристаллы алмаза.

Кристаллическое строение металлов. Кристаллическая решетка металлов

Металлы – особая группа элементов в периодической таблице Менделеева. В отличие от неметаллов элементы этой группы являются исключительно восстановителями с положительной степенью окисления, а также обладают пластичностью, твёрдостью, упругостью, что обусловлено кристаллическим строением металлов.
Общее строение
Металлы – твёрдые вещества, имеющие кристаллическое строение. Исключение составляет ртуть – жидкий металл. Кристаллические решётки представляют собой упорядоченные определённым образом атомы металла. Каждый атом состоит из положительно заряженного ядра и нескольких отрицательно заряженных электронов. В атомах металлов недостаточно электронов, поэтому они являются ионами.
Единица кристаллической решётки – элементарная кристаллическая ячейка, в условных узлах и на гранях которой находятся положительно заряженные ионы. Их удерживают вместе металлические связи, возникающие за счёт беспорядочного движения отделившихся от атомов электронов (благодаря чему атомы превратились в ионы).
Отрицательно заряженные электроны держат на равном расстоянии положительно заряженные электроны, предавая кристаллической решётке правильную геометрическую форму.

Рис. 1. Схема металлической связи.
Свободное движение электронов обусловливает электро- и теплопроводность металлов.
Кристаллизация сплавов
Переход металла из жидкого состояния в твёрдое с образованием кристаллической структуры называется первичной кристаллизацией.
Образования новых кристаллов в твёрдом кристаллическом веществе называется вторичной кристаллизацией (перекристаллизацией).
Процесс кристаллизации состоит из двух одновременных процессов:
- зарождение кристаллов;
- линейный рост кристаллов;
Кристаллы могут зарождаться самопроизвольно (самопроизвольная кристаллизация) или зарождаться и расти на имеющихся готовых центрах кристаллизации (не самопроизвольная кристаллизация) (рис 33).

Рис 34 Рост зародышевых центров и рост кристаллов
Самопроизвольная кристаллизация (рис.35) обусловлена стремлением вещества иметь более устойчивое состояние, характеризуемое уменьшением термодинамического потенциала G, характеристика свободной энергии системы. Второй закон термодинамики – любая система всегда стремится занять то состояние, чтобы она обладала min свободной энергией. Температура, при которой термодинамические потенциалы вещества, как в твёрдом, так и в жидком состояниях равны, называется равновесной температурой (термодинамической температурой) ТG.

Рис.35 Самопроизвольная кристаллизация
Термодинамический потенциал определяется:
G = Е – ТS + РV (по Гельмгольцу)
где G – термодинамический потенциал, свободная энергия системы,
Е – внутренняя энергия системы,
Т – термодинамическая температура
S – энтропия (функция состояния: порядка и беспорядка, связанное с поступательным и колебательным движением),
РV – работа внешних сил (давление на объём)
G = Н – ТS (по Гиббсу)
где Н – энтальпия (Е + РV) сумма работ внутренних и внешних сил.
Разница между равновесной (ТG.) и реальной (Тр) температурой кристаллизации называется степенью переохлаждения (Δ Т).
Образованию зародышей способствуют флуктуации энергии, т.е. отклонение энергии группировок атомов в отдельных зонах жидкого металла от некоторого среднего значения.
Появление зародышей изменяет термодинамический потенциал (свободную энергию) всей системы. С одной стороны, при переходе жидкости в кристаллическое состояние термодинамический потенциал G уменьшается, с другой стороны, он увеличивается (+) вследствие появления поверхности раздела между жидкостью и кристаллическим зародышем.
На рис.36 показано, как изменяется свободная энергия системы при кристаллизации.
Кинетика кристаллизации. Скорость образования зародышей, образующихся в единицу времени в единице объёма (1мм-3с-1); скорость роста – увеличением линейных размеров, растущих кристалла в единицу времени (мм/с). Оба процесса связаны с перемещением атомов и зависят от температуры (степени переохлаждения Δ Т).
Не самопроизвольная кристаллизация (гетерогенная)
В реальных условиях процессы кристаллизации и характер образующих структур в значительной мере зависят от имеющихся готовых центров кристаллизации. Такими центрами являются:
- тугоплавкие частицы неметаллических включений;
- оксиды;
- интерметаллические соединения, образуемых примесей.
Измельчение структуры способствует улучшению механических свойств металла.

Рис.36 Изменение свободной энергии при кристаллизации
На практике для измельчения структуры металла и сплавов широко применяют технологическую операцию, называемую модифицированием. Она состоит во введении в жидкий сплав перед заливкой специальных добавок модификаторов (бор в сталь, натрий в алюминий и его сплавы). Подстуживание металла перед заливкой до температур, незначительно превышающих температуру плавления металла, способствует уменьшению размера зерна.
Формирование кристаллов
Форма и размер зёрен, образующихся при кристаллизации, зависят:
- скорости и направления отвода тепла:
- температуры жидкого металла;
- содержание примесей.
Структура слитка зависит от многих факторов: (рис.37)
- количество и свойства примесей в чистом металле;
- количества легирующих элементов в сплаве;
- температуры разливки сплава;
- скорость охлаждения при кристаллизации и т.д.

Рис.37 Схема строения металлического слитка, полученного при разных температурах
Типичная структура слитка сплавов состоит из трёх зон: (рис.38)
- мелкие равноосные кристаллы на поверхности слитка, из-за большой степени переохлаждения;
- столбчатые кристаллы, наиболее благоприятно ориентированные по отношению к теплоотводу, расположенные нормально к стенкам формы;
- равноосные кристаллы больших размеров в середине слитка, где наблюдается наименьшая степень переохлаждения и не ощущается направленного отвода тепла.
Структура, состоящая из одних столбчатых кристаллов, называется транскристаллитной. Встречается у слитков очень чистых металлов.
Химическая неоднородность по отдельным зонам слитка называется зональной ликвацией. Она отрицательно влияет на механические свойства сплава. В реальных сплавах кроме зональной встречаются и другие виды ликвации.
Виды решёток
Элементарные кристаллические ячейки могут иметь различную конфигурацию. В связи с этим выделяют три типа кристаллических решёток:
- объемно-центрированная (ОЦК) кубическая – состоит из 9 ионов;
- гранецентрированная (ГЦК) кубическая – включает 14 ионов;
- гексагональная плотноупакованная (ГПУ) – состоит из 17 ионов.
ОЦК представляет собой куб, в узлах которого находится по атому. В центре куба, на пересечении диагоналей располагается девятый ион. Этот тип характерен для железа, молибдена, хрома, вольфрама, ванадия.
Элементарной кристаллической ячейкой типа ГЦК является куб с ионами в узлах и в середине каждой грани – на пересечении диагоналей. Такое строение имеют медь, серебро, алюминий, свинец, никель.
Третий тип имеет вид гексагональной призмы, в узлах которой находится по шесть ионов с каждой стороны. Посередине между шестью узлами располагается по одному иону. В середине призмы между шестиугольными гранями находится равносторонний треугольник, который составляют три иона.

Рис. 2. Типы решёток.
Металл может содержать большое количество дефектов атомного строения. Дефекты влияют на свойства металла.
Кристаллические решетки

Примеры: NH3, H2O, Cl2, CO2, N2, Br2, H2, I2. Особо хочется отметить белый фосфор, ромбическую, пластическую и моноклинную серу, фуллерен. Эти аллотропные модификации мы подробно изучили в статье, посвященной классификации веществ.

Ассоциируйте этот ряд веществ с поваренной солью — NaCl. Веществе с ионной решеткой имеют высокие температуры плавления и кипения, легко растворимы в воде, хрупкие, твердые, их растворы и расплавы проводят электрический ток.
Примеры: NaCl, MgCl2, NH4Br, KNO3, Li2O, Na3PO4.


Примеры: SiO2, B, Ge, SiC, Al2O3. Особенно хочется выделить: алмаз и графит (C), красный и черный фосфор (P).

Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию



Характеристика решётки
Кристаллические решётки характеризуются компактностью или степенью наполненности. Компактность определяют показатели:
- параметр решётки – расстояние между атомами;
- число атомов;
- координационное число – количество соседних ячеек;
- плотность упаковки – отношение объёма, занимаемого атомами, к полному объёму решётки.
При подсчёте количества атомов следует помнить, что атомы в узлах и на гранях входят в состав соседних ячеек.

Рис. 3. Кристаллические ячейки составляют решётку.
Общее понятие о металлах
«Химия. 9 класс» — это учебник, по которому проходят обучение школьники. Именно в нем подробно изучаются металлы. Рассмотрению их физических и химических свойств отведена большая глава, ведь разнообразие их чрезвычайно велико.
Именно с этого возраста рекомендуют давать детям представление о данных атомах и их свойствах, ведь подростки уже вполне могут оценить значение подобных знаний. Они прекрасно видят, что окружающее их разнообразие предметов, машин и прочих вещей имеет в своей основе как раз металлическую природу.
Что же такое металл? С точки зрения химии, к данным атомам принято относить те, что имеют:
- малое число электронов на внешнем уровне;
- проявляют сильные восстановительные свойства;
- имеют большой атомный радиус;
- как простые вещества обладают рядом специфических физических свойств.
Основу знаний об этих веществах можно получить, если рассмотреть атомно-кристаллическое строение металлов. Именно оно объясняет все особенности и свойства данных соединений.
В периодической системе для металлов отводится большая часть всей таблицы, ведь они образуют все побочные подгруппы и главные с первой по третью группу. Поэтому их численное превосходство очевидно. Самыми распространенными являются:
- кальций;
- натрий;
- титан;
- железо;
- магний;
- алюминий;
- калий.
Все металлы имеют ряд свойств, которые позволяют объединять их в одну большую группу веществ. В свою очередь, эти свойства объясняет именно кристаллическое строение металлов.
Читайте также:
