Германий металл где содержится
Г Германий является химическим элементом таблицы Менделеева с атомным номером 32 и условным обозначением Ge. Германий представляет собой блестящий, хрупкий, серовато-белый металлоид из углеродной группы.
Как был открыт Германий
История открытия германия очень таинственная. Русский ученый и химик Д.И. Менделеев в своей работе «Периодический закон химических элементов» предположил существование нескольких неизвестных пока химических элементов в 1869 году. Одним из таких элементов был как раз и германий. Дмитрий Иванович назвал этот элемент «экосиликон» и предположил, что его вес будет равен 72 а.е.м.
Через 16 лет в середине 1885 года в одной из шахт расположенных вблизи Фрайдберга (Германия) бвл обнаружен новый минерал. Его назвали аргиродитом из-за высокого содержания серебра. Немецкий химик Клеменс Винклер проанализировал новый минерал и выяснил, что он состоит из серебра, серы и неизвестного элемента. В 1886 году Винклер смог выделить новый элемент и выявил, что он похож на сурьму.
Клеменс Винклер перед тем как опубликовать данные своих опытов решил, что назовет новый элемент нептуний. Это решение он принял потому что открытию планеты Нептун так же предшествовали математические расчеты, как и в истории с Менделеевым. Как оказалось это имя было уже занято другим элементом, но не тем которое имеет такое название сейчас. Сегодняшний нептуний был открыт только в 1940 году. По-этому Винклер принял решение назвать новый элемент Германием в честь своей Родины, аналогично Галлию.
До конца 1930-х годов предполагалось, что этот элемент плохо проводит электричество. В те времена мировое производство германия насчитывало всего несколько килограммов в год. Ситуация координально изменилась только в 1945 году, когда его признали значимым полупроводником. В 1955 году были получены первые кремний-германиевые сплавы, которые уже имели значительный коммерческий вес. К концу этого десятилетия мировое производство германия составляло порядка 40 тонн ежегодно.
Где и как добывают Германий

На сегодняшний день, мировое производство германия составляет порядка 120 тонн ежегодно. Лидерами в этом направлении являются Китай(80 тонн), Россия(5 тонн) и США(3 тонны). В большинстве случаев германий добывают в качестве побочного продукта производства таких металлов как цинк, медь, свинец и серебро. Наибольшее процентное соотношение содержания этого элемента приходится на руду цинка — сфалерит. Его содержание в этом минерале варьируется около 0.3%. По оценкам ученых в известных на сей день запасах цинка содержится как минимум 10 000 тонн германия.
Интересным моментом является то, что это не самый главный источник этого элемента. По оценкам экспертов в месторождениях угля находится порядка 120 000 тонн этого элемента. В таких месторождениях германий добывают из так называемой «летучей золы», которая являлась топливом для электростанций. Такой метод добычи германия был разработан и введен в производство в СССР в 1959 году. Алекса́ндр Адо́льфович Бу́рба совместно с Институтом «Унипромедь» разработали и внедрили его в производство на Медногорский медно-серный комбинат. Еще через три года этот метод внедрили на Ангренском химико-металлургическом заводе. Эти два завода перекрывали потребность СССР в этом химическом элементе и в 1970 году начали продавать его на экспорт. После такого успеха этой технологией начал пользоваться и Китай.
Процесс получения германия из металлических руд на примере сфалерита выглядит следующим образом. Руда методом нагревания и обжига на воздухе превращается в оксиды. В результате одна часть германия остается в пыли, а другая превращается в германаты. Вместе с цинком они выщелачиваются из шлака серной кислотой. В результате в растворе остается только цинк, а остальные металлы выпадают в виде осадка. После этого оставшийся в осадке цинк удаляется так называемым «вельц-процессом» и выщелачивается еще раз. В результате в осадке остается диоксид германия который под воздействием хлора или соляной кислоты преобразуется в тетрахлорид германия. Из-за того, что германий имеет низкую температуру кипения он может быть выделен методом отгонки.
Распространенность Германия

Германий является редким элементом как в природе так и во Вселенной. В межзвездном пространстве этот элемент вырабатывается звездным нуклеосинтезом. Преимущественно это происходит в результате S-синтеза гигантских асимптотических ветвящихся звезд. S-синтез представляет собой медленный нейтронный захват более легких элементов внутри пульсирующих красных гигантских звезд. С помощью спектрального анализа германий был обнаружен в некоторых из самых отдаленных звезд и в атмосфере Юпитера. Процентное содержание этого элемента во Вселенной не было определено.
Что же касается распространенности в земной коре, то содержание германия тут оценивается в 1.6 ppm. Это означает что на одну тонну массы содержится 1.6 граммов элемента. Сегодня науке известно лишь несколько минералов которые содержат заметное содержание металла. К германийсодержащим минералам относятся аргиродит, бриартит, германит и рениерит. Еще такими минералами являются аргутит, бартелькеит и криеселит, но содержание элемента в них чрезвычайно маленькое. Кроме всего прочего эти минералы так же встречаются массово крайне редко. Из-за этого организовать добычу из этих минералов массово не представляется возможным. Редкость элемента и трудозатраты его добычи и переработки обуславливают его высокую цену. Цена за 1 кг чистого германия может достигать 2 тысяч американских долларов. Если вдуматься в цифру то за 1 тонну чистого германия страна производитель может получить до 2 000 000$.
Применение Германия

Применение германия является довольно ограниченным из-за его редкости и высокой стоимости. Основное распределение этого элемента идет по следующим направлениям в зависимости от спроса. 35% идет на изготовление оптоволоконной продукции. 30% находят применение в различного рода тепловизорах. 15% приходится на катализаторы полимеризации. Еще 15% осваиваются для производства электроники и солнечно-электронных приборов. Оставшиеся 5% распределяются между металлургией, химиотерапией и люминофором.
Благодаря таким свойствам германия, как высокий показатель преломления и низкая оптическая дисперсия, он становится полезным для производства широкоугольных объективов камер, микроскопов и сердечной жилы оптоволокна. Так как германий прозрачен в инфракрасных длиннах волн, он становится важным оптическим материалом. Его часто используют в качестве передней оптики тепловизионных камер. Обычно такие приборы работают в диапазоне от 8 до 14 микрон.
Широко распространены в приборах ночного видения и системах пожаротушения. Так же дистанционные измерители температуры. Которые находят применение как в технике(автомобильный измеритель температуры антифриза), медицине(измеритель температуры тела) и военной сфере(самонаводящиеся головки тепловых ракет). В электронике кремниево-германиевые сплавы находят применение в высокоскоростных интегральных схемах. Как показала практика микропроцессоры из кремниево-германиевого сплава намного быстрее чем просто кремниевые.
Так же довольно существенный процент применения германия занимают солнечные батареи. Германий обычно выступает подложкой для пластин высокоэффективных многопереходных фотоэлементов.
Интересные факты

Интересных фактов связанных с германием достаточно много. Стоит начать с того, что некоторые соединения германия являются очень реакционноспособными. В связи с этим они могут взаимодействовать со слизистой человека и могут привести даже к смерти.
Так же интересным фактом является то, что в 1948 году был разработан первый транзистор на основе германия. Считается, что этот момент положил начало твердотельной электронике. На сегодняшний день, германий является самым чистым химическим элементом, который людям удалось очистить. Количество примесей в этом образце составила 1 часть на 10 10 . В 2005 году из-за этого открытия германий стал первым в мире сверхпроводником и его применение открыло второе дыхание.
Германий – свойства, особенности элемента и польза для человека
Этот металл наделен аномальными для большинства химических элементов свойствами. Существование германия предсказал великий русский химик Дмитрий Менделеев, а первооткрыватель назвал в честь своей родины.

Что представляет собой
Германий – это химический элемент, занимающий ячейку №32 периодической системы Дмитрия Менделеева.
Выглядит как сероватый металл, но не относится к металлам.
По физическим и химическим свойствам германий не металл, а полуметалл.
Природное вещество по составу – конгломерат одного радиоактивного и четырех стабильных изотопов.
Международное обозначение – Ge, Germanium. Формула простого вещества – Ge.

Как был открыт
Клеменс Александр Винклер — первооткрыватель германия
История элемента начинается с 1871 года, когда Дмитрий Менделеев «вычислил» его и поместил в свою таблицу как экасилиций.
Через 15 лет немецкому химику Клеменсу Винклеру принесли на исследование новый минерал аргиродит из местных рудников.
Первооткрыватель выделил из него неизвестный элемент, описал его свойства.
Планировал назвать свое детище нептунием, но название было занято. Тогда окрестил новичка германием – по названию родной страны.
Присутствие в природе
Вещество рассеяно в массиве литосферы. Не относится к редким: процент содержания больше, чем у серебра, висмута, сурьмы.
Тонна земной коры содержит 1,5 г германия, литр морской воды – 0,0006 мг.
В сфалеритах, энаргитах, пирагидрите содержание измеряется килограммами на тонну, в сульфидах и силикатах – десятками/сотнями грамм.

Сфалерит
Типичные формы нахождения в природе:
- Собственные минералы: аргиродит, германит, реньерит, другие. Они редки, промышленного интереса не представляют.
Промышленные «поставщики» – угли, полиметаллические, железные руды.
Месторождения
Германий найден во всех уголках Земли.
Российские месторождения сосредоточены в Приморье, Забайкалье, на Сахалине.
Добыча сырья – углей с германием в составе – ведется шахтным способом.
Она рентабельна: тонна сырья содержит 190-210 граммов вещества.
Физико-химические характеристики
Германий хрупок, хотя по структуре его кристаллическая решетка аналогична алмазной.

Элементарная кристаллическая ячейка германия типа алмаза
Важнейшая характеристика, имеющая практическое значение, – полупроводниковость. Это самый распространенный на планете натуральный полупроводник.
Твердая форма вещества имеет следующие свойства:
- Устойчивость к газам, воде, кислотам, щелочам.
- Стабильность при комнатной температуре.
- Быстрая окисляемость при 600+°С.
- Растворяется царской водкой, щелочным раствором перекиси водорода.
- Образует органические и неорганические соединения.
- Соединения имеют показатели окисления 2 и 4, устойчивы четырехвалентные формы.
Большинство кислородных соединений вещества структурно аналогичны кремниевым (поэтому Менделеев классифицировал вещество как экасилиций). Более плотные копируют структуру титановых.
| Название, символ, номер | Герма́ний / Germanium (Ge), 32 |
|---|---|
| Группа, период, блок | 14, 4, >> |
| Атомная масса (молярная масса) | 72,630(8) а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d10 4s2 4p2 |
| Радиус атома | 122,5 пм |
| Химические свойства | |
| Ковалентный радиус | 122 пм |
| Радиус иона | (+4e) 53 (+2e) 73 пм |
| Электроотрицательность | 2,01 (шкала Полинга) |
| Электродный потенциал | 0 |
| Степени окисления | -4; -2; -3; -2; -1; 0; +2; +3; +4 |
| Энергия ионизации | 1‑я: 761,2 (7,89) кДж/моль (эВ) 2‑я: 1537,0 (15,93) кДж/моль (эВ)3‑я: 3301,2 (34,21) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 5,323 г/см³ |
| Температура плавления | 1210,6 K |
| Температура кипения | 3103 K |
| Уд. теплота плавления | 36,8 кДж/моль |
| Уд. теплота испарения | 328 кДж/моль |
| Молярная теплоёмкость | 23,32 Дж/(K·моль) |
| Молярный объём | 13,6 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | алмазная |
| Параметры решётки | 5,660 Å |
| Температура Дебая | 360 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 60,2 Вт/(м·К) |
| Номер CAS | 7440-56-4 |
Германий наделен аномальным свойством не разжижаться, а уплотняться при плавлении.
По этой характеристике его легко отличить от большинства элементов. Но не от галлия, плутония, кремния, церия, висмута, сурьмы, воды. Они ведут себя так же.
Технология получения
Почти весь материал добывают из углей, обогащенного сфалеритового, магнетитового сырья.
Способ получения многоступенчат:
- Вещество извлекается выщелачиванием, возгонкой, сплавлением с едким натром.
- На раскаленный концентрат воздействуют соляной кислотой.
- Конденсат очищается, разлагается методом гидролиза.
- Полученный диоксид восстанавливается до металлической формы водородом.
При производстве чистого металла применяют кристаллизацию и плавку.
Где используется
Традиционные сферы применения вещества – радиоэлектроника и электротехника. Из него делали диоды и транзисторы. Сегодня такие приборы – добыча коллекционеров, поскольку германий вытеснен в этом сегменте кремнием. Однако нашел применение в устройствах, работающих на сверхвысоких частотах (СВЧ).

Пример инфракрасной линзы из германия
Ассортимент продукции из полуметалла:
- Анализаторы рентгенспектроскопии.
- Дозиметры на ядерных объектах.
- Преобразователи ядерной энергии в электричество (на АЭС).
- Теллурид вещества – термоэлектрический материал.
- Сплавы с металлами – исходник для металлургии, машино-, приборостроения.
- Сплав с галлием востребован как сверхпроводник.
Главные сферы потребления германия в новом тысячелетии (%): волоконная оптика – 34, тепловизоры – 31, электроника, химический катализ – по 15. Остаток забирают металлурги.
Стратегическое значение имеет сверхчистый металлический германий как сырье при производстве оптики, работающей в инфракрасном диапазоне (линзы, тепловизоры, гаджеты ночного видения, системы наведения).
Достоинства вещества оценили ювелиры. Микродобавка германия делает внешний слой серебряного изделия (пробы 935 и 960) прозрачным, но стойким.
Биологическое воздействие
Промышленность начала использование германия в середине 1940-х годов. Через 30 лет очередь дошла до целебного потенциала.
Этим занялись японцы. Прорыв произошел в 1967 году, когда доктор Казухико Асаи обнародовал список лечебных возможностей германия:
- Подавление онкологии.
- Повышение сопротивляемости к бактериям, вирусам, нейтрализация токсинов.
- Транспортировка кислорода тканям организма (подобно гемоглобину).
- Повышение порога восприимчивости нервных импульсов.
Команда доктора Асаи нашла германий в традиционных для Востока продуктах и лекарственных растениях. Веществом оказались насыщены трубчатые грибы, женьшень, бамбук, хлорелла. А также привычные для европейцев алоэ, чайный лист, чеснок.
Германием богат чеснок. Повышенным употреблением этого продукта в странах Азии объясняют редкость онкологии у местных жителей.
Официальная медицина элемент не использует.
Главный недостаток вещества – токсичность. Более токсичны двухвалентные соединения. Значение также имеет дозировка: превышение делает вещество опасным.
По стандартам РФ, кубометр воздуха не должен содержать более 2 мг германия либо его оксида.
Стоимость
Цена германия на мировом рынке определяется видом материала ($/ кг): двуокись – 860, металлический – 1250.
Германий
Германий – химический элемент, открытие которого обеспечило прорыв технического прогресса. Германиевые полупроводники в транзисторах и другой радио- и аудиоаппаратуре, практически заменили лампы накаливания. В настоящее время ученые продолжают исследовать германий, открывая новые области его применения.

Описание элемента
Вещество относится к стабильным полуметаллам, имеет серо-белый цвет, реже серебристый или черный, с металлическим блеском. Относится к природным полупроводниковым элементам, по своим действиям уступает кремнию и алмазу.
В современной версии периодической системы материал находится в 14 группе 4 периода (в первичной таблице занимал место в четвертой группе главной подгруппы), имеет порядковый атомный номер 32. Обозначается символом Ge (лат.Germanium), формула простого вещества — Ge.
В таблице ниже можно увидеть некоторые характеристики.
| Характеристики германия: | |
|---|---|
| Основные физические характеристики элемента | Показатели |
| Атомная (молярная) масса | 72,630 (г/моль) |
| Распределение электронов по уровням | 3d10 4s2 4p2 |
| Радиус атома | 122,5 пм |
| Электроотрицательность | 2,01 по шкале Полинга |
| Электронный потенциал | 0 |
| Степень окисления | 4,2 |
| Энергия ионизации | 760,0 (7,88) кДж/моль (эВ) |
| Структура решетки | Алмазная, кубическая |
| Параметры решетки | 5,660 Å |
| Основные характеристики элемента | Показатели |
| Номер CAS | 7440-56-4 |
| Точка плавления | 1210,6 K |
| Точка кипения | 3103 K |
| Удельная теплота плавления | 36,8 кДж/моль |
| Удельная теплота кипения | 328 кДж/моль |
| Температура Дебая | 360 K |
| Теплопроводность | (300 K) 60,2 Вт/(м·К) |
| Плотность | 5,323 г/см³ |
| Молярная теплоемкость | 23,32 Дж/(K·моль) в растворе |
| Молярный объем | 13,6 см³/моль |
История открытия элемента
В 1869 году на заседании Русского химического общества был представлен анализ Д.И. Менделеева, в котором ученый объяснял связь ионов и атомной массы элемента с его свойствами. Параллельно он выдвинул гипотезу о существовании некоторых химических элементов.
В 1870 году в научной статье Менделеев выдвинул предположение о том, какое место в системе будут занимать пока неизвестные науке вещества. Одно из них он назвал экасилицием, поскольку оно должно было находиться за кремнием и обладать схожими свойствами. Менделеев предсказал свойства экасилиции и атомную массу.
Спустя 15 лет в 1885 году в одной из шахт Саксонии нашли органический минерал, названный аргиродитом и имевший неизвестный состав. Провести анализ материала поручили химику Клеменсу Винклеру, который обнаружил, что он практически полностью (на 93%) состоит из серебра. А остальные 7% составляет вещество неизвестного происхождения.
Путем долгих опытов элемент удалось выделить из минерала и изучить. Это оказался металл, схожий по свойствам с сурьмой. В серии научных статей 1886-1887 года химик подробно описывает выделенное вещество, его свойства. В честь своей родины, ученый предложил дать ему название германий (Germanium) и обозначить знаком Ge. Много лет единственным соединением был тетраэтилгерманий.
Многие ученые были возмущены таким поворотом и обвинили Винклера в краже чужого научного достижения, считая, что Д.И. Менделеев уже дал название новому веществу. Для снятия спорного вопроса ученый обратился к «отцу» периодической системы, подробно изложив в обращении суть вопроса. Ответ от Менделеева пришел незамедлительно. Он разъяснил, что название новому органическому веществу может дать его первооткрыватель.
Поскольку Дмитрий Иванович только предсказал его существование и никакого отношения к открытию не имеет, то Винклер имеет право назвать вещество так, как считает нужным. Великие химики расстались друзьями, а экасилиций стал германием, заняв законную позицию в периодической системе химических элементов. Сегодня многие соединения германия, в том числе и тетраэтилгерман, активно применяются в промышленности.
Физико-химические свойства германия
Природный германий состоит из 5 изотопов (4 – стабильных, без полураспада на воздухе и 1 с периодом полураспада 1,78*10 21 ). Несмотря на то, что кубическая решетка 32 элемента имеет сходство с алмазной, это довольно хрупкое вещество.

По своим физико-химическим свойствам полупроводниковый германий, который встречается в природе, имеет сходство с кремнием, что и предполагал Д.И. Менделеев, справедливо поместив их в одну группу. Оба эти вещества могут образовывать растворы с валентностью 2 и 4. У них обнаружились и другие общие физические и химические свойства.
- высокий показатель преломления;
- в реакцию с кислотами вступают только при нагревании;
- в присутствии окислителей взаимодействуют со щелочным раствором (двуокись);
- не активны с водой, азотом, углеродом, водородом;
- водяные пары не вызывают изменений в их структуре;
- щелочной германий воспламеняется при температуре выше 700°C, горит с выделением диоксида;
- ионы вступают в реакцию с галогенами, сульфосолями, хромитами;
- активно взаимодействует с серой, сурьмой, хромом, образуют сульфосоли (GeS), хромиты;
- сульфид германия плохо растворим в воде.
Внешне германий выглядит как твердое вещество бело-серого цвета с ярким металлическим блеском. По минералогической 10 бальной шкале твердости имеет показатель 6,25 при 20°C. При таких условиях он очень хрупкий и легко разбивается, поэтому при низких температурах обработка его невозможна.
При высоких температурах 32 элемент, как и уголь, легко поддается обработке. Так, при 500°C он становится пластичным, а при 600°C можно изменять его форму. Температура плавления 958,5°C, а закипает он при 2700°C. На воздухе расширяется при охлаждении, а при нагревании сжимается. Плотность в твердом состоянии 5,3 г/моль, в жидком виде (двуокись) – 5,5 г/моль.
Являясь типичным полупроводником, германий встречается в чистом виде и имеет высокое удельное электросопротивление, высокую валентность при комнатной температуре.
Это свойство сильнее проявляется при нагреве. Это отличает его от простых проводников, которые теряют это свойство при повышении температуры. А вот наличие посторонних веществ в составе полупроводника значительно снижает сопротивление. Например, у сульфида (GeS).
Добыча и получение германия
Месторождения вещества в природе рассеяны. Его содержание во много раз превышает количество серебра, магнетита, алмазов, висмута, угля или сурьмы.

Общий объем, содержащегося в недрах германия составляет 1000 тонн, основной его объем находится на территории США и Китая, и они являются крупными поставщиками этого элемента в другие страны. В России месторождения германита сосредоточены в Приморье, Забайкалье, на Сахалине.
В полиметаллических рудах и силикатах он обычно присутствует в качестве примеси. Изотопы внедряются в кристаллическую решетку, и места занимает немного. Пример: в сфалеритах германия содержится несколько килограмм на тонну породы, в энаргитах его 5 кило на тонну, а в сульванитах на этот же объем приходиться всего 1 кг. В германите количество главного элемента достигает 10%.
Получение вещества ведут чаще из железных, кремниевых, цветных руд в качестве дополнительного продукта методом обогащения. Полученный при этом GeO2 (оксид IV) доводят до простого вещества, восстанавливая его водородом.
В России впервые добывать германий и магнетит начали в 1959 году. Тогда на медно-серном комбинате Медногорска, в цехе по переработке пыли, открыли новую технологию, которая позволяла добывать концентрат вещества в результате переработки пыли и золы, оставшихся после медеплавильного процесса. После открытия этого способа германий для страны за границей больше не закупался.
Области применения германия
После того, как производство поставили на промышленные рельсы, его стали широко применять как полупроводник в электронике. Но дороговизна вещества заставила отказаться от использования его в транзисторах и полупроводники стали делать из более дешевых кремниевых руд.

До 1930 года германий не использовался в промышленности. Это не уменьшило уникальных свойств элемента, и он нашел «занятие» в других сферах.
Кроме этих сфер германий используют в анализаторах рентгенографов и дозиметрах на ядерных объектах в качестве диодов. В сплавах с металлами германий органические вещества используются в приборостроении, а в соединении с галлием – как сверхпроводник.
Биологическое воздействие на человека
Через 30 лет после открытия германия, японские ученые занялись исследованиями в области его действия в медицине. В 1967 году ими были впервые обнародованы результаты работы. Применение этого вещества показало хорошие результаты в лечении онкологии, вирусных и бактериальных инфекций.

Германий повышает порог восприимчивости нервных импульсов, что позволяет применять его при лечении неврологических заболеваний.
В гематологии препараты с содержанием 32 элемента используют как заменитель гемоглобина благодаря его свойствам рассеивания кислорода по крови к тканям.
Элемент нашли в составе большинства популярных лекарственных растений, которые используют в народной медицине и повседневной жизни. Так, содержанием рекордного количества этого элемента может похвастаться чеснок, бамбук, грибы, женьшень, зеленый чай, алоэ.
По версии японских ученых, именно регулярным употреблением в пищу данных растений жителями Азии объясняются низкие показатели заболеваемости онкологией.
Также его обнаружили в животных организмах. Его воздействие на человеческий организм в малых количествах не ведет к побочным эффектам, но в большом количестве это довольно токсичное вещество. Устойчивыми к токсическому воздействию 32 элемента оказались плесневые грибы и большинство животных.
Цена вещества
Для производства оптоволокна, ценных сплавов, диодов, спектрометров необходима монокристаллическая форма вещества. Его закупают в больших объемах, что довольно выгодно. Тонна монокристаллического германия стоит 100 тысяч рублей, хотя на внешнем рынке можно найти предложения с более низкой ценой (75-85 тыс.р.).
А вот поликристаллическая форма 32 элемента оценивается гораздо дороже. Это связано с тем, что поликристаллы германия имеют меньший размер, повышенную прочность и являются основой для выращивания монокристаллов. Цена на 1 кг поликристаллического вещества варьирует в пределах 160-250 тыс. рублей.
Также 32 элемент реализуется в слитках стандартного размера 28 см. Их стоимость рассчитывается 150 рублей за 10 гр. веса.

В моём личном блоге я познакомлю вас с особенностями разных драгоценных камней, влиянием зодиакальных камней в отношении каждого знака зодиака, а также целебными свойствами некоторых из них.

Германий — химический элемент 14-й группы (по устаревшей классификации — главной подгруппы четвёртой группы) 4-го периода периодической системы химических элементов, с атомным номером 32. Обозначается символом Ge (нем. Germanium ). Простое вещество германий — типичный полуметалл серо-белого цвета, с металлическим блеском. Подобно кремнию, является полупроводником.
Содержание
- 1 История открытия и этимология
- 2 Нахождение в природе
- 3 Получение
- 3.1 Промышленное производство германия в России
- 4.1 Изотопы
- 5.1 Соединения германия
- 5.1.1 Неорганические
- 5.1.2 Органические
- 6.1 Оптика
- 6.2 Радиоэлектроника
- 6.3 Прочие применения
- 7.1 Цены
![Германий]()
История открытия и этимология
![Германий]()
![Германий]()
В своём докладе о периодическом законе химических элементов в 1869 году русский химик Дмитрий Иванович Менделеев предсказал существование нескольких неизвестных на то время химических элементов, в частности и германия. В статье, датированной 11 декабря (29 ноября по старому стилю) 1870 года, Д. И. Менделеев назвал неоткрытый элемент экасилицием (из-за его местонахождения в Периодической таблице) и предсказал его атомную массу и другие свойства.
В 1885 году в Фрайберге (Саксония) в одной из шахт был обнаружен новый минерал аргиродит. При химическом анализе нового минерала немецкий химик Клеменс Винклер обнаружил новый химический элемент. Учёному удалось в 1886 году выделить этот элемент, также химиком была отмечена схожесть германия с сурьмой. Об открытии нового элемента Винклер сообщил в двухстраничной статье, датируемой 6 февраля 1886 года и предложил в ней имя для нового элемента Germanium и символ Ge. В последующих двух больших статьях 1886—1887 гг. Винклер подробно описал свойства германия.
Первоначально Винклер хотел назвать новый элемент «нептунием», но это название было дано одному из предполагаемых элементов, поэтому элемент получил название в честь родины учёного — Германии.
Путём анализа тетрахлорида германия GeCl4 Винклер определил атомный вес германия, а также открыл несколько новых соединений этого металла.
До конца 1930-х годов германий не использовался в промышленности. Во время Второй мировой войны германий использовался в некоторых электронных устройствах, главным образом в диодах.
Нахождение в природе
Общее содержание германия в земной коре 1,5⋅10 −4 % по массе, то есть больше, чем, например, сурьмы, серебра, висмута. Германий вследствие незначительного содержания в земной коре и геохимического сродства с некоторыми широко распространёнными элементами обнаруживает ограниченную способность к образованию собственных минералов, внедряясь в кристаллические решётки других минералов. Поэтому собственные минералы германия встречаются исключительно редко. Почти все они представляют собой сульфосоли: германит Cu2(Cu, Fe, Ge, Zn)2 (S, As)4 (6—10 % Ge), аргиродит Ag8GeS6 (3,6—7 % Ge), конфильдит Ag8(Sn, Ge) S6 (до 2 % Ge) и др. редкие минералы (ультрабазит, ранерит, франкеит). Основная масса германия рассеяна в земной коре в большом числе горных пород и минералов. Так, например, в некоторых сфалеритах содержание германия достигает килограммов на тонну, в энаргитах до 5 кг/т, в пираргирите до 10 кг/т, в сульваните и франкеите 1 кг/т, в других сульфидах и силикатах — сотни и десятки г/т. Германий концентрируется в месторождениях многих металлов — в сульфидных рудах цветных металлов, в железных рудах, в некоторых окисных минералах (хромите, магнетите, рутиле и др.), в гранитах, диабазах и базальтах. Кроме того, германий присутствует почти во всех силикатах, в некоторых месторождениях каменного угля и нефти. Концентрация германия в морской воде 6⋅10 −5 мг/л.
Получение
Германий встречается в виде примеси к полиметаллическим, никелевым, вольфрамовым рудам, а также в силикатах. В результате сложных и трудоёмких операций по обогащению руды и её концентрированию германий выделяют в виде оксида GeO2, который восстанавливают водородом при 600 °C до простого вещества:
Получение чистого германия происходит методом зонной плавки, что делает его одним из самых химически чистых материалов.
Промышленное производство германия в России
![Германий]()
Производство германия в промышленных масштабах в России началось в 1959 году, когда на Медногорском медно-серном комбинате (ММСК) был введён в действие цех переработки пыли. Специалисты комбината под руководством А. А. Бурбы в сотрудничестве с проектным институтом «Унипромедь» разработали и внедрили в производство уникальную химико-металлургическую технологию получения германиевого концентрата путём комплексной переработки пылей шахтных металлургических печей медеплавильного производства и золы от сжигания энергетических углей, служивших топливом для электростанции. После этого СССР смог полностью отказаться от импорта германия. Впервые в мировой практике было выполнено извлечение германия из медноколчеданных руд. Пуск промышленного цеха переработки пыли на ММСК относят к крупнейшим внедрениям в цветной металлургии XX века.
В 1962 году по инициативе и при участии А. А. Бурбы аналогичное производство было создано также на Ангренском химико-металлургическом заводе (АХМЗ) в городе Ангрен в Узбекистане (ныне предприятие «Ангренэнергоцветмет»). Практически весь объём производства концентрата германия в СССР приходился на ММСК и АХМЗ. Создание крупномасштабного производства германия внесло значительный вклад в обеспечение экономической и оборонной безопасности страны. Уже в 1960-е годы Советский Союз смог отказаться от импорта германия, а в 1970-е начать его экспорт и стать мировым лидером по производству германия.
Для переработки выпускавшегося на ММСК и АХМЗ германиевого концентрата в конечные продукты (чистый германий и его соединения) в 1961—1962 гг. на Красноярском аффинажном заводе (с 1967 г. — Красноярский завод цветных металлов, затем — ОАО «Красцветмет») был создан цех по производству германия (с 1991 г. — ОАО «Германий»). В 1962—1963 гг. цех производил 600 кг монокристаллического германия в год. В 1968—1969 гг., когда внутренние потребности в германии были обеспечены, СССР впервые начал экспортировать диоксид германия, а в 1970 г. начался также экспорт поликристаллического зонноочищенного германия. СССР удерживал мировое лидерство по производству германия, увеличив выпуск металла настолько, что до 40 % производства уходило на экспорт. После распада СССР, вплоть до 2010 г., ММСК оставался единственным производителем германиевого концентрата в России. С 2010 г. производство германия в концентрате на ММСК приостановлено, а оборудование законсервировано. Одновременно с этим начато производство германия в концентрате на ООО «Германий и приложения» в г. Новомосковске Тульской области.
В 2000-х годах для получения германия в России используются германиеносные угли следующих месторождений: Павловское (Михайловский район Приморского края), Новиковское (Корсаковский городской округ Сахалинской области), Тарбагатайское (Петровск-Забайкальский район Забайкальского края). Германиеносные угли этих месторождений в среднем содержат 200 граммов германия на тонну.
Физические свойства
![Германий]()
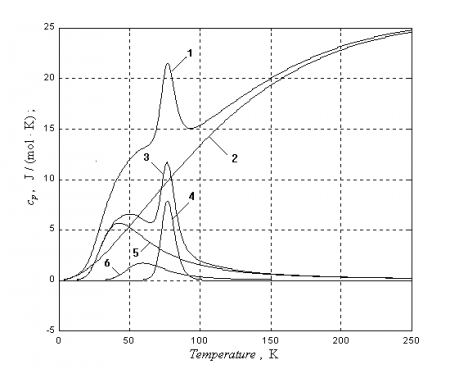
Аномальный пик на кривой теплоёмкости германия: 1 — экспериментальная кривая; 2 — дебаевская (колебательная) составляющая; 3 — аномальный остаток (разность кривой 1 и 2); 4,5,6 — больцмановские составляющие аномального остатка 3.
Германий — хрупкий, серебристо-белый полуметалл. Кристаллическая решётка устойчивой при нормальных условиях аллотропной модификации — кубическая типа алмаза.
Температура плавления 938,25 °C, температура кипения 2850 °C, плотность германия 5,33 г/см 3 .
Теплоёмкость германия имеет аномальный вид, а именно, содержит пик над уровнем нормальной (колебательной) составляющей, который, как пишет Ф.Зейтц : «не может быть объяснён никакой теорией, предполагающей гуковский закон сил, ибо никакая суперпозиция эйнштейновских функций не даёт кривой с максимумом» и объясняется, как и аномальность поведения теплоёмкостей гафния, алмаза и графита, больцмановским фактором, контролирующим диффузионную (диссоциационную) компоненту.
Германий является одним из немногих аномальных веществ, которые увеличивают плотность при плавлении. Плотность твёрдого германия 5,327 г/см 3 (25 °С), жидкого — 5,557 г/см 3 (1000 °С). Другие вещества, обладающие этим свойством — вода, кремний, галлий, сурьма, висмут, церий, плутоний.
Германий по электрофизическим свойствам является непрямозонным полупроводником.
- Статическая диэлектрическая проницаемость ε = 16,0
- Ширина запрещённой зоны (при 300 К) Eg = 0,67 эВ
- Собственная концентрация ni=2,33⋅10 13 см −3
- Эффективная масса:
- электронов, продольная: mII=1,58m0, mII=1,64m0
- электронов, поперечная: m┴=0,0815m0 , m┴=0,082m0
- дырок, тяжелых: mhh=0,379m0
- дырок, легких: mhl=0,042m0
Легированный галлием германий в виде тонкой плёнки переходит при низких температурах в сверхпроводящее состояние.
Изотопы
Природный германий состоит из смеси пяти изотопов: 70 Ge (20,55 % ат.), 72 Ge (27,37 %), 73 Ge (7,67 %), 74 Ge (36,74 %), 76 Ge (7,67 %).
Первые четыре изотопа стабильны, пятый ( 76 Ge) весьма слабо радиоактивен и испытывает двойной бета-распад с периодом полураспада 1,58⋅10 21 лет.
Искусственно получено 27 радиоизотопов с атомными массами от 58 до 89. Наиболее стабильным из радиоизотопов является 68 Ge, с периодом полураспада 270,95 суток. А наименее стабильным — 60 Ge, с периодом полураспада 30 мс.
Химические свойства
В химических соединениях германий обычно проявляет валентности 4 или 2. Соединения с валентностью 4 стабильнее. При нормальных условиях устойчив к действию воздуха и воды, щелочей и кислот, растворим в царской водке и в щелочном растворе перекиси водорода.
Соединения германия
Неорганические
- Гидриды
- Гермилен GeH2
- Герман GeH4
- Дигерман Ge2H6
- Тригерман Ge3H8
- Оксид германия (II) GeO
- Оксид германия (IV) GeO2
- Гидроксид германия (II) Ge(OH)2
- Гидроксид германия (IV) Ge(OH)4
- Метагидроксид германия (IV) GeO(OH)2
- Галогениды
- Бромид германия (IV) GeBr4
- Йодид германия (II) GeI2
- Йодид германия (IV) GeI4
- Фторид германия (IV) GeF4
- Хлорид германия (IV) GeCl4
Органические
Германийорганические соединения — металлоорганические соединения содержащие связь «германий-углерод». Иногда ими называются любые органические соединения, содержащие германий.
Первое германоорганическое соединение — тетраэтилгерман, было синтезировано немецким химиком Клеменсом Винклером (нем. Clemens Winkler ) в 1887 году
Применение
В 2007 году основными потребителями германия были: 35 % волоконная оптика; 30 % тепловизорная оптика; 15 % химические катализаторы; 15 % электроника; небольшие количества германия потребляет металлургия.
Оптика
![Германий]()
![Германий]()
- Благодаря прозрачности в инфракрасной области спектра металлический германий сверхвысокой чистоты имеет стратегическое значение в производстве оптических элементов инфракрасной оптики: линз, призм, оптических окон датчиков. Наиболее важная область применения — оптика тепловизионных камер, работающих в диапазоне длин волн от 8 до 14 микрон. Это диапазон для наиболее популярных инфракрасных матриц на микроболометрах используемых в системах пассивного тепловидения, военных системах инфракрасного наведения, приборах ночного видения, противопожарных системах. Германий также используется в ИК-спектроскопии в оптических приборах, использующих высокочувствительные ИК-датчики. Германий проигрывает по пропускающей способности света в диапазоне от 8 до 14 микрон сульфиду цинка. Однако германий в отличие от сульфида цинка продолжает пропускать порядка 25 % инфракрасного излучения до длины волны 23 микрона, поэтому является одним из основных материалов для длинноволновой инфракрасной оптики, обычно используемой в военных прицелах.
- Оптические детали из Ge обладают очень высоким показателем преломления (4,0) и обязательно требует использования просветляющих покрытий. В частности, используется покрытие из очень твердого алмазоподобного углерода, с показателем преломления 2,0.
- Наиболее заметные физические характеристики оксида германия (GeO2) — его высокий показатель преломления и низкая оптическая дисперсия. Эти свойства находят применение в изготовлении широкоугольных объективов камер, микроскопии, и производстве оптического волокна.
- Тетрахлорид германия используется в производстве оптоволокна, так как образующийся в процессе разложения этого соединения диоксид германия удобен для данного применения благодаря своему высокому показателю преломления и низкому оптическому рассеиванию и поглощению.
- Сплав GeSbTe используется при производстве перезаписываемых DVD. Сущность перезаписи заключается в изменении оптических свойств этого соединения при фазовом переходе под действием лазерного излучения.
Радиоэлектроника
- До 1970-х годов германий был основным полупроводниковым материалом электронной промышленности и широко использовался в производстве транзисторов и диодов. Впоследствии германий был полностью вытеснен кремнием. Германиевые транзисторы и диоды обладают характеристиками, отличными от кремниевых, ввиду меньшего напряжения отпирания p-n-перехода в германии — 0,35…0,4 В против 0,6…0,7 В у кремниевых приборов. Кроме того, обратные токи у германиевых приборов имеют сильную зависимость от температуры, и на несколько порядков больше таковых у кремниевых — скажем, в одинаковых условиях кремниевый диод будет иметь обратный ток 10 пА, а германиевый — 100 нА, что в 10000 раз больше. Также у германиевых приборов значительно выше шум и ниже температура, при которой происходит разрушение p-n-переходов. По советскому ГОСТ 10862-64 (1964 г.) и более поздним стандартам германиевые полупроводниковые приборы имеют обозначение, начинающиеся с буквы Г или цифры 1, например: ГТ313, 1Т308 — высокочастотные маломощные транзисторы, ГД507 — импульсный диод. До того транзисторы имели индексы, начинающиеся с букв С, Т или П (МП), а диоды — Д, и определить материал прибора по индексу было сложнее. Диоды и транзисторы с индексами меньше 100, были германиевыми, от 100 до 199, — кремниевыми. Далее индексы зависели от частоты и мощности, причём, у транзисторов и диодов правила отличались. До конца 1960-х гг. германиевые полупроводниковые приборы использовались повсеместно, в настоящее время германиевые диоды и транзисторы практически полностью вытеснены кремниевыми, как имеющими значительно лучшие эксплуатационные характеристики.
- Сейчас в электронике германий используется в СВЧ-устройствах, как составная часть структур SiGe, позволяя достичь субтерагерцовых частот. Работы Жореса Алфёрова по структурам SiGe, в частности, заложили основу этого направления.
- Теллурид германия применяется как стабильный термоэлектрический материал и компонент термоэлектрических сплавов (термо-ЭДС 50 мкВ/К).
Прочие применения
- Германий широко применяется в ядерной физике в качестве материала для детекторов гамма-излучения.
- В ювелирном сплаве Argentium® (серебро пробы 935 либо 960) германий является легирующим элементом, обеспечивающим формирование прозрачного и стойкого защитного оксидного слоя на поверхности изделий.
Экономика
Год Цена
($/кг)1999 1 400 2000 1 250 2001 890 2002 620 2003 380 2004 600 2005 660 2006 880 2007 1 240 2008 1 490 2009 950 Средние цены на германий в 2007 году
- Германий металлический $1200/кг
- Германия диоксид $840/кг
Биологическая роль
Германий обнаружен в животных и растительных организмах. Малые количества германия не оказывают физиологического действия на растения, но токсичны в больших количествах. Германий нетоксичен для плесневых грибков.
Для животных германий малотоксичен. У соединений германия не обнаружено фармакологическое действие. Допустимая концентрация германия и его оксида в воздухе — 2 мг/м³, то есть такая же, как и для асбестовой пыли.
Соединения двухвалентного германия значительно более токсичны.
Eu, Sm, Li, Cs, Rb, K, Ra, Ba, Sr, Ca, Na, Ac, La, Ce, Pr, Nd, Pm, Gd, Tb, Mg, Y, Dy, Am, Ho, Er, Tm, Lu, Sc, Pu,
Th, Np, U, Hf, Be, Al, Ti, Zr, Yb, Mn, V, Nb, Pa, Cr, Zn, Ga, Fe, Cd, In, Tl, Co, Ni, Te, Mo, Sn, Pb, H2,
W, Sb, Bi, Ge, Re, Cu, Tc, Te, Rh, Po, Hg, Ag, Pd, Os, Ir, Pt, AuЧитайте также: