Дописать определение металлами называют химически простые вещества
В уроке 3 «Молекулы и простые вещества» из курса «Химия для чайников» рассмотрим, что такое молекулы, простые вещества, а также металлы и неметаллы. Напоминаю, что в прошлом уроке «Относительная атомная масса химических элементов» мы рассмотрели разные способы выражения массы химических элементов.

Атомы химических элементов существуют в природе как в свободном, так и в связанном состоянии. Например, благородные газы — гелий He, неон Ne, аргон Ar, криптон Kr, ксенон Xe — находятся в воздухе в виде одиночных атомов. Атомы всех остальных элементов в природе не существуют изолированно друг от друга. Они всегда стремятся соединиться, связаться с другими атомами за счет особых сил. Почему? Так они достигают более устойчивого состояния. Это одна из иллюстраций всеобщего принципа природы — стремления к максимально устойчивому состоянию.
Что такое молекула?
Из курса физики вы уже немного знаете о молекулах — частицах вещества, состоящих обычно из двух и более атомов. Что же такое молекула?
Молекула — наименьшая частица вещества, способная существовать самостоятельно и сохраняющая его химические свойства.
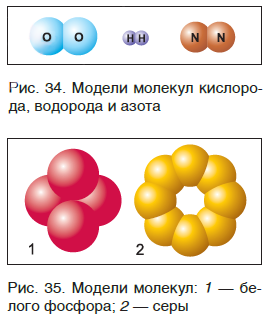
Молекулы благородных газов одноатомны, а молекулы таких веществ, как кислород, водород, азот, хлор, бром, состоят из двух атомов (рис. 34). Молекула фосфора содержит четыре атома, а серы — восемь (рис. 35).
Простые вещества
Если вещества состоят из атомов одного вида, то они относятся к простым веществам.
Простыми называются вещества, которые образованы атомами одного химического элемента.
Простые вещества — одна из форм существования химических элементов в природе. Простые вещества, состоящие из молекул, относятся к веществам молекулярного строения. При обычных условиях среди них есть газы (водород, кислород, азот, фтор, хлор, благородные газы), жидкости (бром) и твердые вещества (сера, иод, фосфор).
Элемент кислород существует в виде двух простых веществ молекулярного строения: одно из них (просто кислород) состоит из двухатомных молекул, а второе (озон) — из трехатомных.
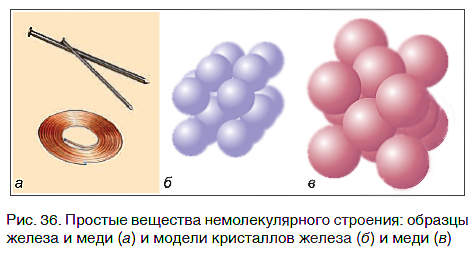
Связываясь друг с другом, атомы образуют не только молекулы. Гораздо больше простых веществ, которые имеют немолекулярное строение. Они обычно представляют собой твердые кристаллические вещества, построенные из атомов, например кристаллы алмаза, графита, меди, железа (рис. 36).
Металлы и неметаллы
Простые вещества по их свойствам делят на металлы и неметаллы.
Все металлы при комнатной температуре являются твердыми веществами (за исключением ртути), которые проводят электрический ток и теплоту, имеют характерный металлический блеск. Многие из металлов пластичны, т. е. меняют свою форму при механическом воздействии. Благодаря этому свойству металлы можно ковать, расплющивать, вытягивать в проволоку.
Большинство простых веществ — металлы, и все они имеют немолекулярное строение.

Хотя простых веществ неметаллов гораздо меньше, по своим свойствам они различаются между собой значительно сильнее, чем металлы. Почти все они плохо проводят электрический ток и теплоту. Многие из неметаллов при обычных условиях являются хрупкими твердыми веществами (рис. 37), другие — газами (рис. 38), а бром — жидкостью (рис. 39). Большинство неметаллов существует в виде молекул, но некоторые имеют немолекулярное строение, например бор, углерод, кремний.
Алмаз и графит — это простые вещества, состоящие из атомов одного и того же химического элемента — углерода. Хотя они оба имеют немолекулярное строение, свойства этих веществ сильно отличаются: алмаз — прозрачное, самое твердое в природе вещество, а графит — темно-серое, непрозрачное, мягкое вещество (рис. 40). Их свойства различны потому, что различно строение их кристаллов, хотя состоят эти кристаллы из одних и тех же атомов — атомов углерода.

Названия простых веществ
В настоящее время известно более 400 простых веществ, хотя элементов пока открыто только 118. Названия большинства простых веществ такие же, как и названия соответствующих химических элементов. Только у элемента углерода простые вещества (как вы уже знаете) имеют собственные названия, да еще у элемента кислорода есть простое вещество озон.
Необходимо различать понятия простое вещество и химический элемент, поскольку в большинстве случаев их названия совпадают.
Химический элемент — это определенный вид атомов. Поэтому название химического элемента — это то, что объединяет атомы данного вида. У всех таких атомов есть общие черты. Каждый химический элемент обозначается с помощью соответствующего химического знака.
В то же время понятие простое вещество обозначает конкретное химическое вещество, образованное атомами одного вида. Оно характеризуется определенными составом, строением, физическими и химическими свойствами.
Например, если говорят о том, что в состав какого-то вещества входит азот, то имеют в виду атомы этого химического элемента, а когда говорят об азоте, который входит в состав воздуха, то, конечно, речь идет о простом веществе.
Более подробно о различии понятий «простое вещество» и «химический элемент» вы узнаете в главах 2, 3.
Краткие выводы урока:
- Молекула — наименьшая частица вещества, способная существовать самостоятельно и сохраняющая его химические свойства.
- Простые вещества состоят из атомов одного химического элемента.
- Простые вещества имеют молекулярное или немолекулярное строение.
- Простые вещества делят на металлы и неметаллы.
Надеюсь урок 3 «Молекулы и простые вещества» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Урок 8. Общие свойства металлов

Известно, что все простые вещества условно можно разделить на простые вещества-металлы и простые вещества-неметаллы.
МЕТАЛЛЫ, по определению М. В. Ломоносова — это «светлые тела, которые ковать можно». Обычно это ковкие блестящие материалы, обладающие высокой тепло- и электропроводностью. Эти физические и многие химические свойства металлов связаны со способностью их атомов ОТДАВАТЬ электроны.
НЕМЕТАЛЛЫ, напротив, способны ПРИСОЕДИНЯТЬ электроны в химических процессах. Большинство неметаллов проявляют противоположные металлам свойства: не блестят, не проводят электрический ток, не куются. Являясь противоположными по свойствам, металлы и неметаллы легко реагируют друг с другом.
Эта часть Самоучителя посвящена краткому освещению свойств металлов и неметаллов. Описывая свойства элементов, желательно придерживаться следующей логической схемы:
1. Вначале описать строение атома (указать распределение валентных электронов), сделать вывод о принадлежности данного элемента к металлам или неметаллам, определить его валентные состояния (степени окисления) — см. урок 3;
2. Затем описать свойства простого вещества, составив уравнения реакций
- с кислородом;
- с водородом;
- с металлами (для неметаллов) или с неметаллами (для металлов);
- с водой;
- с кислотами или со щелочами (там, где это возможно);
- с растворами солей;
3. Затем нужно описать свойства важнейших соединений (водородных соединений, оксидов, гидроксидов, солей). При этом вначале следует определить характер (кислотный или основной) данного соединения, а затем, вспомнив свойства соединений этого класса, составить необходимые уравнения реакций;
4. И наконец нужно описать качественные реакции на катионы (анионы), содержащие этот элемент, способы получения простого вещества и важнейших соединений этого химического элемента, указать практическое применение изучаемых веществ этого элемента.
Так, если вы определите, что оксид кислотный, то он будет реагировать с водой, основными оксидами, основаниями (см. урок 2.1) и ему будет соответствовать кислотный гидроксид (кислота). При описании свойств этой кислоты также полезно заглядывать в соответствующий раздел: урок 2.2.
Внутреннее строение и физические свойства металлов
Металлы — это простые вещества, атомы которых могут только отдавать электроны. Такая особенность металлов связана с тем, что на внешнем уровне этих атомов мало электронов (чаще всего от 1 до 3) или внешние электроны расположены далеко от ядра. Чем меньше электронов на внешнем уровне атома и чем дальше они расположены от ядра, — тем активнее металл (ярче выражены его металлические свойства).
Задание 8.1. Какой металл активнее:
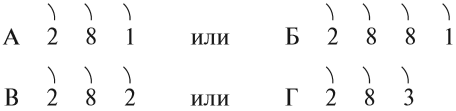
Назовите химические элементы А, Б, В, Г.
Металлы и неметаллы в Периодической системе химических элементов Менделеева (ПСМ) разделяет линия, проведённая от бора к астату. Выше этой линии в главных подгруппах находятся неметаллы (см. урок 3). Остальные химические элементы — металлы.
Задание 8.2. Какие из следующих элементов относятся к металлам: кремний, свинец, сурьма, мышьяк, селен, хром, полоний?
Вопрос. Как можно объяснить тот факт, что кремний — неметалл, а свинец — металл, хотя число внешних электронов у них одинаково?
Существенной особенностью атомов металлов является их большой радиус и наличие слабо связанных с ядром валентных электронов. Для таких атомов величина энергии ионизации* невелика.
* ЭНЕРГИЯ ИОНИЗАЦИИ равна работе, затрачиваемой на удаление одного внешнего электрона из атома (на ионизацию атома), находящегося в основном энергетическом состоянии.
Часть валентных электронов металлов, отрываясь от атомов, становятся «свободными». «Свободные» электроны легко перемещаются между атомами и ионами металлов в кристалле, образуя «электронный газ» (рис. 28).
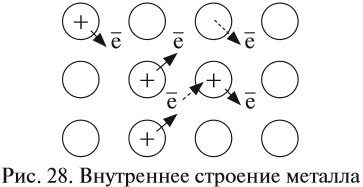
В последующий момент времени любой из «свободных» электронов может притянуться любым катионом, а любой атом металла может отдать электрон и превратиться в ион (эти процессы показаны на рис. 28 пунктирами).
Таким образом, внутреннее строение металла похоже на слоёный пирог, где положительно заряженные «слои» атомов и ионов металла чередуются с электронными «прослойками» и притягиваются к ним. Наилучшей моделью внутреннего строения металла является стопка стеклянных пластинок, смоченных водой: оторвать одну пластинку от другой очень трудно (металлы прочные), а сдвинуть одну пластинку относительно другой очень легко (металлы пластичные) (рис. 29).
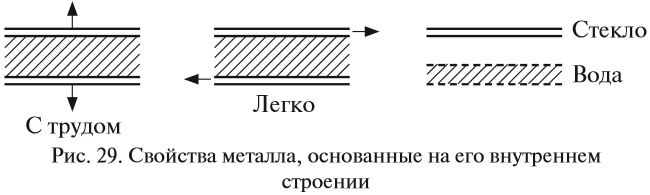
Задание 8.3. Сделайте такую «модель» металла и убедитесь в этих свойствах.
Химическая связь, осуществляемая за счёт «свободных» электронов, называется металлической связью.
«Свободные» электроны обеспечивают также такие физические свойства металлов, как электро- и теплопроводность, пластичность (ковкость), а также металлический блеск.
Задание 8.4. Найдите дома металлические предметы.
Выполняя это задание, вы легко найдёте на кухне металлическую посуду: кастрюли, сковородки, вилки, ложки. Из металлов и их сплавов делают станки, самолёты, автомобили, тепловозы, инструменты. Без металлов невозможна современная цивилизация, так как электрические провода также делают из металлов — Cu и Al. Только металлы годятся для получения антенн для радио- и телеприёмников, из металлов делают и лучшие зеркала. При этом чаще используют не чистые металлы, а их смеси (твёрдые растворы) — СПЛАВЫ.

Сплавы
Металлы легко образуют сплавы — материалы, имеющие металлические свойства и состоящие из двух или большего числа химических элементов (простых веществ), из которых хотя бы один является металлом. Многие металлические сплавы имеют один металл в качестве основы с малыми добавками других компонентов. В принципе, чёткую границу между металлами и сплавами трудно провести, так как даже в самых чистых металлах имеются «следовые» примеси других химических элементов.
Все перечисленные выше предметы — станки, самолёты, автомобили, сковородки, вилки, ложки, ювелирные изделия — делают из сплавов. Металлы-примеси (легирующие компоненты) очень часто изменяют свойства основного металла в лучшую, с точки зрения человека, сторону. Например, и железо и алюминий — довольно мягкие металлы. Но, соединяясь друг с другом или с другими компонентами, они превращаются в сталь, дуралюмин и другие прочные конструкционные материалы. Рассмотрим свойства самых распространённых сплавов.
Сталь — это сплавы железа с углеродом, содержащие последнего до 2 %. В состав легированных сталей входят и другие химические элементы — хром, ванадий, никель. Сталей производится гораздо больше, чем каких-либо других металлов и сплавов, и все виды их возможных применений трудно перечислить. Малоуглеродистая сталь (менее 0,25 % углерода) в больших количествах потребляется в качестве конструкционного материала, а сталь с более высоким содержанием углерода (более 0,55 %) идет на изготовление режущих инструментов: бритвенные лезвия, сверла и др.
Железо составляет основу чугуна. Чугуном называется сплав железа с 2–4 % углерода. Важным компонентом чугуна является также кремний. Из чугуна можно отливать самые разнообразные и очень полезные изделия, например крышки для люков, трубопроводную арматуру, блоки цилиндров двигателей и др.
Бронза — сплав меди, обычно с оловом как основным легирующим компонентом, а также с алюминием, кремнием, бериллием, свинцом и другими элементами, за исключением цинка. Оловянные бронзы знали и широко использовали ещё в древности. Большинство античных изделий из бронзы содержат 75–90 % меди и 25–10 % олова, что делает их внешне похожими на золотые, однако они более тугоплавкие. Это очень прочный сплав. Из него делали оружие до тех пор, пока не научились получать железные сплавы. С применением бронзы связана целая эпоха в истории человечества: Бронзовый век.
Латунь — это сплавы меди с Zn, Al, Mg. Это цветные сплавы с невысокой температурой плавления, их легко обрабатывать: резать, сваривать и паять.
Мельхиор — является сплавом меди с никелем, иногда с добавками железа и марганца. По внешним характеристикам мельхиор похож на серебро, но обладает большей механической прочностью. Сплав широко применяют для изготовления посуды и недорогих ювелирных изделий. Большинство современных монет серебристого цвета изготавливают из мельхиора (обычно 75 % меди и 25 % никеля с незначительными добавками марганца).
Дюралюминий, или дюраль — это сплав на основе алюминия с добавлением легирующих элементов — медь, марганец, магний и железо. Он характеризуется своей стальной прочностью и устойчивостью к возможным перегрузкам. Это основной конструкционный материал в авиации и космонавтике.

Химические свойства металлов
Металлы легко отдают электроны, т. е. являются восстановителями. Поэтому они легко реагируют с окислителями.
- Какие атомы являются окислителями?
- Как называются простые вещества, состоящие из атомов, которые способны принимать электроны?
Таким образом, металлы реагируют с неметаллами. В таких реакциях неметаллы, принимая электроны, приобретают обычно НИЗШУЮ степень окисления.
Рассмотрим пример. Пусть алюминий реагирует с серой:
Вопрос. Какой из этих химических элементов способен только отдавать электроны? Сколько электронов?
Алюминий — металл, имеющий на внешнем уровне 3 электрона (III группа!), поэтому он отдаёт 3 электрона:
Поскольку атом алюминия отдает электроны, атом серы принимает их.
Вопрос. Сколько электронов может принять атом серы до завершения внешнего уровня? Почему?
У атома серы на внешнем уровне 6 электронов (VI группа!), следовательно, этот атом принимает 2 электрона:
Таким образом, полученное соединение имеет состав:
В результате получаем уравнение реакции:

Задание 8.5. Составьте, рассуждая аналогично, уравнения реакций:
Составляя уравнения реакций, помните, что атом металла отдаёт все внешние электроны, а атом неметалла принимает столько электронов, сколько их не хватает до восьми.
Названия полученных в таких реакциях соединений всегда содержат суффикс ИД:
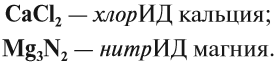
Корень слова в названии происходит от латинского названия неметалла (см. урок 2.4).
Металлы реагируют с растворами кислот (см. урок 2.2). При составлении уравнений подобных реакций и при определении возможности такой реакции следует пользоваться рядом напряжений (рядом активности) металлов:
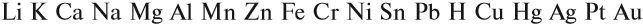
Металлы, стоящие в этом ряду до водорода, способны вытеснять водород из растворов кислот:
Задание 8.6. Составьте уравнения возможных реакций:
- магний + серная кислота;
- никель + соляная кислота;
- ртуть + соляная кислота.
Все эти металлы в полученных соединениях двухвалентны.
Реакция металла с кислотой возможна, если в результате её получается растворимая соль. Например, магний практически не реагирует с фосфорной кислотой, поскольку его поверхность быстро покрывается слоем нерастворимого фосфата:
Металлы, стоящие после водорода, могут реагировать с некоторыми кислотами, но водород в этих реакциях не выделяется:
Задание 8.7. Какой из металлов — Ва, Mg, Fе, Рb, Сu — может реагировать с раствором серной кислоты? Почему? Составьте уравнения возможных реакций.
Металлы реагируют с водой, если они активнее железа (железо также может реагировать с водой). При этом очень активные металлы (Li – Al) реагируют с водой при нормальных условиях или при небольшом нагревании по схеме:
где х — валентность металла.
Задание 8.8. Составьте уравнения реакций по этой схеме для К, Nа, Са. Какие ещё металлы могут реагировать с водой подобным образом?
Возникает вопрос: почему алюминий практически не реагирует с водой? Действительно, мы кипятим воду в алюминиевой посуде, — и… ничего! Дело, в том, что поверхность алюминия защищена оксидной пленкой (условно — Al2O3). Если её разрушить, то начнётся реакция алюминия с водой, причём довольно активная. Полезно знать, что эту плёнку разрушают ионы хлора Cl – . А поскольку ионы алюминия небезопасны для здоровья, следует выполнять правило: в алюминиевой посуде нельзя хранить сильно солёные продукты!
Вопрос. Можно ли хранить в алюминиевой посуде кислые щи, компот?
Менее активные металлы, которые стоят в ряду напряжений после алюминия, реагируют с водой в сильно измельчённом состоянии и при сильном нагревании (выше 100 °C) по схеме:
Металлы, менее активные, чем железо, с водой не реагируют!
Металлы реагируют с растворами солей. При этом более активные металлы вытесняют менее активный металл из раствора его соли:

Задание 8.9. Какие из следующих реакций возможны и почему:
- серебро + нитрат меди II;
- никель + нитрат свинца II;
- медь + нитрат ртути II;
- цинк + нитрат никеля II.
Составьте уравнения возможных реакций. Для невозможных поясните, почему они невозможны.
Следует отметить (!), что очень активные металлы, которые при нормальных условиях реагируют с водой, не вытесняют другие металлы из растворов их солей, поскольку они реагируют с водой, а не с солью:
А затем полученная щёлочь реагирует с солью:
Поэтому реакция между сульфатом железа и натрием НЕ сопровождается вытеснением менее активного металла:
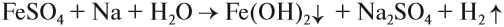

Коррозия металлов
Коррозия — самопроизвольный процесс окисления металла под действием факторов окружающей среды.
В природе практически не встречается металлов в свободном виде. Исключение составляют только «благородные», самые неактивные металлы, например золото, платина. Все остальные активно окисляются под действием кислорода, воды, кислот и др. Например, ржавчина образуется на любом незащищённом железном изделии именно в присутствии кислорода или воды. При этом окисляется железо:
а восстанавливаются компоненты атмосферной влаги:
В результате образуется гидроксид железа (II), который, окисляясь, превращается в ржавчину:
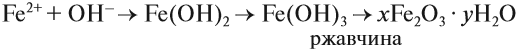
Подвергаться коррозии могут и другие металлы, правда, ржавчина на их поверхности не образуется. Так, нет на Земле металла алюминия — самого распространённого металла на планете. Но зато основу многих горных пород и почвы составляет глинозём Al2O3. Дело в том, что алюминий мгновенно окисляется на воздухе. Коррозия металлов наносит колоссальный ущерб, разрушая различные металлические конструкции.
Чтобы уменьшить потери от коррозии, следует устранить причины, которые её вызывают. В первую очередь, металлические предметы следует изолировать от влаги. Это можно сделать разными способами, например, хранить изделие в сухом месте, что далеко не всегда возможно. Кроме того, можно поверхность предмета покрасить, смазать водоотталкивающим составом, создать искусственную оксидную плёнку. В последнем случае в состав сплава вводят хром, который «любезно» распространяет собственную оксидную плёнку на поверхность всего металла. Сталь становится нержавеющей.
Изделия из нержавеющей стали дороги. Поэтому для защиты от коррозии используют тот факт, что менее активный металл не изменяется, т. е. не участвует в процессе. Поэтому если к сохраняемому изделию приварить более активный металл, то, пока он не разрушится, изделие корродировать не будет. Этот способ защиты называется протекторной защитой.

Выводы
Металлы — это простые вещества, которые всегда являются восстановителями. Восстановительная активность металла убывает в ряду напряжений от лития к золоту. По положению металла в ряду напряжений можно определить, как металл реагирует с растворами кислот, с водой, с растворами солей.
Атомы и молекулы. Химический элемент. Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура неорганических соединений

Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Молекулой называют наименьшую электронейтральную частицу вещества, способную к самостоятельному существованию и обладающую его химическими свойствами. Молекула представляет собой систему взаимодействующих между собой атомов, образующих определённую структуру с помощью химических связей.
Химический элемент — совокупность атомов, характеризующихся одинаковым значением (величиной) заряда ядра.
Ионами называют электрически заряженные частицы, возникающие при потере или присоединении электронов атомами или молекулами.
Катионами называют положительно заряженные ионы.
Анионами называют отрицательно заряженные ионы.
Вещество — любая совокупность атомов и молекул.
Свойства веществ (температуры плавления и кипения, плотность, цвет и т. д.) относятся к совокупности атомов или молекул.
По химическому составу неорганические вещества делят на простые и сложные.
Простыми называют вещества, которые образуют атомы одного и того же химического элемента (например, H2, O2).
Простые вещества делят на металлы и неметаллы.
Металлами называют простые вещества, которые обладают характерными металлическими свойствами, а именно высокой электро- и теплопроводностью и металлическим блеском.
Простые вещества, которые образуют атомы элементов-неметаллов, при нормальных условиях такими свойствами не обладают.
В периодической таблице Д.И. Менделеева неметаллы расположены в главных подгруппах справа вверху от условной диагонали, проведённой через бор и астат. В главных подгруппах слева от этой диагонали и во всех побочных подгруппах располагаются металлы.
Сложными называют вещества, которые состоят из атомов двух и более элементов (например, H2S, NO2).
Для выражения состава вещества используют различные химические формулы. При их написании используют общепринятые символы химических элементов. Символ элемента состоит из первой буквы или первой и одной из последующих букв латинского названия элемента, при этом первая буква всегда прописная, а вторая — строчная.
Названия и обозначения атомов совпадают с символами химических элементов. Например, О — атом кислорода, 2О — два атома кислорода, О2 — молекула кислорода, О3 — молекула озона.
Сложные вещества разделяют на условно электроположительную (катион) и условно электроотрицательную (анион) составляющие. В формуле сложного вещества вначале ставят катион, а затем — анион, например KBr, CuSO4. Названия сложного вещества читают справа налево, т. е. вначале называют его электроотрицательную составляющую в именительном падеже, а затем электроположительную в родительном падеже.
Для бинарных, т. е. состоящих из двух элементов соединений, действуют следующие правила. Если соединение состоит из металла и неметалла, то на первом месте всегда ставят металл (как более электроположительный элемент): K2S, BaCl2.
В формулах соединений, состоящих только из неметаллов, на первом месте всегда ставят элемент, находящийся левее в условном ряду неметаллов, построенном по их возрастающей электроотрицательности:
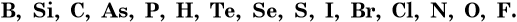
Например, IBr — бромид йода, CS2 — дисульфид углерода.
Формула молекулярная (брутто-формула) включает символы всех химических элементов, входящих в состав соединений. Около каждого символа ставят числовой индекс, показывающий, сколько атомов данного вида входит в состав соединения. Таким образом, молекулярная формула показывает качественный и количественный состав молекулы. Например, формула KNO3 показывает, что вещество состоит из 1 атома калия (индекс, равный 1, не ставится), 1 атома азота и 3 атомов кислорода.
Чтобы правильно прочитать формулу, надо знать как русские, так и латинские обозначения элементов. Называя вещество «вода», мы говорим, что его формула H2O (читается «аш два о»). Данное вещество состоит из двух атомов водорода и одного атома кислорода.
Называя вещество сульфат калия, K2SO4, мы читаем его формулу «калий два эс о четыре». Данное вещество состоит из двух атомов калия, одного атома серы и четырех атомов кислорода.
Если в формуле структурный фрагмент повторяется несколько раз, его заключают в круглые скобки и за скобками ставят числовой индекс, который произносят «дважды», «трижды», например, Ca(NO3)2 читается «кальций эн о три дважды», Mg3(PO4)2 читается «магний три пэ о четыре дважды».
Коэффициент, стоящий перед формулой вещества в уравнении реакции, читают как число, например: 3HNO2 — «три аш эн о два».
Оксидами называют класс химических соединений, состоящий из какого-либо элемента и атома кислорода со степенью окисления –2.
Называют оксиды, руководствуясь следующими правилами:
- Вначале указывают слово оксид, а затем в родительном падеже название второго элемента;
- Если элемент может образовать несколько оксидов, то после названия элемента в скобках указывают его валентность;
- При написании формул оксидов кислород всегда ставят на втором месте.
Примеры: K2O — оксид калия, N2O5 — оксид азота (V), CrO3 — оксид хрома (IV).
Для некоторых распространённых оксидов используют тривиальные названия, например CaO — негашеная известь, N2O — веселящий газ, CO — угарный газ, CO2 — углекислый газ.
Оксиды классифицируют так.
Низшими называют оксиды, в которых элемент проявляет низшую степень окисления, например MnO — оксид марганца (II).
Высшими называют оксиды, в которых элемент проявляет высшую степень окисления, например Mn2O7 — оксид марганца (VII).
Несолеобразующими, или безразличными, называют оксиды, не проявляющие ни основные, ни кислотные свойства, например N2O, NO, CO.
Солеобразующими называют группу кислотных, основных и амфотерных оксидов.
Основные оксиды образуют металлы в низших степенях окисления. Наиболее известные из них: Li2O, Na2O, K2O, Rb2O, Cs2O, MgO, CaO, SrO, BaO, Cu2O, Ag2O, HgO, CrO, FeO.
Амфотерными называют оксиды, которые проявляют как основные, так и кислотные свойства, в зависимости от другого реагента. Наиболее известные амфотерные оксиды Al2O3, Cr2O3, ZnO, BeO, PbO, SnO. Ряд оксидов, например CuО, Fe2O3, проявляет амфотерные свойства с преобладанием основных.
Существует несколько способов получения оксидов.
Реакции простых веществ с кислородом:
При взаимодействии сложных веществ с кислородом часто образуется смесь оксидов элементов:
Оксиды металлов реагируют с химически более активными металлами. При этом образуется новый оксид и новый металл:
Некоторые высшие оксиды получают доокислением низших оксидов, а ряд низших оксидов получают разложением высших оксидов:
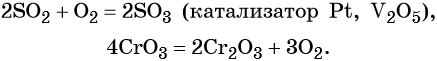
Иногда для получения оксидов используют реакции разложения солей и гидроксидов:
Основаниями называют класс химических соединений, которые состоят из катиона металла или иона аммония и одной или нескольких гидроксильных групп, способных к замещению на анионы.
Число гидроксильных групп определяет кислотность основания, например: NaOH — однокислотное, Mg(OH)2 — двухкислотное и т. д.
Щелочами называют растворимые в воде основания.
Сильные основания: гидроксиды щелочных и щёлочноземельных металлов LiOH, NaOH, KOH, RbOH, CsOH, Ba(OH)2, Ca(OH)2, Sr(OH)2. Слабые основания: все нерастворимые в воде гидроксиды металлов и гидрат аммиака.
Называют основания следующим образом:
- Вначале указывают слово гидроксид, а затем добавляют название металла в родительном падеже;
- Если элемент может образовывать несколько оснований, то после его названия в круглых скобках римской цифрой указывают валентность: KOH — гидроксид калия, Fe(OH)2 — гидроксид железа (II), Fe(OH)3 — гидроксид железа (III);
- При написании формул гидроксидов гидроксильную группу всегда ставят на втором месте.
Для некоторых распространённых гидрокидов используют тривиальные названия, например: Ca(OH)2 — гашёная известь; NaOH — едкий натр, или каустик.
Существуют следующие способы получения оснований:
Реакция основных оксидов с водой:
Взаимодействие некоторых металлов с водой:
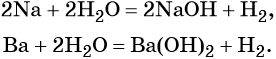
Реакция обмена между солями и основаниями:
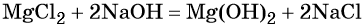
Первые два способа применяют для получения растворимых, а последний — для получения нерастворимых в воде оснований. Существуют и иные способы получения оснований.
Все растворы щелочей имеют pH > 7. При этих значениях pH происходит изменение окраски индикаторов: лакмуса — на синюю, фенолфталеина — на малиновую, метилового оранжевого — на жёлтую, что является качественным методом обнаружения щелочей. Более подробный материал о показателе pH будет изложен в уроке 24.
Кислотами называют класс химических соединений, которые содержат в своём составе один или несколько катионов водорода, способных замещаться на атомы металлов, и анионов кислотных остатков.
Основностью кислоты называют число способных замещаться на металл атомов водорода в её молекуле. По основности кислоты делят на одно-, двух- и трёхосновные, например HBr, H2S и H3PO4 соответственно.
В зависимости от элементного состава кислоты делят на бескислородные и кислородные, например HBr и H2SO3. Кислотный остаток — это структурный элемент молекулы кислоты, который выступает как единое целое в ходе химических реакций.
В таблице 4 приведены формулы и названия наиболее распространенных кислот и их солей.
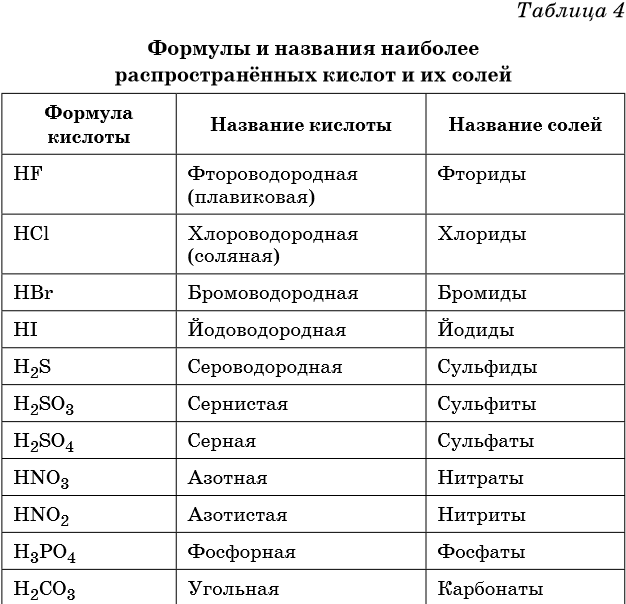

Сильные кислоты: HI, HBr, HCl, HClO3, HClO4, H2SO4, HNO3.
Кислородсодержащие кислоты и основания объединяют в общий класс гидроксидов.
Амфотерными называют гидроксиды, способные реагировать как с кислотами, так и с основаниями. Амфотерные гидроксиды: Al(OH)3, Cr(OH)3, Zn(OH)2, Pb(OH)2, Be(OH)2, Sn(OH)2. Некоторые гидроксиды, например Cu(OH)2, Fe(OH)3, проявляют амфотерные свойства с преобладанием основных.
Большинство кислородных кислот получают реакцией соответствующих оксидов с водой:
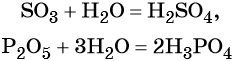
Некоторые кислоты получают из солей путём вытеснения более сильной кислотой, например:
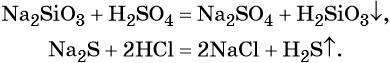
Бескислородные кислоты получают прямым взаимодействием неметалла с водородом либо действием более сильных кислот на соответствующие соли:
Солями называют класс химических соединений, которые представляют собой продукты взаимодействия кислот с основаниями.
По составу соли классифицируют на средние, кислые и основные.
Средними называют соли, которые состоят только из катиона металла или иона аммония и аниона кислотного остатка, например: CsBr, MgSO4.
Кислыми называют соли, которые наряду с катионом металла содержат катионы водорода, способные замещаться на другие катионы в ходе обменных реакций, например: LiHCO3 (гидрокарбонат лития), CaHPO4 (гидрофосфат кальция).
Основными называют соли, которые наряду с анионом кислотного остатка содержат одну или несколько гидроксильных групп, способных замещаться на анионы в ходе реакций обмена, например: Al(OH)2Br, Cu(OH)I.
При написании формул солей на первом месте ставят катион, а при написании названий — анион. Названия солей состоят из названия аниона в именительном падеже и названия катиона в родительном. Например, NaBr — бромид натрия, BaCO3 — карбонат бария. Если металл проявляет различные степени окисления, то в названиях степень окисления указывается римской цифрой: FeCl2 — хлорид железа (II), FeCl3 — хлорид железа (III). Кислые соли называют добавлением к аниону приставки гидро-, а если необходимо, то и соответствующего числительного, например: NaHCO3 — гидрокарбонат натрия, КH2PO4 — дигидрофосфат калия, Al(OH)2Br — дигидроксобромид алюминия, Cu(OH)I — гидроксойодид меди (II).
Основные соли называют добавлением приставки гидроксо- к названию кислотного остатка, указывая, если необходимо, соответствующее числительное: Mg(OH)Cl — гидроксохлорид магния, Al(OH)2Cl — дигидроксохлорид алюминия.
Существует множество путей получения солей. Приведём наиболее важные из них.
Реакция нейтрализации, т. е. взаимодействие кислот и оснований, взаимодействие кислот с основными и амфотерными оксидами и реакция оснований с кислотными оксидами:
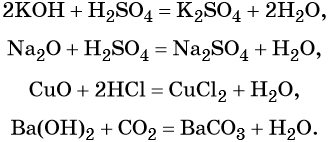
Взаимодействие кислот или щелочей с солями:
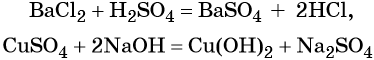
Взаимодействие металлов с неметаллами, кислотами, солями:
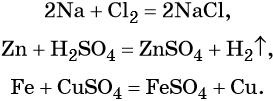
Взаимодействие основных и кислотных оксидов:
По своим физическим свойствам соли — твёрдые кристаллические вещества, часто имеющие высокие температуры плавления. По растворимости в воде соли делятся на растворимые (более 1 г вещества на 100 г воды), малорастворимые (от 0,1 до 1 г вещества на 100 г воды) и нерастворимые (менее 0,1 г вещества на 100 г воды). В воде растворимы все соли азотной и уксусной кислот.
Тренировочные задания
1. Кислотой и амфотерным гидроксидом соответственно являются
2. Основанием и кислотным оксидом соответственно являются
3. Кислой солью и несолеобразующим оксидом соответственно являются
4. Гидроксидом и щёлочью соответственно являются
5. Вещество, химическая формула которого Cr2(SO4)3, имеет название
1) сульфат хрома (III)
2) сульфит хрома (III)
3) сульфат хрома (II)
4) сульфит хрома (II)
6. Вещество, химическая формула которого CaHPO4, называется
1) фосфат кальция
2) гидрофосфат кальция
3) дигидрофосфат кальция
4) фосфид кальция
7. К простым веществам относится
1) поваренная соль
2) кислород
3) оксид кремния
4) пищевая сода
8. К простым веществам относится
1) поташ
2) углекислый газ
3) веселящий газ
4) бром
9. К сложным веществам относится
1) поташ
2) сера
3) озон
4) бром
10. К сложным веществам относится
1) фтор
2) фосфор
3) углекислый газ
4) бром
11. Только основные оксиды приведены в списке
12. Только несолеобразующие оксиды приведены в списке
13. В перечне веществ, формулы которых: А) H2O В) HNO3 Д) CaO Б) N2O Г) H2SO4 Е) NaOH к оксидам относятся
1) АБВ
2) АБД
3) БВД
4) БДЕ
14. В перечне веществ, формулы которых: А) CaO В) Cr2O3 Д) SrO Б) Fe2O3 Г) NO Е) Li2O к основным оксидам относятся
1) АБВ
2) АБД
3) БВД
4) АДЕ
15. В перечне веществ, формулы которых: А) CO2 В) SO2 Д) SrO Б) CrO3 Г) Cr2O3 Е) CrO к кислотным оксидам относятся
16. В перечне веществ, формулы которых: А) CrO В) ZnO Д) Al2O3 Б) CrO3 Г) Cr2O3 Е) NO к амфотерным оксидам относятся
1) АБВ
2) АВД
3) ВГД
4) АДЕ
1) АБВ
2) БВГ
3) БВД
4) АБД
18. В перечне веществ, формулы которых: А) HCl В) (NH4)2HPO4 Д) H3PO4 Б) HNO3 Г) NH4HSO4 Е) Ca(HCO3)2 к кислотам относятся
Урок 3. Молекулы и простые вещества
Читайте также:
